обмен веществ
ОБМЕН ВЕЩЕСТВ (метаболизм)
совокупность хим. процессов, обеспечивающих жизнедеятельность организма. Хим. превращ. в организме осуществляются в двух противоположных направлениях-синтез сложных соед. из более простых (а н а б о л и з м, или а с с и м и л я ц и я) и расщепление сложных соед. до более простых (к а т а б о л и з м, или д и с с и м и л я ц и я).
Первонач. представления об О. в. возникли в связи с изучением процессов обмена между организмами и внеш. средой (т. наз. внешний, или общий, О. в.). Послед. исследования превращений веществ внутри организма привели к представлениям о в н у т р е н н е м, или п р о м е ж у т о ч н о м, О. в.
Во внутреннем и внешнем О. в. принято различать структурный (пластический) и энергетический обмены. В структурном обмене рассматривают превращения разл. соед. в организме, их перенос (транспорт) внутри организма и между организмом и средой. В энергетич. обмене рассматривают превращения хим. энергии, образующейся в О. в., в тепло, мышечную работу, а также механизмы ее использования в активном транспорте, биосинтезе и др.
В соответствии с природой участвующих в О. в. соед. различают орг. обмен (обмен углеводов, липидов, азотсодержащих соед. и др.) и минер. обмен (водно-солевой обмен и обмен микроэлементов); в физиологии выделяют также газовый обмен. О. в. с участием свободного O2 наз. а э р о б н ы м, без участия O2-а н а э р о б н ы м. Ввиду различий О. в. у организмов, принадлежащих к разл. таксономич. группам, выделяют О.в. растений, животных, микроорганизмов, а также более мелких таксономич. единиц, напр. О.в. млекопитающих, злаковых, дрожжей, человека, бактерии Escherichia coli. При изучении О.в. учитывают половые и возрастные различия, а также отклонения в О.в., вызванные влиянием внеш. среды и питания. Раздельно рассматривают О.в. в разл. тканях и органах. Устойчивые отклонения О.в. от нормы квалифицируют как болезни О.в.
Структурный обмен
В зависимости от того, в какой хим. форме живые организмы способны усваивать из внеш. среды углерод, они делятся на две большие группы-а в т о т р о ф ы и г е т е р о-т р о ф ы. Для первых осн. источником углерода служит CO2, для вторых-разл. орг. соединения. Автотрофное питание осуществляют зеленые растения и фотосинтезирующие бактерии, гетеротрофное — животные и грибы. У микроорганизмов встречаются тот и др. типы питания. О.в. автотрофных организмов является по преимуществу анаболическим, гетеротрофных — катаболическим. Основу пластического обмена составляет органический обмен. Традиционное разделение его на углеводный обмен, липидный обмен и обмен азотсодержащих соединений обусловлено большой распространенностью в живой природе соед. этих классов и различием их свойств.
Субстратами орг. обмена являются вещества, поступающие из внеш. среды, и вещества внутр. происхождения. В процессе О.в. часть конечных продуктов выводится во внеш. среду, др. часть используется организмом. Конечные продукты орг. обмена в тканях, способные накапливаться или расходоваться в зависимости от условий существования организма (напр., триацилглицерины, гликоген, крахмал, проламины), наз. запасными, или резервными, веществами. Если скорость поглощения субстратов превосходит скорость выведения конечных продуктов, то анаболизм преобладает над катаболизмом и организм развивается или накапливает резервные вещества. При равенстве этих скоростей рост организма прекращается и О.в. переходит в состояние, близкое к стационарному. В случае превышения скорости выведения конечных продуктов над скоростью потребления после истощения запаса резервных веществ организм обычно погибает. Последнее наблюдается при искусств. ограничении потребления внеш. субстратов (напр., алиментарная дистрофия при голодании животных, самосбраживание дрожжей в условиях дефицита углеводов) или в естеств. условиях (напр., при интенсивном дыхании плодов и семян растений).
Гл. катаболич. процесс в О. в. — биол. окисление (совокупность реакций окисления, протекающих во всех живых клетках, -дыхание и окислительное фосфорилированиё ). Интегральной характеристикой биол. окисления служит дыхат. коэф., который представляет собой отношение объема выделенного организмом CO2 к объему поглощенного O2. При окислении углеводов объем расходуемого O2 соответствует объему образующегося CO2 и поэтому дыхат. коэф. в этих случаях равен единице. При окислении жиров и белков такое соответствие отсутствует, т. к. кроме окисления углерода до CO2 часть O2 расходуется на окисление водорода с образованием воды. Вследствие этого величины дыхат. коэф. в случае окисления жиров и белков составляют соотв. ок. 0,7 и 0,8. Подавляющая часть белкового азота при окислении белка в организме млекопитающих переходит в мочевину. Поэтому по дыхат. коэф. и данным о количестве выделяемой мочевины у млекопитающих можно определять соотношение участвующих в биол. окислении углеводов, жиров и белков.
Осн. анаболич. процессом, противоположным биол. окислению, является осуществляемый автотрофами фотосинтез орг. соед. из CO2 и воды. Вместе с тем автотрофы осуществляют частичное окисление продуктов фотосинтеза. Для характеристики их общего О.в. также используют дыхат. коэффициент.
Последовательности реакций в организме, в которых осуществляется превращ. субстратов в конечные продукты О.в., наз. п у т я м и О. в., или м е т а б о л и ч. п у т я м и, а вещества, участвующие в этих реакциях,-м е т а б о л и т а м и. В зависимости от характера превращ. субстратов метаболич. пути подразделяют на анаболические и катаболические. Обратимые участки метаболич. путей, состоящие из равновесных реакций и используемые организмами как для синтеза, так и для расщепления сложных соед., наз. а м ф и б о л и ч е с к и м и. Подавляющую часть реакций, составляющих метаболич. пути, катализируют ферменты. Для своего функционирования мн. ферменты нуждаются в низкомол. соед., наз. коферментами. У высших животных большая часть коферментов (или их непосредственных предшественников) поступает в организм с пищей в виде незаменимых факторов питания-витаминов.
В простых случаях стационарность О.в. обеспечивают метаболич. пути, образованные линейными последовательностями реакций (напр., гликолиз, синтез и расщепление жирных кислот). Если метаболич. пути включают реакции, в которых образуются вещества, не выводимые во внеш. среду, то стационарность О.в. поддерживается дополнит. реакциями, обеспечивающими регенерирование этих веществ в предшествующие метаболиты. В результате метаболич. пути принимают вид циклич. последовательностей реакций (см., напр., трикарбоновых кислот цикл, глиоксилатный цикл).
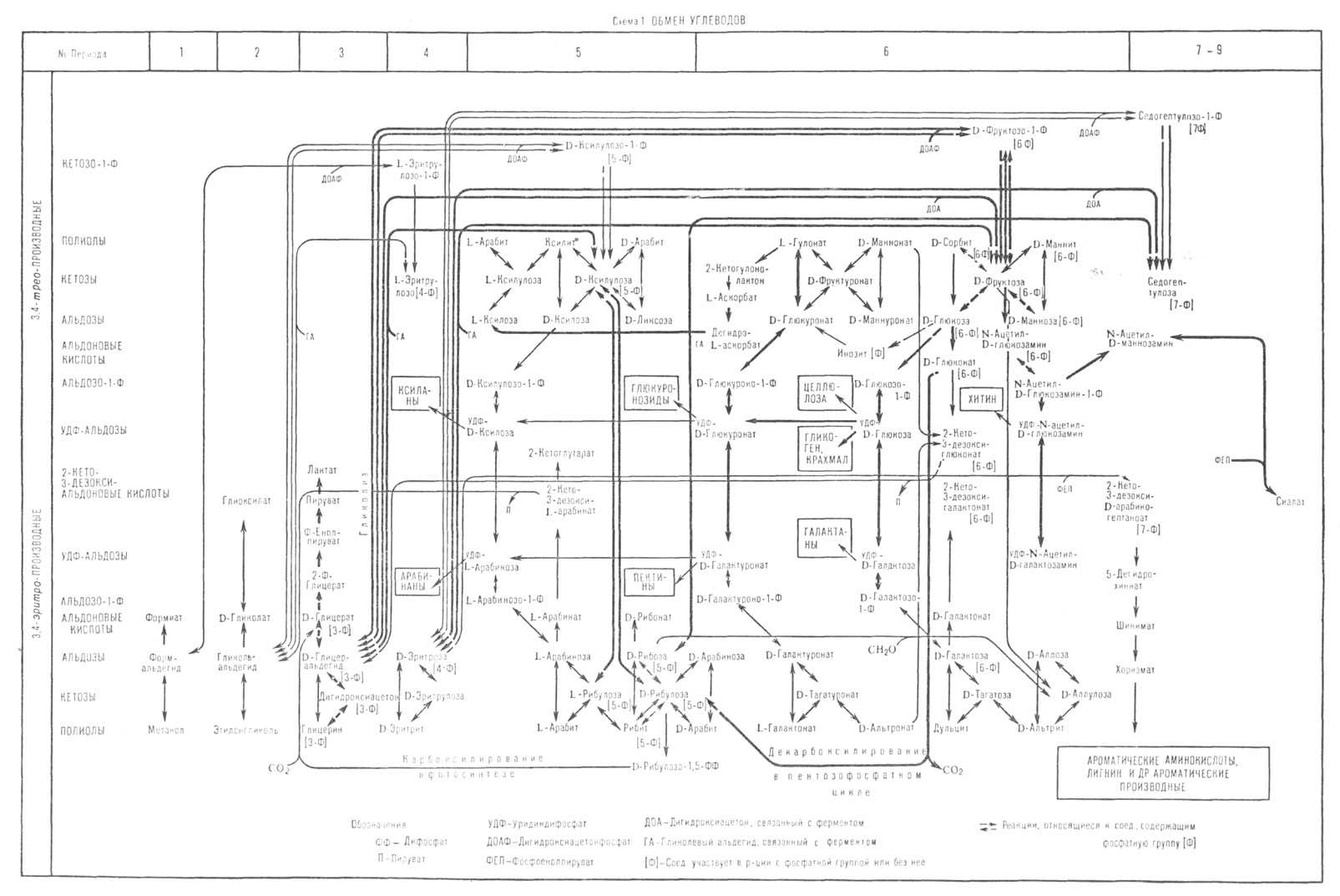
Разл. метаболич. пути включают много общих промежут. соед. и поэтому образуют единую сеть реакций, которая обнаруживает структурную регулярность. Эта регулярность, обусловленная наличием большого количества сходных реакций у метаболитов с одинаковыми функц. группами, отражена в схемах 1–3. Эти схемы объединяют данные по О.в. у животных, растений и микроорганизмов. Реакции О.в. человека и близких по О.в. млекопитающих выделены жирными стрелками. Соед. с одинаковыми функциональными группами размещены на схемах на одной горизонтали в порядке увеличения числа атомов С в скелете их молекул. По вертикали схемы разделены на участки, связанные сходными реакциями и включающие соед. с одинаковым числом атомов С в скелете. Эти участки, соответствующим образом пронумерованные, названы периодами (номер периода соответствует числу атомов С в скелете молекулы). Смежные периоды имеют сходную структуру; соед., занимающие в них соответствующее положение, являются гомологами. Назв. и формулы некоторых кислот, встречающихся в тексте и на схемах 1–3, приведены в таблице.
О б м е н у г л е в о д о в. Важнейший метаболич. путь в обмене углеводов — гликолиз, в котором осуществляется превращение гексоз в две молекулы лактата. Этот путь широко представлен в тканях животных и обеспечивает двигат. функцию скелетных мышц. В печени амфиболич. реакции этого пути участвуют в глюконогенезе-биосинтезе глюкозы из образующегося в мышцах лактата. Гликолиз рассматривают в качестве осн. пути, связывающего углеводный обмен с обменом карбоновых кислот и липидов. К модификации гликолиза относят путь спиртового брожения. В отсутствие свободного О 2 дрожжи по этому пути количественно расщепляют глюкозу на этанол и CO2, осуществляя т. наз. анаэробное дыхание.
НАЗВАНИЯ И ФОРМУЛЫ НЕКОТОРЫХ КИСЛОТ, ВСТРЕЧАЮЩИХСЯ В ТЕКСТЕ И НА СХЕМАХ 1–3


Важную роль в катаболизме углеводов играет пентозофосфатный цикл. Ключевые реакции этого пути — окисление глюкозо-6-фосфата до 6-фосфоглюконата и декарбоксилирование последнего с образованием CO2, воды и рибулозо-5-фосфата. Благодаря цикличности этого процесса обеспечивается стационарность окисления глюкозы в тканях. Так же как и в случае гликолиза, равновесные реакции этого пути составляют амфиболич. участок, который наряду с реакцией карбоксилирования рибулозо-1,5-дифосфата обеспечивает при фотосинтезе у зеленых растений обратный процесс-биосинтез глюкозы из CO2 и воды. При этом глюкоза в результате ферментативного превращ. в олиго- и полисахариды выводится из сферы О.в. в виде крахмала, целлюлозы и др.
С реакциями пентозофосфатного цикла связан метаболизм входящих в состав нуклеиновых кислот пентоз, а также биосинтез углеводных предшественников биополимера лигнина и ароматич. аминокислот.
Осн. углеводным субстратом в О.в. человека и высших животных служит глюкоза. Она сохраняется в виде резервного полисахарида гликогена в печени и частично в мышцах. Восстановление запасов гликогена происходит благодаря его синтезу из глюкозы, образуемой при глюконеогенезе или поступающей в кровоток через стенки кишечника. В последний глюкоза попадает в результате гидролиза крахмала пищ. продуктов амилазой слюны и ферментами желудочно-кишечного тракта.
Наряду с крахмалом высшие животные усваивают гликоген, некоторые олигосахариды и дисахариды, напр. сахарозу, мальтозу, лактозу и др. Специализир. микроорганизмы могут расщеплять ксилан, целлюлозу, хитин, лигнин и др. устойчивые полисахариды. Способность жвачных животных усваивать целлюлозу и ксилан обусловлена жизнедеятельностью микрофлоры, обитающей в сложном желудке животных.
На схеме 1 показаны осн. пути обмена углеводов. В ее верх. части представлены моносахариды и их производные с трео-конфигурацией в положении 3–4. В ниж. части размещены ряды соед. тех же классов, но с эритро-конфигурацией в этом же положении. Высшие моносахариды образуются из низших в обратимых реакциях конденсации с соед., содержащими в молекуле два или три атома С. В реакциях, катализируемых транскетолазами и соединяющих периоды n и п + 2 схемы (начиная с п = 2), из D-альдоз ниж. ряда образуются 3,4-D-трео-кетозы верх. ряда, имеющие углеродный скелет на два атома С больше, чем исходные альдозы. В реакциях конденсации D-альдоз с соед., содержащими три атома С, обеспечивающих связь между периодами n и n + 3, углеродный скелет увеличивается на 3 атома С. Пентозы образуются в результате декарбоксилирования уридиндифосфатных (УДФ) производных уроновых кислот. Переход от 3,4-D-mpeo-моносахаридов к 3,4-D-эритро-моносахаридам (периоды 5 и 6) осуществляется эпимеризацией соответствующих кетоз и УДФ-альдоз. Реакции окисления альдоз в альдоновые кислоты, дегидратации альдоновых кислот до 2-кето-3-дезоксиальдоновых кислот и расщепления последних на соответствующие альдозы и пируват составляют пути распада углеводов у микроорганизмов.
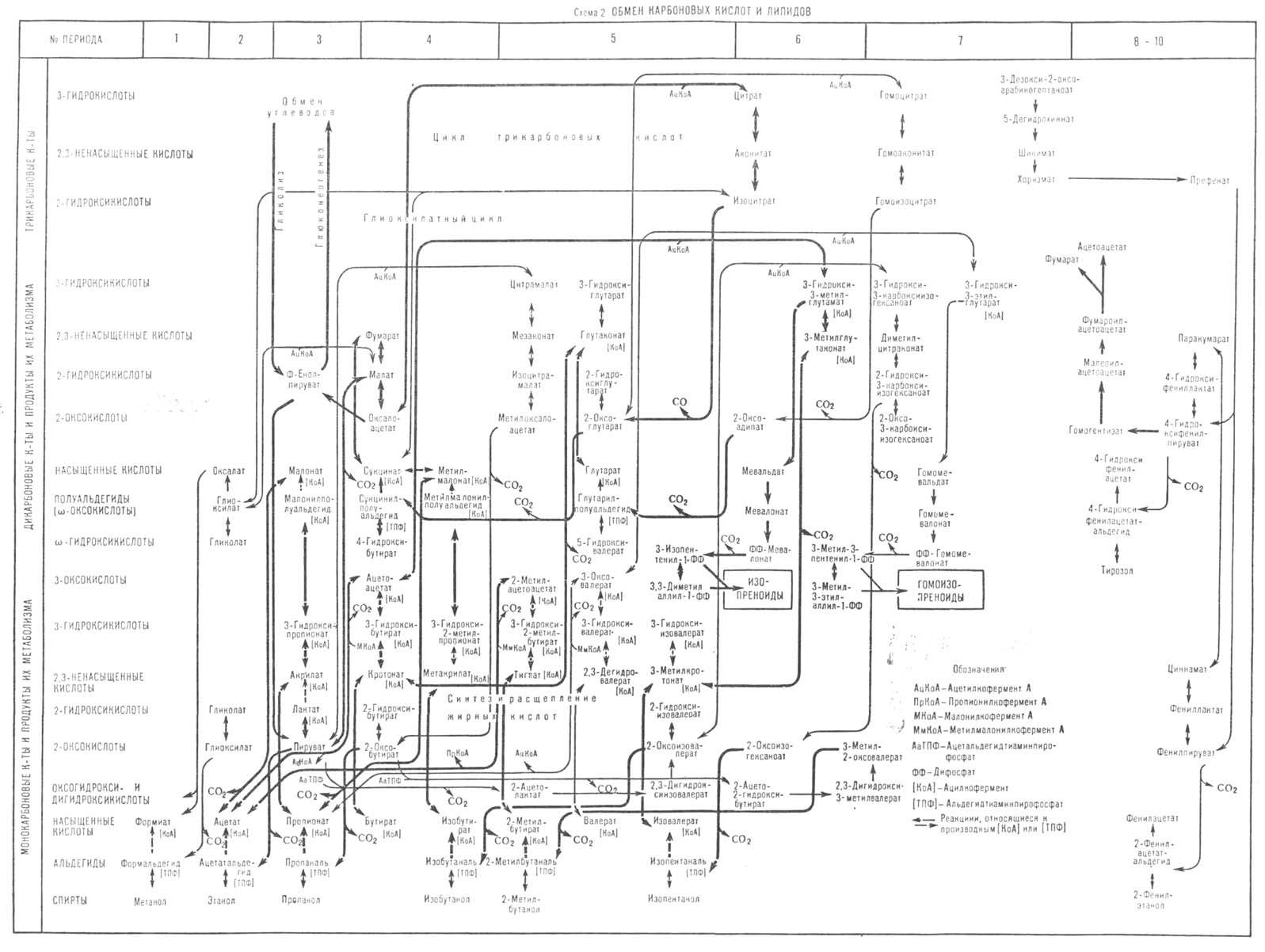
О б м е н к а р б о н о в ы х к и с л о т и л и п и д о в. Обмен этих веществ тесно связан с обменом углеводов. Образующийся на предпоследней стадии гликолиза пируват в результате окислит. декарбоксилирования превращ. в ацетилкофермент А (АцКоА; см. пантотеновая кислота). Т. к. АцКоА является непосредств. предшественником в биосинтезе жирных кислот и изопреноидов, гликолиз и окислит. декарбоксилирование служат путем, в котором осуществляется превращ. углеводов в липиды. Наиболее распространенными липидами в организме животных являются триацилглицерины и некоторые изопре-ноиды. К последним относятся стероиды (гл. обр. холестерин и его производные) и каротиноиды.
Обратный процесс-биосинтез углеводов из жиров-для животных не характерен. У растений и микроорганизмов он протекает в глиоксилатном цикле. В последнем из образующегося в результате расщепления жирных кислот АцКоА синтезируется сукцинат, который в результате реакций окисления и декарбоксилирования превращ. в фосфоенолпируват. Далее из фосфоенолпирувата на амфиболич. участке пути гликолиза образуются углеводы.
Катаболич. путь утилизации АцКоА состоит в окислении содержащегося в нем остатка уксусной кислоты в цикле три-карбоновых кислот до CO2 и воды. При дефиците углеводов АцКоА для осуществления их биосинтеза образуется в результате расщепления жирных кислот или некоторых аминокислот. Таким образом, у мн. организмов цикл трикарбоновых кислот служит общим завершающим механизмом окисления углеводов, жиров и белков. В то же время у растений в условиях фотосинтеза т. наз. обращенный цикл трикарбоновых кислот может, подобно пентозофосфатному циклу, выполнять анаболическую функцию — превращ. CO2 в органические соединения.
Осн. метаболич. пути в обмене карбоновых кислот и липидов приведены на схеме 2. На ней показаны превращения три-, ди- и монокарбоновых кислот, а также их производных. Общим путем биосинтеза ди- и трикарбоновых кислот служат реакции конденсации соответствующих моно- и дикарбоновых кислот с АцКоА или глиоксилатом. Три-, ди- и монокарбоновые кислоты переходят соотв. в ди-, монокарбоновые кислоты и альдегиды в реакциях декарбоксилирования. Связь между соед. внутри периодов осуществляется в реакциях окисления и восстановления карбонильных групп (соотв. до карбоксильных и гидроксильных), в обратимых реакциях дегидратации гидроксикислот в 2,3-ненасыщ. кислоты и гидрирования 2,3-ненасыщ. кислот в насыщенные. В перечисл. реакциях образуются и расщепляются алифатич. 2-оксокислоты — предшественники соответствующих аминокислот. Углеродные скелеты оксокислот-предшественников валина и изолейцина (в периодах 5 и 6) — образуются в реакциях конденсации соотв. пирувата и 2-оксо-бутирата с активным ацетальдегидом (продукт тиаминза-висимого декарбоксилирования пирувата-a-гидроксиэтил-тиаминопирофосфат; см. тиамин). Реакции оксопредшествен-ников ароматич. аминокислот представлены в периодах 7–10. Превращения дикарбоновых и трикарбоновых кислот в верх. части периодов 4–6 составляют цикл трикарбоновых кислот и глиоксилатный цикл. В ниж. части схемы представлены начальные этапы путей биосинтеза и расщепления линейных и разветвленных жирных кислот. Первые наращивают углеводородную цепь благодаря конденсации с ацетильным фрагментом малонил-кофермента А, переходя из периода n в п + 2, вторые — в аналогичной реакции с пропионильным фрагментом метилмалонил-коферментом А, переходя из периода n в п + 3. В периодах 6 и 7 приведены пути биосинтеза мевалоната и гомомевалоната — предшественников соотв. изопреноидов (терпенов, стероидов, каротино-идов и др.) и реже встречающихся гомоизопреноидов (напр., ювенильный гормон насекомых).
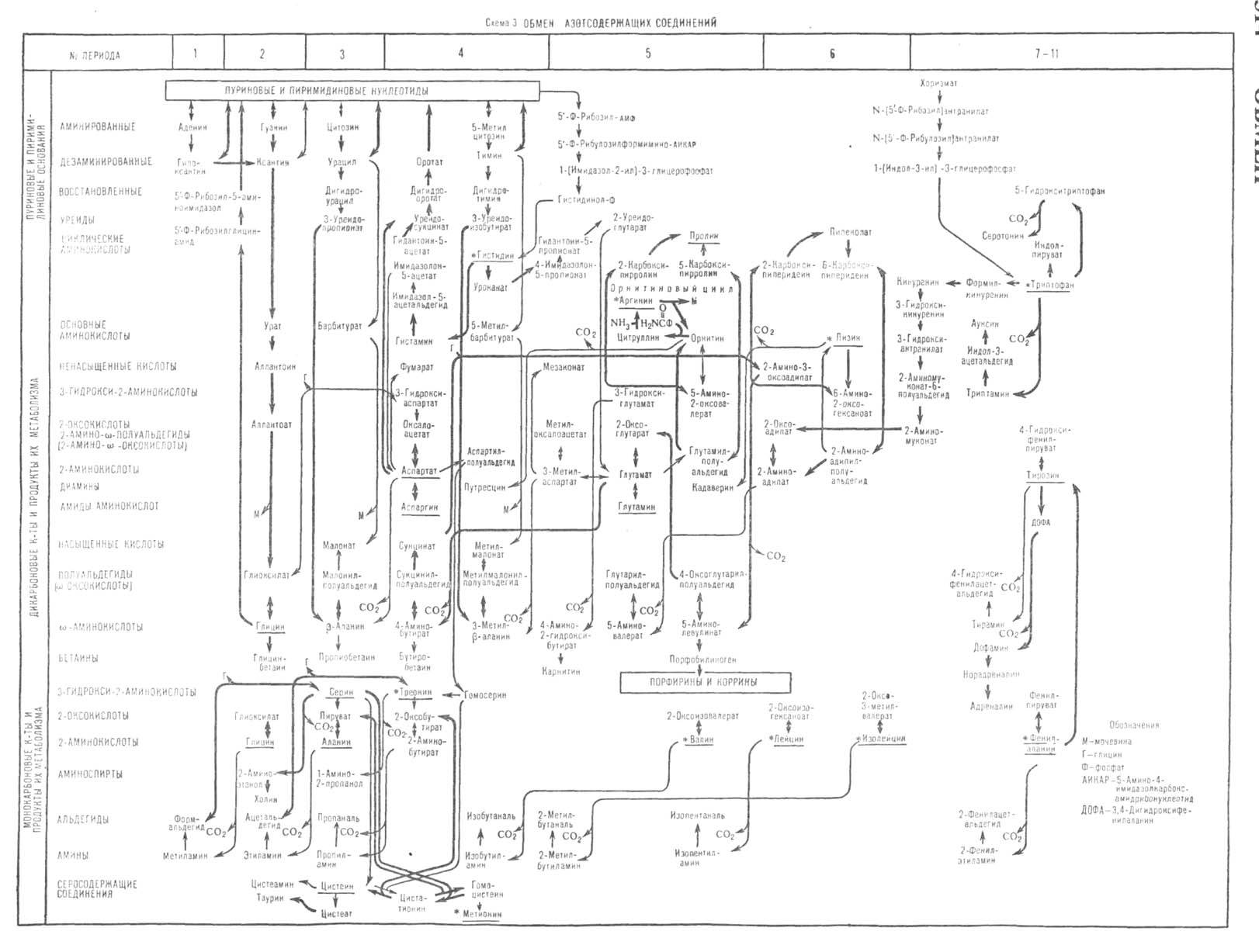
О б м е н а з о т с о д е р ж а щ и х с о е д и н е н и й. Первичный источник азота в О. в. — атмосфера. Непосредственно использовать своб. азот могут мн. виды бактерий. Однако большая часть микроорганизмов и все животные и растения усваивают лишь связанный азот в виде солей аммония, нитритов, нитратов или продуктов расщепления белков. Основу внутр. азотистого обмена составляют биосинтез и расщепление белков, нуклеиновых кислот и порфиринов. Аминокислоты в организме образуются в реакциях восстановит. аминирования или переаминирования a-оксокислот. Белки включают лишь 20 из всех встречающихся в живой природе аминокислот, наз. протеиногенными. Из них в организме высших животных синтезируется примерно половина. Др. половина относится к незаменимым и в организм поступает только с пищей. Синтез полилептидной цепи белка из аминокислот (трансляция) осуществляется рибосомой. Последовательность аминокислот в белке определяется последовательностью триплетов генетич. кода в матричной РНК.
Катаболизм белков у всех организмов начинается с их расщепления по пептидным связям протеолитич. ферментами. В желудочно-кишечном тракте животных белки гидро-лизуются трипсином, химотрипсином, пепсином и др. ферментами до своб. аминокислот, которые всасываются стенками кишечника и попадают в кровоток. Часть аминокислот подвергается дезаминированию до оксокислот, претерпевающих дальнейшее расщепление, др. часть используется печенью или тканями организма для биосинтеза белков. У млекопитающих отщепляющийся от аминокислот аммиак превращ. в орнитиновом цикле в мочевину. Этот процесс осуществляется в печени. Образующаяся мочевина вместе с др. растворимыми продуктами О.в. выводится из кровотока почками.
У человека половина всех тканевых белков расщепляется и строится заново в среднем в течение 80 сут, белки печени и сыворотки крови наполовину обновляются каждые 10 сут, белки мышц-каждые 180 сут, отдельные ферменты печени-каждые 2–4 ч.
Нуклеиновые кислоты-продукты углеводного и азотистого обмена. ДНК образуется в клетке в результате репликации или обратной транскрипции из дезоксирибонуклеозидтри-фосфатов, РНК — в результате транскрипции из рибонуклео-зидтрифосфатов. Нуклеиновые кислоты выполняют функции хранителей и переносчиков наследств. информации, закодированной в последовательности четырех разл. оснований в цепочках нуклеиновых кислот. Эта информация реализуется в структуре белка. Через ферментативные и структурные функции белка она определяет наследуемые особенности О.в. организмов. Катаболизм нуклеиновых кислот состоит в их гидролизе нуклеазами до нуклеотидов, которые затем расщепляются на составляющие их фосфат, пентозы, пури-новые и пиримидиновые основания. При этом пуриновые основания окисляются до мочевой кислоты, которая у млекопитающих расщепляется до глиоксилата и мочевины. Пиримидиновые основания в организме животных расщепляются до b-аланина и 3-аминоизобутирата.
Исходными субстратами в биосинтезе порфириновых соед. служат сукцинат и глицин. Порфириновые соед. выполняют в О.в. важные функции, принимая участие в окислительно-восстановит. процессах. В частности, в составе тема в гемоглобине порфириновое кольцо участвует в переносе O2 в крови. Порфириновое кольцо входит в состав цитохромов и хлорофиллов. Катаболизм порфиринов в животном организме состоит в раскрытии и частичной деградации пор-фиринового кольца. Продукты катаболизма в виде окраш. соед. (биливердина, билирубина и др.) наряду с продуктами частичного окисления стероидов (холевыми кислотами) выводятся через желчные протоки в кишечник.
На схеме 3 показаны превращения пуриновых и пири-мидиновых оснований, уреидов карбоновых кислот, а также дикарбоновых и монокарбоновых аминокислот и их производных. Протеиногенные аминокислоты на схеме подчеркнуты (незаменимые для человека аминокислоты отмечены звездочкой). Основной путь биосинтеза мочевины у млекопитающих (орнитиновый цикл) представлен в периоде 5. Реакции образования и расщепления пуриновых и пиримидиновых оснований размещены в периодах 2–4 в верх. части схемы (для этих групп соед. периоды не всегда соответствуют количеству атомов С в скелете молекулы). В средней части схемы показан путь биосинтеза предшественников порфириновых и корриновых соед.-d-аминолевулиновой кислоты и порфо-билиногена из глицина и сукцината.
Взаимоотношение между обменом углеводов, липидов и карбоновых кислот, а также азотсодержащих соед. показано на схеме 4.
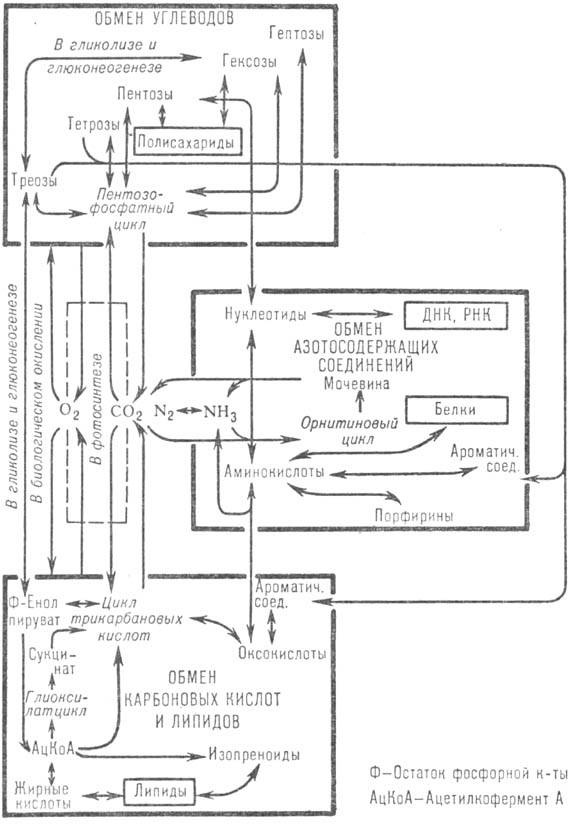
Схема 4. Обобщенная схема обмена веществ.
М и н е р. о б м е н. Под минер. обменом понимают процессы усвоения, превращ. и выведения организмом неорг. веществ. Поскольку такие неорг. вещества, как вода, CO2, NH3, фосфаты, сульфаты, иод и др., включаются при О.в. в орг. соед., между орг. и минер. обменами четкая граница отсутствует. Наиб. уд. вес в минер. обмене занимает водно-солевой обмен, в котором принимают участие катионы (Na+ , K+, Ca2+ , Mg2+) и анионы (Cl−, HPO42−, НCO3−, SO42−). В результате активного трансмембранного переноса ионы Na+ непрерывно удаляются из клеток в межклеточную среду, а замещающие их ионы К+ концентрируются внутри клеток. Ионы Ca2+ у животных участвуют в проведении нервного импульса, поэтому постоянство их концентрации в организме имеет существ. значение для нормального функционирования нервной системы. У позвоночных животных Ca2+ и фосфат HPO42− в виде кальциевых солей фосфорной кислоты служат главными компонентами костной ткани. Из карбонатов Ca и Mg беспозвоночные строят раковины. У растений Mg2+ входит в состав хлорофилла. Сульфатная группа-фрагмент желчных кислот и хондроитинсульфата хрящей. В организме сульфат образуется в результате окисления сульфгидрильных групп цистеина и гомоцистеина. Водно-солевой обмен обеспечивает постоянство ионного состава, осмотич. давления, pH и объема жидкостей организма. Потребность взрослого человека в Na+, K+, Ca2+, Mg2+ , Cl− и HPO42−составляет соотв. 215, 75, 60, 35, 25 и 105 мг/сут. Выведение из организма растворимых минер. продуктов О.в., так же как и органических, осуществляется у человека и животных почками.
Функция мн. металлов (напр., железа, меди, цинка, кобальта, молибдена) в О.в. состоит в их участии в биохим. реакциях в качестве коферментов. Иод участвует в О.в. в составе гормона тироксина. Большая часть из перечисл. элементов присутствует в организме в концентрации меньшей, чем 10−3%, и относится к микроэлементам. Особо в О.в. рассматривают минер. питание растений. Соли аммония, калия, нитраты, фосфаты и микроэлементы широко используют в качестве удобрений, улучшающих рост и увеличивающих продуктивность растений.
Энергетический обмен
Движущей силой О.в. служит разность термодинамич. потенциалов участвующих в реакциях соединений. По источникам используемой при О.в. энергии организмы делят на ф о т о т р о ф ы и х е м о т р о ф ы. У первых роль богатых энергией субстратов выполняют эндогенные продукты начального этапа фотосинтеза, у вторых-разл. соед. экзогенной природы. Если в качестве субстратов окисления хемотрофы используют орг. соед., то их относят к х е м о о р г а н о т р о-ф а м, если неорганические (напр., H2, NH3, CO, H2S) — к л и т о т р о ф а м.
В рамках общего О.в. изучение энергетич. обмена у фототрофов состоит в определении энергетич. параметров фотосинтеза, у хемотрофов — в исследовании баланса между энергией, выделяемой при расщеплении субстратов О.в., и энергией, расходуемой на биосинтез конечных продуктов О.в., на совершение мех. работы, а также рассеиваемой в виде тепла. В общем энергетич. обмене животных выделяют о с н. о б м е н-миним. количество энергии, необходимое для поддержания жизни организма в состоянии покоя. У взрослого человека он составляет 1600–1700 ккал/сут (6700–7100 кДж/сут). Количество тепла, выделяемое теплокровными животными при осн. обмене, пропорционально поверхности их тела (правило Рубнера). Более точно теплопродукция (в ккал/сут) организма животных выражается формулой W = = 70 М0,75 (М-масса тела в кг). Данные об общем энергетич. обмене используют для вычисления калорийности продуктов питания и составления сбалансированных по энергозатратам организма рационов питания.
Мол. механизмы генерирования и утилизации энергии на промежут. этапах О.в. изучает биоэнергетика, которая рассматривает сопряжение биол. окисления с фосфорилированием. Это обусловлено тем, что своб. энергия гидролиза осн. продукта фосфорилирования-АТФ и в меньшей степени др. фосфатных производных, напр. гуанозинтрифосфата, креатинфосфата,-обеспечивает в сопряженных реакциях синтез сложных соед., мышечное сокращение, транспорт соед. через биол. мембраны против градиента концентрации (активный транспорт), создание на мембране электрич. потенциала, разряд которого, в частности, обеспечивает проведение нервного импульса и др. биоэлектрич. явления. Энергия гидролиза АТФ может также трансформироваться в световую энергию или служить в организме источником тепла.
Различают субстратное фосфорилирование, состоящее в фосфорилировании молекул субстрата при их окислении никотинамидными коферментами (см. ниацин) и окислит. фосфорилирование, наблюдаемое на стадии образования АТФ из аденозиндифосфата (АДФ) при переносе электронов (атомов водорода) по цепи коферментов в процессе дыхания и в фотосинтезе. Пример субстратного фосфорилирования — катализируемая в гликолизе глицсральдегидфосфат-дегидрогеназой реакция образования D-1,3-дифосфоглицери-новой кислоты (НО)2Р(О)OCH2CH(OH)C(O)ОР(О)(OH)2 из не-орг. фосфата и D-глицеральдегид-3-фосфата. Фосфатная группа в положении 1 этого соед. с помощью фермента фосфоглицераткиназы может переходить к АДФ, образуя АТФ. Субстратное фосфорилирование более характерно для организмов, живущих в анаэробных условиях. Объектом для переноса электронов (атомов водорода) у них обычно служат карбонильные группы промежуточных продуктов окисления субстрата. Так, НАДН (восстановл. форма нико-тинамидадениндинуклеотида) восстанавливает продукт де-карбоксилирования пирувата (ацетальдегид) до этанола (при брожении), а пируват-до лактата (при гликолизе). Пример окислит. фосфорилирования — синтез АТФ в аэробных условиях, а также у сульфатных бактерий в анаэробных условиях. Во всех этих случаях образование АТФ сопряжено с переносом электронов (атомов водорода) по цепи окислительно-восстановит. коферментов, включающей никотинамидные и флавиновые коферменты (см. рибофлавин), убихиноны (у животных), пластохиноны (у растений), негеминовое железо и медь. В митохондриях первонач. донором электронов (атомов водорода) служат орг. соед., а конечным акцептором — атмосферный O2, в хлоропластах донором и акцептором электронов (атомов водорода) служат продукты фотореакции. У сульфатных бактерий донором являются орг. соед., а акцептором-сульфат, восстанавливаемый до сульфида.
Особенность биол. окисления в аэробных условиях состоит в том, что орг. субстрат обычно полностью окисляется до CO2 и воды в циклич. последовательностях реакций. Пример такого окисления — превращения в цикле трикарбоновых кислот ацетата, образующегося в виде АцКоА при окислит. расщеплении жирных кислот, углеводов и некоторых аминокислот. Др. пример — полное окисление глюкозы в пентозофосфатном цикле. Циклич. пути благодаря полному окислению субстратов позволяют извлекать из орг. соед. максимум заключенной в них своб. энергии.
Регуляция обмена веществ
На О.в. постоянно оказывают воздействие разл. факторы внеш. и внутр. среды. Большая часть из них эффективно используется организмами для своего роста и развития. Это происходит благодаря функционированию механизмов регуляции О.в. Наиб. простым из них, способствующим сохранению внутр. среды организма (поддерживанию гомеостаза), является механизм восстановления в хим. системе равновесия в соответствии с законом действующих масс. Благодаря этому значения pH в буферных жидкостях организма устойчивы к случайным воздействиям. Предотвращение накопления в организме невыводимых продуктов О.в. также осуществляется благодаря восстановлению равновесия в замыкающих участках циклич. путей О.в.
Более сложные механизмы регуляции О.в. обусловлены прямыми и обратными управляющими связями. Суть их состоит в воздействии метаболитов на интенсивность био-хим. процессов, в которых они сами образуются или испытывают превращения. В О.в. регуляция активности ферментов часто осуществляется посредством аллостерич. взаимод. ферментов с субстратами или промежут. продуктами (см. ферменты). Классич. пример подобной регуляции с отрицат. обратной связью-подавление изолейцином собств. биосинтеза в результате его аллостерич. взаимод. с ферментом треониндегидратаза, катализирующим начальную реакцию пути биосинтеза изолейцина. Пример положит. прямой связи — стимуляция синтеза фосфоенолпирувата в гликолизе предшествующими метаболитами: фруктозо-1,6-дифосфатом, глюкозо-6-фосфатом и глицеральдегид-3-фосфатом. Управляющие связи такого рода позволяют стабилизировать концентрации метаболитов в неравновесной системе.
Сходным образом осуществляется регуляция О.в. на уровне биосинтеза ферментов. При этом субстрат или продукт реакции регулирует активность белкового репрессора, подавляющего транскрипцию (синтез матричной РНК на ДНК-матрице) соответствующего оперона (участок ДНК, кодирующий одну молекулу матричной РНК под контролем белка-рспрессора). Примером регуляции при помощи положит. прямой связи может служить в данном случае управление расщеплением лактозы. Появление в среде лактозы инактивирует у бактерии Escherichia coli соответствующий репрессор и тем самым разрешает транскрипцию оперона, кодирующего ферменты, катализирующие расщепление лактозы. Пример регуляции при помощи отрицат. обратной связи — управление биосинтезом гистидина. Избыток гисти-дина активирует репрессор, ингибирующий транскрипцию оперона, кодирующего ферменты биосинтеза гистидина. Если репрессор и белки, синтез которых он подавляет, кодируются одним опероном, то отрицат. обратная связь осуществляется без участия внеш. модуляторов активности репрессора. Аналогичным образом осуществляется регуляция биосинтеза белка на уровне трансляции (синтез белка на РНК-матрице). Такой механизм регуляции позволяет синтезировать белок в строгом соответствии с потребностью в нем на данном этапе существования организма.
Многоклеточные организмы наряду с рассмотренными внутриклеточными механизмами имеют надклеточные-гормональные механизмы регуляции О.в. Гормональная регуляция координирует О.в. в разл. тканях и органах и интегрирует его в рамках организма в целостную систему. Гормональная регуляция О.в. у растений осуществляется группой фитогормонов, напр. ауксинами и гиббереллинами. Гормональную регуляцию О.в. у животных осуществляет эндокринная система, источниками гормонов в которой являются центр. и переферич. железы внутр. секреции. Характер управляющих связей в этой системе иллюстрирует механизм поддержания концентрации глюкозы в крови на постоянном уровне. Так, повышение концентрации глюкозы в крови увеличивает продукцию инсулина, который стимулирует клетки на усиленное потребление глюкозы. Возникающий при этом дефицит глюкозы приводит к увеличению продукции др. пептидного гормона-глюкагона, который стимулирует восстановление концентрации глюкозы благодаря расщеплению гликогена в клетках.
Как правило, механизмы гормональной регуляции многоступенчаты. Воздействие гормонов на О.в. осуществляется через клеточную мембрану, во мн. случаях посредством активирования аденилатциклазной системы (см. аденилатциклаза). Обратные связи в эндокринной системе часто замыкаются через нервную систему. При этом нервная система, получая сигналы из внеш. среды или от внутр. органов, управляет железами внутр. секреции. Например, гипоталамус по сигналам от центр. нервной системы, передаваемым гормонами-медиаторами (напр., норадренали-ном, ацетилхолином), секретирует пептидные нейрогормо-ны (релизинг-факторы), разрешающие секрецию гормонов гипофиза. Последние стимулируют секрецию гормонов периферич. эндокринными железами. Эти гормоны влияют на О.в. в соответствующих органах и тканях т. обр., чтобы компенсировать изменения во внутр. среде или подготовиться к возможным ее изменениям, прогнозируемым центр. нервной системой (напр., при стрессовых ситуациях). Гипо-таламо-гипофизарная система, в частности, играет центр. роль в регуляции водно-солевого обмена животных (см. вазопрессин, окситоцин).
Регуляция при помощи управляющих связей допускает возникновение в О.в. состояний с автоколебат. режимами (см. колебательные реакции), обусловливающими периодич. изменение концентраций некоторых метаболитов. Такие автоколебат. режимы лежат в основе разл. периодич. процессов у живых организмов, напр. сердечных сокращений, суточных ритмов активности и др.
Нарушения обмена веществ
Различают нарушения О.в., вызываемые прямым влиянием на него неблагоприятных факторов (недостаток или несбалансированность орг. и минер. субстратов О.в., избыточности или недостатка внеш. физ. воздействий-температуры, света, звука и др.), и нарушения, вызываемые изменениями в наследств. аппарате организма. В соответствии с этим заболевания О.в. у людей подразделяют на болезни недостаточности и врожденные болезни. Например, к болезням недостаточности относятся алиментарная дистрофия при голодании или недостатке в пище незаменимых аминокислот, авитаминозы (цинга — при недостатке аскорбиновой кислоты, рахит — при недостатке витамина D). К болезням недостаточности более чувствительны организмы в стадии роста и развития. Примеры врожденных болсзней-алкаптонурия, связанная с недостаточной активностью ферментов, расщепляющих гомогентезиновую кислоту, и серповидноклеточная анемия (см. гемоглобин).
Нарушения О.в. у микроорганизмов, вызванные изменениями в составе субстратов или полученные в результате мутагенеза, широко используют в практич. целях. Так, добавляя в питат. среду дрожжей сульфит натрия, удается переключить алкогольное брожение на глицериновое и создать на этой основе биотехнологию получения глицерина. В микробиол. промышленности широко используют полученные селекцией штаммы микроорганизмов-суперпродуценты отдельных аминокислот, антибиотиков и др. Методы генной инженерии позволяют избирательно изменять наследственный аппарат клеток и благодаря этому целенаправленно воздействовать на структуру и динамику О.в. у организмов.
Лит.: Дэгли С., Никольсон Д., Метаболические пути, пер. с англ., М., 1973; Ньюсхолм Э., Старт К., Регуляция метаболизма, М., 1977; Лукнер М., Вторичный метаболизм у микроорганизмов, растений и животных, пер. с англ., М., 1979; Мак-Мюррей У., Обмен веществ у человека, пер. с англ., М., 1980; Малыгин А. Г., Симметрия сети реакций метаболизма, М., 1984.
А. Г. Малыгин
Значения в других словарях
- Обмен веществ — Или метаболизм, — лежащий в основе жизни закономерный порядок превращения веществ и энергии в живых системах, направленный на их сохранение и самовоспроизведение; совокупность всех химических реакций, протекающих в организме. Большая советская энциклопедия
- обмен веществ — См. метаболизм. Микробиология. Словарь терминов
- обмен веществ — ОБМЕН ВЕЩЕСТВ, метаболизм, совокупность хим. н связанных с ними энергетич. процессов превращения поступающих извне и возникающих в клетках в-в; лежит в основе жизнедеятельности живых организмов и является одним из осн. признаков жизни. О. Сельскохозяйственный словарь
- обмен веществ — ОБМЕН ВЕЩЕСТВ — см. метаболизм. Ботаника. Словарь терминов
- обмен веществ — Метаболизм, совокупность протекающих в живых организмах химич. превращений, обеспечивающих их рост, жизнедеятельность, воспроизведение, постоянный контакт и обмен с окружающей средой. Благодаря О. Биологический энциклопедический словарь
- обмен веществ — (метаболизм), совокупность процессов химических и физических превращений, происходящих в живых организмах и обеспечивающих их жизнедеятельность при взаимодействии с внешней средой. Биология. Современная энциклопедия
- ОБМЕН ВЕЩЕСТВ — ОБМЕН ВЕЩЕСТВ (метаболизм) — совокупность всех химических изменений и всех видов превращений веществ и энергии в организмах, обеспечивающих развитие, жизнедеятельность и самовоспроизведение организмов... Большой энциклопедический словарь
