трикарбоновых кислот цикл
ТРИКАРБОНОВЫХ КИСЛОТ ЦИКЛ (цикл Кребса)
цик-лич. последовательность ферментативных реакций (схема 1; назв. неионизир. форм кислот см. в ст. обмен веществ), в которых осуществляются превращения ди- и трикарбоновых кислот, образующихся как промежут. продукты в организме животных, в растениях и микробах.
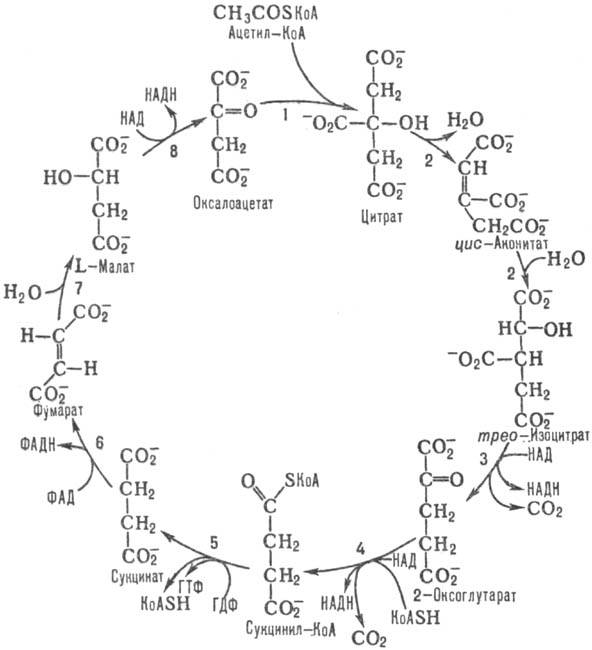
Схема 1. Цикл трикарбоновых кислот.
Одновременно Т. к. ц. — метаболии, путь окисления до CO2 и H2O аминокислот, жирных кислот и углеводов, которые вступают в этот цикл на разл. его стадиях (схема 2). Кроме того, образующиеся ди- и трикарбоновые кислоты м. б. исходными субстратами в биосинтезе мн. соед. (схема 3). Так, оксало-ацетат-субстрат в глюконеогепезе; сукцинил-КоА — промежут. продукт в синтезе порфиринов, ацетил-КоА — в синтезе жирных кислот, стероидов, ацетилхолина. Образующийся в цикле CO2 используется в реакциях карбоксилирования в синтезе жирных кислот, орнитиновом цикле и др. Участие Т. к. ц. в биосинтезе и катаболизме мн. веществ обусловливает его важное место в обмене веществ.
Т. к. ц. широко распространен у всех аэробных организмов, у эукариот (все организмы, за исключением бактерий и синезеленых водорослей) он осуществляется в митохондриях.
Суммарная реакция Т. к. ц. у животных имеет вид:
CH3C(O)SKoA + 3НАД + ФАД + ГДФ + Ф + H2O → 2CO2 + 3НАДН + ФАДН + ГТФ + 2Н + KoASH
НАДН и НАД, ФАДН и ФАД — соотв. восстановленные и окисленные формы кофермента никотинамидадениндинук-леотида (см. ниацин) и кофермента флавинадениндинуклео-тида (см. рибофлавин); ГДФ и ГТФ — соотв. гуанозинди- и гуанозинтрифосфат, Ф-неорг. фосфат, KoASH-кофер-мент А.
НАДН и ФАДН, образующиеся в цикле, окисляются в цепи переноса электронов (см. дыхание, окислительное фосфорилирование) с образованием АТФ, который играет важную роль в энергетич. обмене.
В реакции 1 цикла, катализируемой цитрат — оксалоацетат-лиазой, CH3C(O)SKoA стереоспецифично конденсируется с карбонильной группой оксалоацетата с образованием цитрата и свободного KoASH. Реакция сопровождается значит. изменением своб. энергии (ΔG0 −32,24 кДж/моль) и является практически необратимой. Активность митохонд-риального фермента у дрожжей ингибируется АТФ.
Реакция 2 цикла, катализируемая аконитат-гидратазой,-изомеризация цитрата в изоцитрат путем последоват. дегидратации — регидратации через промежут. образование цис-аконитата. Реакция обратима, равновесие сдвинуто в сторону синтеза цитрата, однако в условиях непрерывного функционирования цикла конечным продуктом реакции является изоцитрат.
В реакции 3, катализируемой НАД- или НАДФ-зависимой изоцитратдегидрогеназой, происходит дегидрирование изо-цитрата при атоме С-2 с одновременным декарбоксили-рованием и образованием 2-оксоглутарата и CO2. Бактерии содержат НАДФ-зависимую изоцитратдегидрогеназу, активность которой регулируется хим. модификацией — фосфо-рилированием (инактивация) и дефосфорилированием (активация) при участии бифункцион. фермента изоцитратдегидрогеназа-киназа (фосфатаза), играющего существ. роль в переключении обмена с Т. к. ц. на анаплеротич. ("возмещающий" образование промежут. продуктов Т. к. ц.) глиокси-латный цикл. Эукариоты содержат обе формы изоцитрат-дегидрогеназы. Активность НАДФ-зависимого фермента, локализованного в митохондриальном матриксе и цитозоле, контролируется продуктами реакции. Активность НАД-зави-симой изоцитратдегидрогеназы, локализованной исключительно в митохондриальном матриксе, активируется у грибов аденозинмонофосфатом (АМФ) и цитратом, у животных — аденозиндифосфатом (АДФ), цитратом и ионами Ca2+.
Реакция 4 катализируется мультиферментным 2-оксоглута-ратдегидрогеназным комплексом, состоящим из трех осн. ферментов: 2-оксоглутаратдегидрогеназы, дигидролипоил-сукцинилтрансферазы и дигидролипоилдегидрогеназы.
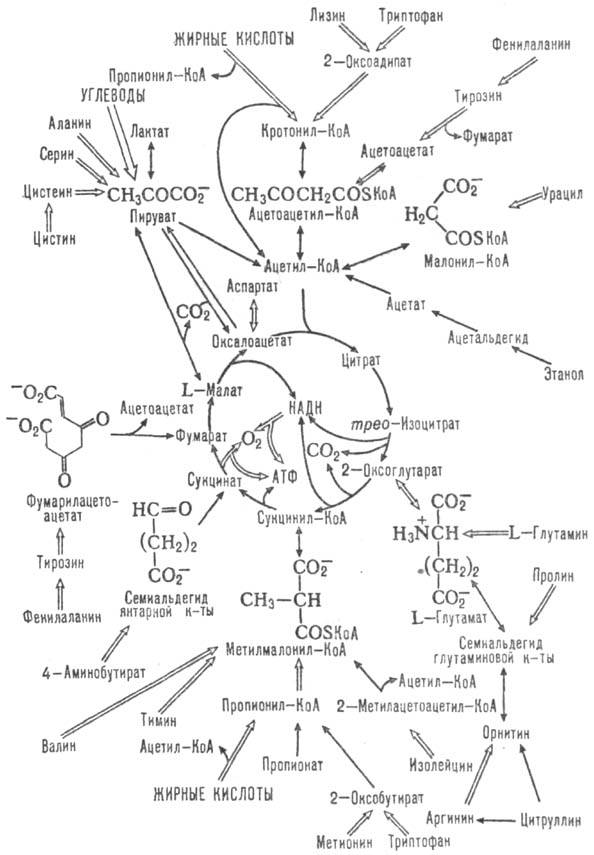
Схема 2. Цикл трикарбоновых кислот и катаболич. реакции. Двойными стрелками отмечены многостадийные реакции; семиальдегиды кислот w-оксокислоты.
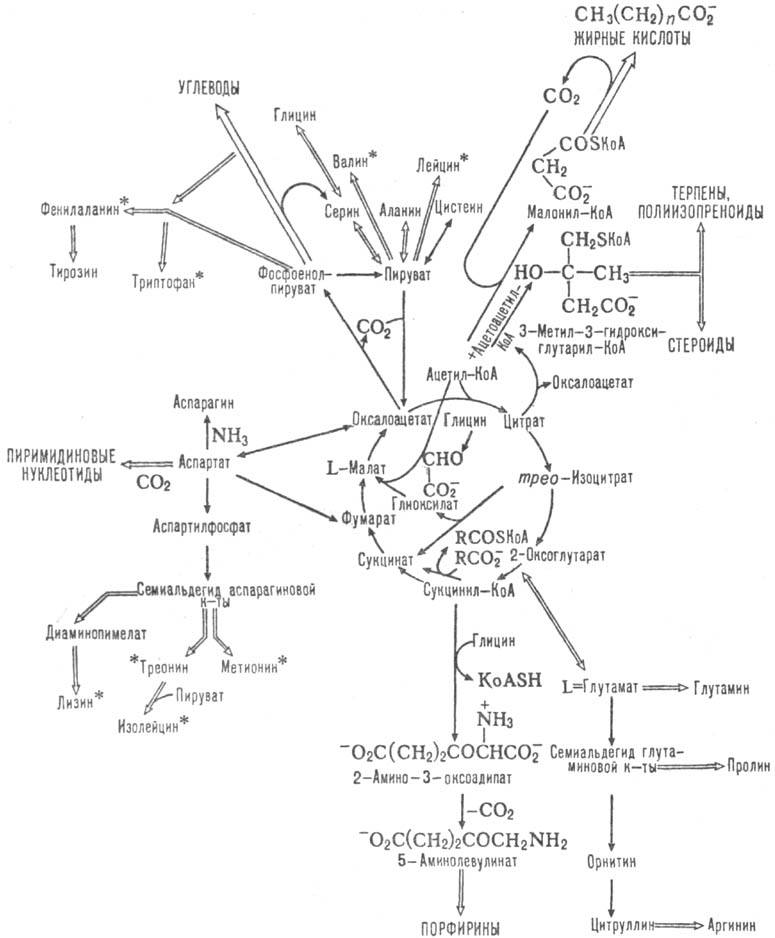
Схема 3. Биосинтетич. и др. реакции, сопутствующие циклу трикарбоновых кислот; аминокислоты, отмеченные звездочкой, в организме высших животных несинтезируются.
Сукцинил-КоА в реакции 5, катализируемой сукцинил-КоА — синтетазой, подвергается распаду, в результате которого энергия тиоэфирной связи сукцинил-КоА запасается в виде синтезир. нуклеозидтрифосфата (у бактерий, грибов, растений-АТФ, у животных — ГТФ).
В реакции 6, катализируемой сукцинатдегидрогеназой, происходит превращение сукцината в фумарат. Фермент входит в состав более сложного сукцинатдегидрогеназного комплекса (комплекса II) дыхат. цепи, поставляя восстановит. эквиваленты, образующиеся в реакции, в дыхат. цепь.
Фумарат-гидратаза, катализирующая реакцию 7, осуществляет гидратирование фумарата с образованием L-малата. Активность фермента ингибируется АТФ.
Последняя реакция цикла, 8, катализируется L-малатдегидрогеназой; L-малат при этом превращ. в оксалоацетат, который может взаимод. с новой молекулой ацетил-КоА. Реакция обратима, равновесие сдвинуто в сторону образования L-малата (ΔG0 +29,73 кДж/моль), но в условиях функционирования цикла конечным продуктом реакции является оксалоацетат.
Предполагают, что катализируемые индивидуальными ферментами реакции осуществляются благодаря действию надмолекулярного "сверхкомплекса", т. наз. метаболона. Преимущества такой организации ферментов очевидны — при этом не происходит диффузии кофакторов и субстратов, что способствует более эффективной работе цикла.
Наличие в Т. к. ц. 4 восстановит. реакций (3, 4, 6 и 8), в результате которых на 1 молекулу CH3C(O)SKoA синтезируются 3 молекулы НАДН и 1 молекула ФАДН, определяет необходимые условия для его функционирования. Непрерывная работа цикла требует реокисления НАДН и ФАДН, которое в аэробных условиях, как правило, осуществляется через совокупность переносчиков электронов, составляющих дыхат. цепь, и сопровождается запасанием значит. количества энергии. У животных это 11 молекул АТФ на 1 молекулу окисленного ацетил-КоА. У грибов, растений и особенно бактерий число молекул АТФ, образующихся при окислении НАДН и ФАДН, м. б. меньше вследствие разветвления дыхат. цепи.
В анаэробных условиях вместо Т.к.ц. функционируют его окислит. ветвь до 2-оксоглутарата (реакции 1 : 2 : 3) и восстановительная — от оксалоацетата до сукцината (реакции 8 : 7 : 6). При этом не происходит запасания большого количества энергии и функция цикла целиком определяется доставкой веществ для синтеза клеточного материала.
При переходе организма от покоя к активному состоянию возникает потребность в ускоренной мобилизации энергии (обменных процессов). У животных это достигается, в частности, шунтированием наиб. медленных реакций Т. к. ц. (реакции 1–3) и преимуществ. окислением сукцината. При этом исходный субстрат укороченного Т. к. ц. (2-оксоглутарат) образуется в результате быстрой реакции переаминирования:
Глутамат + Оксалоацетат ⇄ 2-Оксоглутарат + Аспартат
Связь Т. к. ц. с глиоксилатным циклом осуществляется благодаря синтезу в последнем сукцината, который в Т. к. ц. окисляется до оксалоацетата и служит, т. обр., поставщиком молекул с 4 атомами С в оба цикла на начальных стадиях их функционирования. Благодаря этому возможно функционирование этих циклов, когда в организме избыток соед. с 2 атомами С, напр. при выращивании бактерий на средах с CH3COOH и C2H5OH, а также при прорастании семян масличных растений, во время которого усиленно образуется ацетил-КоА.
Др. модификация Т. к. ц. (т. наз. 4-аминобутиратный шунт) — превращение 2-оксоглутарата в сукцинат, через глу-таминовую кислоту, 4-аминобутират и янтарный семиальдегид (3-формилпропионовая кислота). Эта модификация имеет большое значение для ткани мозга, в которой ок. 10% глюкозы распадается по этому пути.
Тесное сопряжение реакций Т. к. ц. с дыхат. цепью, особенно в митохондриях животных, а также особенности регуляции активности индивидуальных ферментов цикла (для большинства из них АТФ является ингибитором) предопределяют снижение активности цикла в условиях генерирования высокого фосфорильного потенциала (отношения АТФ/АДФ) в клетке, и наоборот — активацию цикла при пониж. фосфорильном потенциале. У большинства растений, бактерий и мн. видов грибов тесное сопряжение цикла с дыхат. цепью преодолевается развитием альтернативных несопряженных путей окисления, позволяющих поддерживать дыхат. активность и активность Т. к. ц. на высоком уровне даже в условиях высокого фосфорильного потенциала. Т. к. ц. открыт в 1937 Х. Кребсом и У. Джонсоном.
Лит.: Страйер Л., Биохимия, пер. с англ., т. 2, М., 1985, с. 49–68; Ленинджер А., Основы биохимии, пер. с англ., т. 2, М., 1985, с. 477–507; Кондрашова М.Н., "Биохимия", 1991, т. 56, в. 3, с. 388–404; Krebs H. А., Kornberg H. L., Energy transformations in living matter, В., 1957; Krebs H. А., "Persp. Biol. Med.", 1970, v. 14, p. 154–70; Srere P. A., "Ann. Rev. Biochem.", 1987, v. 56, p. 89–124.
Р. А. Звягильская
Значения в других словарях
- Трикарбоновых кислот цикл — Цикл лимонной кислоты, цикл Кребса, широко представленный в организмах животных, растений и микробов путь окислительных превращений ди- и трикарбоновых кислот, образующихся в качестве промежуточных продуктов при распаде белков, жиров и углеводов. Большая советская энциклопедия
- трикарбоновых кислот цикл — Цикл лимонной кислоты, цикл Кребса, циклич. последовательность ферментативных окислит, превращений три- и дикарбоновых к-т; общий заключит, этап окислит, распада продуктов обмена углеводов, жиров и белков (или аминокислот) до CO2 и Н20. Открыт X. Биологический энциклопедический словарь
- Трикарбоновых кислот цикл — Совокупность из 8 ферментативных реакций, приводящих к окислению активированной уксусной кислоты до воды и двуокиси углерода; завершает распад углеводов, белков и жиров в живом организме, сопровождается синтезом макроэргических соединений и накоплением в них энергии — см. Обмен веществ и энергии. Медицинская энциклопедия
- ТРИКАРБОНОВЫХ КИСЛОТ ЦИКЛ — ТРИКАРБОНОВЫХ КИСЛОТ ЦИКЛ (Кребса цикл — лимонной кислоты цикл) — циклический ферментативный процесс полного окисления в живых организмах активированной уксусной кислоты до СО2 и Н2О; общий конечный путь, которым завершается распад углеводов... Большой энциклопедический словарь
