бария нитрат
БАРИЯ НИТРАТ (бариевая селитра) Ba(NO3)2
бесцветные кристаллы с кубич. решеткой (а = 0,813нм; пространственная группа P21/3); т. пл. 595 °C (с разл.); плотн. 3,24 г/см3; C0p 151,6 Дж/(моль∙К)); 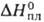 53,1 кДж/моль.
53,1 кДж/моль.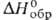 −978,6 кДж/моль,
−978,6 кДж/моль, 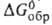 −783,2 кДж/моль; S0298 213,8 Дж/(моль∙К)). Диамагнитен (
−783,2 кДж/моль; S0298 213,8 Дж/(моль∙К)). Диамагнитен (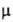 — 0,254∙103). Растворимость в воде (г на 100 г): 5,0 (0 °C), 9,2 (20 °C), 34,2 (100 °C); в присутствии Ca(NO3)2 и CaCl2 растворимость сильно снижается. В спирте и конц. HNO3 практически не растворяется. С нитратами Cs, Li, NH4+, Na, Rb, T1(I), BaBr2, Ba(NO2)2 образует эвтектич. смеси, с нитратами Со и Sr-непрерывный ряд твердых растворов. С KNO3 дает Ba(NO3)2*2KNO3. Выше 595 °C пре-вращ. в Ba(NO2)2, который ок. 670 °C разлагается до BaO.
— 0,254∙103). Растворимость в воде (г на 100 г): 5,0 (0 °C), 9,2 (20 °C), 34,2 (100 °C); в присутствии Ca(NO3)2 и CaCl2 растворимость сильно снижается. В спирте и конц. HNO3 практически не растворяется. С нитратами Cs, Li, NH4+, Na, Rb, T1(I), BaBr2, Ba(NO2)2 образует эвтектич. смеси, с нитратами Со и Sr-непрерывный ряд твердых растворов. С KNO3 дает Ba(NO3)2*2KNO3. Выше 595 °C пре-вращ. в Ba(NO2)2, который ок. 670 °C разлагается до BaO.
Б. н. встречается в природе в виде минерала нитробарита. Получают Б. н. взаимод. BaS или BaCO3 с HNO3, обменными реакциями BaCl2, Ba(OH)2 или BaS с нитратами Ca, аммония, К или Na. Применяют Б. н. для получения BaO и Ва2O2, как компонент эмалей и глазурей, для изготовления пиротехн. составов (пламя зеленого цвета). Б.н. токсичен; ПДК 0,5 мг/м3.
Лит. см. при статьях барий, бария гидроксид.
Т. Г. Ахметов
