целлюлозы нитраты
ЦЕЛЛЮЛОЗЫ НИТРАТЫ (нитроцеллюлоза)
сложные целлюлозы эфиры общей формулы [C6H7O2(OH)3-x(ONO2)x]n. Твердые волокнистые вещества белого цвета. Степень этерификации х, или степень замещения (СЗ), изменяется в диапазоне 0–3; ее рассчитывают, исходя из содержания азота [N] (% по массе) по формуле: СЗ = 3,6[N]/(31,1 — [N]). В зависимости от СЗ различают след. осн. виды технических Ц. н.: коллоксилин (10,7–12,2% N), пироксилин №2 (12,2–12,5% N), пироксилин № 1 (13,0–13,5% N). Степень полимеризации n Ц. н. колеблется в широких пределах: от 150 до 3500 (мол. м. 38,5–500 тыс.). Ц. н. — бризантные взрывчатые вещества; осн. свойства: теплота взрыва ок. 3600 кДж/кг; скорость детонации 7,3 км/с (при плотн. 1,2 г/см3); чувствительность к удару 5–10% (груз 2 кг, высота падения 25 см).
Плотность Ц. н. незначительно зависит от содержания N; напр., для коллоксилина, содержащего 11,8–12,2% N, плотн. 1,58–1,65 г/см3. Температуры плавления Ц. н. лежат выше температур разложения; водопоглощение и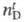 для Ц. н., содержащих, напр., 11,8–12,2% N, составляют соотв. 2–3% и 1,51.
для Ц. н., содержащих, напр., 11,8–12,2% N, составляют соотв. 2–3% и 1,51.
Растворимость Ц. н. в разл. растворителях зависит от СЗ. Низкозамещенные нитраты (0,5–2% N) раств. при комнатной температуре только в 6%-ном растворе NaOH, при содержании 9–11% N — в этаноле. Ц. н., содержащие 11,0–12,7% (СЗ 2,0–2,5), раств. в кетонах, сложных эфирах (напр., этилацетате), фурфуроле, диоксане, циклогексаноне, бутилцеллозольве и др.; универсальным растворителем Ц. н., содержащих 10,5–14,4% N (СЗ 1,8–3,0), служит ацетон. Ц. н. с любой СЗ не раств. в воде и неполярных растворителях (напр., в бензоле, CCl4). Ц. н. не устойчивы к действию кислот (разб. минер. кислоты вызывают медленную денитрацию) и щелочей (омыляют и разрушают, особенно спиртовые растворы).
Нестабилизированные Ц. н. обладают малой атмосферостойкостью и очень низкой термич. стабильностью; в обычных условиях безводные нитраты разлагаются менее чем через 3 мес. При нагревании Ц. н. подвергаются деструкции уже при 40–60 °C, причем скорость разложения быстро возрастает с повышением температуры и в присутствии кислот и щелочей. Термич. разложение Ц. н. — самоускоряющийся процесс, а при быстром нагревании возможны вспышка (для Ц. н., увлажненных спиртами, т. всп. 13 °C) и взрыв. Температура воспламенения зависит от скорости подвода теплоты: при медленном нагревании −190 °C, при быстром — от 160–170 до 141 °C. Энергия активации термич. распада и тепловой эффект термич. разложения на воздухе Ц. н. составляют соотв. 119–142 МДж/моль и 3,15 МДж/кг. Введение стабилизаторов (напр., дифениламина) повышает атмосфере- и термостойкость Ц. н.
Для получения Ц. н. применяют облагороженную хлопковую целлюлозу. После разрыхления и сушки ее нитруют в спец. аппаратах (нитраторах) или центрифугах при 30–45 °C смесью, которая при производстве коллоксилина (пироксилинов) включает 20–25 (20–30)% HNO3, 55–60 (60–70)% H2SO4 и 18–20 (5–10)% H2O; отношение массы нитрующей смеси к массе целлюлозы 40–50. Чем выше содержание в смеси воды, тем ниже степень полимеризации образующихся эфиров. Максимальная СЗ (2,8) достигается при содержании в смеси 3,5–5,0% H2O. После нитрования полученный продукт отфильтровывают от кислотной смеси, многократно промывают холодной водой, разб. раствором соды и снова водой, затем отжимают и хранят при содержании воды 20–35%. При необходимости Ц. н. обезвоживают спиртом. Наряду с описанным периодическим известны непрерывные способы про-из-ва Ц. н.
Области применения Ц. н. зависят от содержания в них азота. Коллоксилин используют в производствах нитроцеллюлозных пластмасс (этролов), целлулоида, нитролаков. нитроэмалей, бездымного пороха, динамита и др. ВВ, для жела янизации нитроглицерина; пироксилины — в производстве бездымного пороха. Осн. недостаток Ц. н. — высокая горючесть (т. воспл. и т. самовоспл. 141 °C), что ограничивает возможности их применения.
Лит.: Закощиков А. П., Нитроцеллюлоза, М., 1950; Роговин 3. А., Химия целлюлозы, М., 1972; Энциклопедия полимеров, т. 2, М., 1974, с. 377–80; Коваленко В.И., "Успехи химии", 1995, т. 64, № 8, с. 803–17.
В. Н. Кряжев
