теплоемкость
ТЕПЛОЕМКОСТЬ
количество теплоты, затрачиваемое для изменения температуры на 1 °C. Согласно более строгому определению, Т. — термодинамич. величина, определяемая выражением:
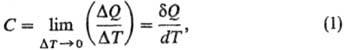
где ΔQ- количество теплоты, сообщенное системе и вызвавшее изменение ее температуры на ΔТ. Отношение конечных разностей ΔQ/ΔТ наз. средней Т., отношение бесконечно малых величин dQ/dT-истинной Т. Поскольку dQ не является полным дифференциалом функции состояния, то и Т. зависит от пути перехода между двумя состояниями системы. Различают Т. системы в целом (Дж/К), удельную Т. [Дж/(г∙К)], молярную Т. [Дж/(моль∙К)]. Во всех ниже приведенных формулах использованы молярные величины Т.
Из второго начала термодинамики следует, что Т. пропорциональна производной от энтропии системы S по температуре Т при постоянстве внеш. силы или термодинамич. координаты (обозначается индексом z):

Наиб. важными видами Т. являются Т. CV при постоянном объеме V и Т. Cр при постоянном давлении р:
CV = (9U/9T)V = T(9S/9T)V, Cр = (9Н/9Т)р = Т(9S/9Т)р,
где U — внутр. энергия, H-энтальпия системы. Значения Cр и CV связаны соотношением:
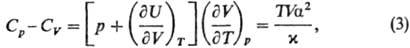
где α = V−1(9V/9Т)р-коэф. термич. расширения, x = = — V−1(9V/9р)T-коэф. изотермич. сжимаемости. Поскольку по условиям устойчивости фаз Cр, CV > 0 и (9V/9р)T < 0, то согласно (3) Cр > CV. Это естественно, т. к. при изобарич. нагревании часть тепла, помимо увеличения внутр. энергии системы, идет на работу расширения. Для идеальных газов (9U/9V)T = 0 и учет уравнения состояния pV= RT приводит к соотношению: Cp — CV = R (R-газовая постоянная). Из определений (1) и (2) следует, что для изотермич. процесса С = ,, для адиабатич. процесса С = 0.
Т. газов. Вычисление Т. сводится к вычислению средней энергии теплового движения отдельных молекул, которое складывается из поступат. и вращат. движений молекулы как целого и из колебаний атомов внутри молекулы. Молярная Т. одноатомного газа равна 3R/2 (по R/2 на каждую степень поступат. движения молекулы). Т. многоатомного газа в общем случае м. б. представлена суммой вкладов от отдельных видов движения-поступательного, вращательного, колебательного.
Поступательная Т. рассчитывается так же, как для одноатомного газа. Вращательная и в особенности колебательная Т. должны, как правило, вычисляться на основе квантовой статистики. Согласно классич. статистике, вклады в молярную Т. в расчете на одну степень свободы равны: для вращат. движения R/2, для колебат. движения R. Для большинства молекул при низких и средних температурах колебат. степени свободы вырождены и не дают вклада в Т. Например, Т. двухатомного газа при обычных температурах равна 5R/2. Лишь при достаточно высоких температурах возбуждаются колебания определенной частоты.
Т. твердых тел. При низких температурах Т. одноатомных кристаллов пропорциональна кубу абс. температуры (закон Дебая): CV ! Т3. При высоких температурах CV стремится к предельному значению 3R, определяемому классич. теорией и не зависящему от природы атомов (правило Дюлонга и Пти). Значение 3R может, однако, не достигаться, если ранее происходит плавление вещества или его разложение. Методами квантовой статистики доказывается равенство нулю Т. любого тела при абс. нуле температуры (CV : 0 при Т : 0). Если бы это было не так, энтропия системы, согласно (2), должна была бы обращаться в — , при T : 0, что противоречит третьему началу термодинамики (см. тепловая теорема). Предельное значение CV = 3R достигается уже при обычных температурах у металлов. Для некоторых простых соед. с числом атомов в молекуле n предельное значение CV = 3nR [NaCl, MnS (n = = 2), PbCl2(n = 3) и др.].
Для кристаллич. твердых тел существует характеристич. температура qD, названная температурой Дебая, разделяющая "классич. область" температур Т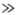 qD, в которой Т. описывается законом Дюлонга и Пти, и "квантовую область" T
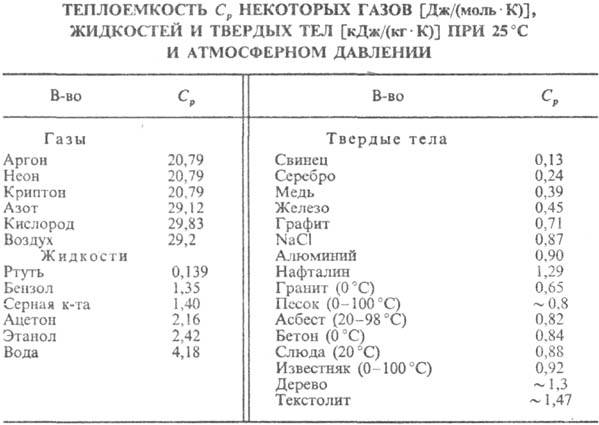
qD, в которой Т. описывается законом Дюлонга и Пти, и "квантовую область" T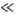 qD. Температура Дебая связана с предельной частотой колебаний атомов в кристаллич. решетке и зависит от упругих постоянных вещества (см. табл.).
qD. Температура Дебая связана с предельной частотой колебаний атомов в кристаллич. решетке и зависит от упругих постоянных вещества (см. табл.).
У металлов вклад в значение CV дают электроны проводимости (электронная Т.). Эта часть Т. может быть вычислена на основе квантовой статистики Ферми, которой подчиняются электроны. Электронная Т. пропорциональна температуре в первой степени, однако ее вклад пренебрежимо мал при температурах, когда велика "решеточная" Т. (пропорциональная T3). Антиферромагнетики и ферримагнетики, обладающие упорядоченным расположением спиновых магн. моментов атомов, имеют дополнит. магн. составляющую Т., которая испытывает резкий подъем при температуре фазового перехода вещества в парамагнитное состояние (см. Кюри точка).
Методы определения Т. индивидуальных веществ. Осн. эксперим. методом является калориметрия. Теоретич. расчет Т. веществ осуществляется методами статистической термодинамики, но он возможен только для сравнительно простых молекул в состоянии идеального газа и для кристаллов, причем в обоих случаях для расчета требуются эксперим. данные о строении вещества.
Эмпирич. методы определения Т. веществ в состоянии идеального газа основаны на представлении об аддитивности вкладов отдельных групп атомов или хим. связей. Опубликованы обширные таблицы групповых атомных вкладов в значение Cр. Для жидкостей, помимо аддитивно-групповых, применяют методы, основанные на соответственных состояний законе, а также на использовании термодинамич. циклов, позволяющих перейти к Т. жидкости от Т. идеального газа через температурную производную энтальпии испарения.
Для раствора вычисление Т. как аддитивной функции Т. компонентов в общем случае некорректно, т. к. избыточная Т. раствора, как правило, значительна. Для ее оценки требуется привлечение молекулярно-статистич. теории растворов (см. растворы неэлектролитов). Экспериментально избыточная Т. может быть определена по температурной зависимости энтальпии смешения, после чего возможен расчет Cр раствора.
Т. гетерог. систем представляет наиб. сложный случай для термодинамич. анализа. На диаграмме состояния перемещение вдоль кривой равновесия фаз сопровождается изменением и р, и Т. Если в процессе нагрева происходит смещение точки фазового равновесия, то это дает дополнит. вклад в Т., поэтому Т. гетерог. системы не равна сумме Т. составляющих ее фаз, но превосходит ее. На фазовой диаграмме при переходе от гомог. состояния к области существования гетерог. системы Т. испытывает скачок (см. фазовые переходы).
Практическое значение исследований Т. важно для расчетов энергетич. балансов процессов в хим. реакторах и др. аппаратах хим. производства, а также для выбора оптим. теплоносителей. Эксперим. измерение Т. для разных интервалов температур — от предельно низких до высоких-является осн. методом определения термодинамич. свойств веществ. Для расчета энтальпий и энтропии вещества (в интервалах от 0 до Г) используют интегралы от Т.:
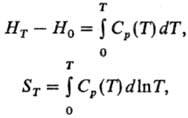
к которым добавляются соответствующие эффекты фазовых переходов. Знание Т. реагентов в некотором интервале температур позволяет осуществить расчет теплового эффекта реакции (см. Кирхгофа уравнение), а знание Т. растворов — рассчитать их термодинамич. свойства при любой температуре в пределах исследованного интервала.
Особо следует подчеркнуть роль Т. в структурных исследованиях индивидуальных веществ в конденсир. состоянии и растворов. Величины, являющиеся второй производной потенциалов Гиббса или Гельмгольца по параметрам состояния (а Т. относится к таковым), весьма чувствительны к структурным изменениям системы. В твердых телах и сплавах при фазовых переходах 2-го рода типа порядок — беспорядок наблюдаются λ-образные скачки Т. В жидкостях такие скачки имеют место вблизи критич. точек равновесия жидкость-газ и жидкость-жидкость (см. критические явления). В жидкости, напр., при нагр. часть энергии может идти не на возбуждение новых степеней свободы молекул, а на изменение потенц. энергии взаимодействующих молекул. Этот вклад наз. "конфигурационной" Т.; она связана с характером мол. упорядочения в жидкостях и растворах. В биохимии политермич. измерения Т. дают информацию о структурных переходах в белках.
Лит.: Рид Р., Праусниц Дж., Шервуд Т., Свойства газов и жидкостей, пер. с англ., 3 изд., Л., 1982; Шульц М. М., Филиппов В. К., "Ж. Весе. хим. общества им. Д.И. Менделеева", 1982, т. 27, с. 485–94; Панов М.Ю., Белоусов В. П., в сб.: Химия и термодинамика растворов, в. 5, Л., 1982, с. 56–87; Термодинамические свойства индивидуальных веществ, под ред. В. П. Глушко, 3 изд., т. 1–4, М., 1978–82; Experimental thermodynamics, ed. by J. P. McCullough, D. W. Scott, v. 1, N. Y. — L., 1968.
М. Ю. Панов
Значения в других словарях
- теплоемкость — Количество теплоты, переданное массе материала при повышении его температуры на один градус Цельсия. [82] Строительная терминология
- ТЕПЛОЕМКОСТЬ — ТЕПЛОЕМКОСТЬ (количество теплоты, обозначение С), в физике — способность объекта поглощать тепло. Произведение массы объекта на его УДЕЛЬНУЮ ТЕПЛОЕМКОСТЬ, или отношение количества теплоты, поглощаемой телом, к изменению его температуры... Научно-технический словарь
- теплоемкость — ТЕПЛОЁМКОСТЬ -и; ж. Физ. Количество теплоты, поглощаемой телом при нагревании на 1 градус (по Цельсию) или отдаваемой при остывании на 1 градус (по Цельсию). Т. металла, пластмассы. Удельная т. (количество теплоты, потребное для нагревания 1 грамма вещества на 1 градус по Цельсию). Толковый словарь Кузнецова
- Теплоемкость — См. Газы, Теплота, Физические свойства простых тел. Энциклопедический словарь Брокгауза и Ефрона
- ТЕПЛОЕМКОСТЬ — ТЕПЛОЕМКОСТЬ — количество теплоты, которое необходимо подвести к телу, чтобы повысить его температуру на 1 К, точнее — отношение количества теплоты, полученного телом (веществом) при бесконечно малом изменении его состояний в каком-либо процессе... Большой энциклопедический словарь
- теплоемкость — теплоёмкость ж. Количество тепла тепло I 1., теплоты теплота 1., необходимое для нагревания тела на 1 градус по Цельсию или отдаваемое телом при остывании на 1 градус по Цельсию (в физике). Толковый словарь Ефремовой
- теплоемкость — ТЕПЛОЁМКОСТЬ, теплоёмкости, мн. нет, ·жен. (физ.). Количество тепла, необходимое для того, чтобы нагреть данное тело на 1°. Удельная теплоёмкость (количество тепла, необходимое для того, чтоб нагреть 1 ·г на 1°). Толковый словарь Ушакова
