поверхностное натяжение
ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
стремление вещества (жидкости или твердой фазы) уменьшить избыток своей потенциальной энергии на границе раздела с др. фазой (поверхностную энергию). Определяется как работа, затрачиваемая на создание единицы площади поверхности раздела фаз (размерность Дж/м2). Согласно др. определению, П. н. — сила, отнесенная к единице длины контура, ограничивающего поверхность раздела фаз (размерность Н/м); эта сила действует тангенциально к поверхности и препятствует ее самопроизвольному увеличению.
П. н.-осн. термодинамич. характеристика поверхностного слоя жидкости на границе с газовой фазой или др. жидкостью. П. н. разл. жидкостей на границе с собств. паром изменяется в широких пределах: от единиц для сжиженных низкокипящих газов до неск. тыс. мН/м для расплавл. тугоплавких веществ. П. н. зависит от температуры. Для мн. однокомпо-нентных неассоциир. жидкостей (вода, расплавы солей, жидкие металлы) вдали от критич. температуры хорошо выполняется линейная зависимость:
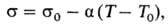
где σ и s0-П. н. при температурах T и T0 соотв., α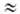 0,1 мН/(м∙К)-температурный коэффициент П.н. Осн. способ регулирования П. н. заключается в использовании поверхностно-активных веществ (ПАВ).
0,1 мН/(м∙К)-температурный коэффициент П.н. Осн. способ регулирования П. н. заключается в использовании поверхностно-активных веществ (ПАВ).
П.н. входит во мн. уравнения физики, физ. и коллоидной химии, электрохимии. Оно определяет след. величины: 1) капиллярное давление 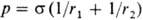 , где r1 и r2 — главные радиусы кривизны поверхности, и давление насыщ. пара рr над искривленной поверхностью жидкости:
, где r1 и r2 — главные радиусы кривизны поверхности, и давление насыщ. пара рr над искривленной поверхностью жидкости: 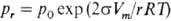 , где r — радиус кривизны поверхности, R — газовая постоянная, Vn-молярный объем жидкости, p0- давление над плоской поверхностью (законы Лапласа и Кельвина, см. капиллярные явления).
, где r — радиус кривизны поверхности, R — газовая постоянная, Vn-молярный объем жидкости, p0- давление над плоской поверхностью (законы Лапласа и Кельвина, см. капиллярные явления).
2) Краевой угол смачивания 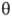 в контакте жидкости с поверхностью твердого тела: cos
в контакте жидкости с поверхностью твердого тела: cos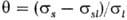 , где
, где 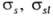 -уд. своб. поверхностные энергии твердого тела на границе с газом и жидкостью,
-уд. своб. поверхностные энергии твердого тела на границе с газом и жидкостью, 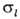 -П.н. жидкости (закон Юнга, см. смачивание).
-П.н. жидкости (закон Юнга, см. смачивание).
3) Адсорбцию ПАВ 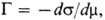 где m-хим. потенциал адсорбируемого вещества (уравнение Гиббса, см. адсорбция). Для разб. растворов
где m-хим. потенциал адсорбируемого вещества (уравнение Гиббса, см. адсорбция). Для разб. растворов 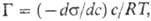 где с — молярная концентрация ПАВ.
где с — молярная концентрация ПАВ.
4) Состояние адсорбц. слоя ПАВ на поверхности жидкости: (πs + a/A2)∙(A — b)= kT, где πs = (σ0 — σ) — двухмерное давление, σ0 и <�т-соответственно П.н. чистой жидкости и той же жидкости при наличии адсорбц. слоя, а — постоянная (аналог постоянной Ван-дер-Ваальса), A-площадь поверхностного слоя, приходящаяся на одну адсорбир. молекулу, b — площадь, занимаемая 1 молекулой жидкости, k — постоянная Больцмана (уравнение Фрумкина — Фольмера, см. поверхностная активность).
5)Электрокапиллярный эффект: — dσ/dφ = rs, где rs-плотность поверхностного заряда, φ-потенциал электрода (уравнение Липмана, см. электрокапиллярные явления).
6) Работу образования критич. зародыша новой фазы Wc. Например, при гомог. конденсации пара при давлении 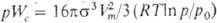 , где p0- давление пара над плоской поверхностью жидкости (уравнение Гиббса, см. зарождение новой фазы).
, где p0- давление пара над плоской поверхностью жидкости (уравнение Гиббса, см. зарождение новой фазы).
7) Длину λ капиллярных волн на поверхности жидкости: 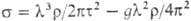 , где ρ-плотность жидкости, т-период колебаний, g-ускорение своб. падения.
, где ρ-плотность жидкости, т-период колебаний, g-ускорение своб. падения.
8) Упругость жидких пленок со слоем ПАВ: модуль упругости 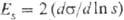 , где s — площадь пленки (уравнение Гиббса, см. тонкие пленки).
, где s — площадь пленки (уравнение Гиббса, см. тонкие пленки).
П.н. измерено для мн. чистых веществ и смесей (растворов, расплавов) в широком интервале температур и составов. Поскольку П. н. весьма чувствительно к наличию примесей, измерения разными методиками не всегда дают совпадающие значения. Осн. методы измерения следующие:
1) подъем смачивающих жидкостей в капиллярах. Высота подъема 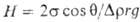 , где
, где 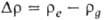 — разность плотностей жидкости и вытесняемого газа, r-радиус капилляра. Точность определения П.н. растет с уменьшением отношения r/а (а-капиллярная постоянная жидкости).
— разность плотностей жидкости и вытесняемого газа, r-радиус капилляра. Точность определения П.н. растет с уменьшением отношения r/а (а-капиллярная постоянная жидкости).
2) Измерение макс. давления в газовом пузырьке (метод Ребиндера); расчет основан на уравнении Лапласа. При выдавливании пузырька в жидкость через калиброванный капилляр радиусом г перед моментом отрыва давление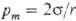
3) Метод взвешивания капель (сталагмометрия): 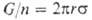 (уравнение Тейта), где G — общий вес n капель, оторвавшихся под действием силы тяжести от среза капиллярной трубки радиусом r. Для повышения точности правую часть умножают на поправочный коэф., зависящий от г и объема капли.
(уравнение Тейта), где G — общий вес n капель, оторвавшихся под действием силы тяжести от среза капиллярной трубки радиусом r. Для повышения точности правую часть умножают на поправочный коэф., зависящий от г и объема капли.
4) Метод уравновешивания пластины (метод Вильгельми). При погружении пластины с периметром сечения L в смачивающую жидкость вес пластины 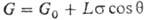 , где G0- вес сухой пластины.
, где G0- вес сухой пластины.
5) Метод отрыва кольца (метод Дю Нуи). Для отрыва проволочного кольца радиусом R от поверхности жидкости требуется сила 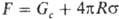
6) Метод сидящей капли. Профиль капли на несмачиваемой подложке определяется из условия постоянства суммы гидростатич. и капиллярного давлений. Дифференциальное уравнение профиля капли решается численным интегрированием (метод Башфорта — Адамса). По измерениям геом. параметров профиля капли с помощью соответствующих таблиц находят П.н.
8) Метод вращающейся капли. Капля жидкости плотностью r1 помещается в трубку с более тяжелой (плотность r2) жидкостью. При вращении трубки с угловой скоростью w капля вытягивается вдоль оси, принимая приближенно форму цилиндра радиуса r. Расчетное уравнение: 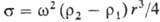 . Метод применяют для измерения малых П.н. на границе двух жидкостей.
. Метод применяют для измерения малых П.н. на границе двух жидкостей.
П. н. является определяющим фактором мн. технол. процессов: флотации, пропитки пористых материалов, нанесе-ния покрытий, моющего действия, порошковой металлургии, пайки и др. Велика роль П. н. в процессах, происходящих в невесомости.
Понятие П.н. впервые ввел Я. Сегнер (1752). В 1-й пол. 19 в. на основе представления о П.н. была развита мат. теория капиллярных явлений (П. Лаплас, С. Пуассон, К. Гаусс, А.Ю. Давидов). Во 2-й пол. 19 в. Дж. Гиббс развил термодинамич. теорию поверхностных явлений, в которой решающую роль играет П.н. В 20 в. разрабатываются методы регулирования П.н. с помощью ПАВ и электрокапиллярных эффектов (И. Ленгмюр, П. А. Ребиндер, A. H. Фрумкнн). Среди совр. актуальных проблем-развитие мол. теории П.н. разл. жидкостей (включая расплавл. металлы), влияние кривизны поверхности на П. н.
Лит.: Семенченко В. К., Поверхностные явления в металлах и сплавах, М., 1957; Оно С., Кон до С., Молекулярная теория поверхностного натяжения в жидкостях, пер. с англ., М., 1963; Русанов А. И., Фазовые равновесия и поверхностные явления, Л., 1967; Ребиндер П. А., Избранные труды. Поверхностные явления в дисперсных системах. Коллоидная химия, М., 1978; АдамсонА., Физическая химия поверхностей, пер. с англ., М., 1979; Гиббс Дж. В., Термодинамика. Статистическая механика, М., 1982; Щукин E. Д., ПерцовА. В., Амелина E. А., Коллоидная химия, М., 1982.
Б. Д. Сумм
Значения в других словарях
- ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ — Термодинамич. характеристика поверхности раздела 2 фаз (тел), определяемая работой обратимого изотермич. образования единицы площади этой поверхности. Измеряется в Дж/м2 или Н/м. В случае жидкой поверхности раздела П. Физический энциклопедический словарь
- Поверхностное натяжение — Важнейшая термодинамическая характеристика поверхности раздела фаз (тел), определяемая как работа обратимого изотермического образования единицы площади этой поверхности. В случае жидкой поверхности раздела П. Большая советская энциклопедия
- ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ — ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ, молекулярная сила, связанная с граничным слоем жидкости. Из-за поверхностного натяжения жидкость ведет себя так, будто на ее поверхности находится пленка. Научно-технический словарь
- Поверхностное натяжение — Сила взаимодействия молекул жидкости, действующая в плоскости, касательной к ее поверхности в сторону сокращения последней; измерение величины П. Медицинская энциклопедия
- ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ — ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ — стремление вещества (жидкости или твердой фазы) уменьшить избыток своей потенциальной энергии (поверхностную энергию) на границе раздела с газовой фазой (напр., с собственным паром) или др. жидкой или твердой фазой. Большой энциклопедический словарь
