кремниевые кислоты
КРЕМНИЕВЫЕ КИСЛОТЫ
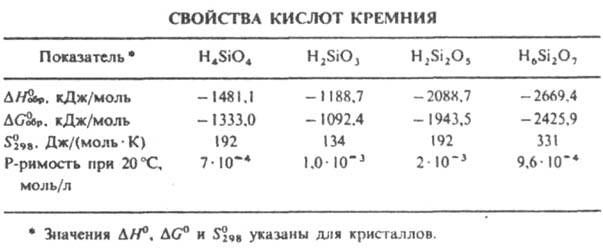
соед. общей формулы nSiO23mH2O. Известны: ортокремниевая кислота H4SiO4 (плотн. аморфной 2,1–2,3 г/см , о других свойствах см. табл.), мстакремниевая H2SiO3, пирокремниевая H6Si2O7, дикремниевые H2Si2O5 и H10Si2O9 (растворимость в воде при 20 °C 2,9∙10−4 моль/л) и поликремниевые кислоты.
К. к. — слабые кислоты; для H2SiO3 K1 =(2–3)∙10−10, K2=10−11–10−13; для H4SiO4 K1=2∙10−10, K2=K3=K4=2∙10−12. Растворы К.к. могут быть получены: растворением аморфного SiO2 в воде; из растворов силикатов щелочных металлов взаимод. с кислотами, ионным обменом или электродиализом; гидролизом соед. кремния (напр., хлорсиланов); поликонденсацией одних К. к. до других и т. д. В равновесном растворе аморфного SiO2 находятся мономерные формы К.к., в осн. H4SiO4. Ортокремниевая кислота стабильна при комнатной температуре, если концентрация SiO2 в растворе составляет менее ~0,01% по массе (т. е. не превышает растворимость твердой фазы аморфного кремнезема). Переход H4SiO4 в раствор можно представить схемой:
(SiO2)x+2H2ODH4SiO4+(SiO2)x-1
В процессе образования К. к. вначале получают неустойчивый истинный раствор H4SiO4; эта кислота в дальнейшем, благодаря наличию реакционноспособных силанольных групп SiOH, вступает в поликонденсацию, первая стадия которой 2H4SiO4:(HO)3SiOSi(OH)3+H2O. В результате поликонденсации могут образовываться разнообразные поликремниевые кислоты с линейной, разветвленной, смешанной структурой. К продуктам поликонденсации К. к. относятся гидрозоль (коллоидный кремнезем) и гидрогели кремнезема, силикагели (силикаксерогели) и др. Поликремниевые кислоты имеют изоэлектрич. точку в интервале pH 2,0–3,0. Скорость поликонденсации минимальна при pH ~ 2–3, причем в области pH<2 реакция ускоряется протонами, а при pH>2 — ионами OH−. Поликонденсация в кислой среде протекает по донорно-акцепторному механизму с образованием переходного комплекса, в котором атом Si временно приобретает координац. число 6 (вместо 4). Устойчивость золя К. к. зависит от концентрации К. к., температуры, pH и др. Со временем золь теряет устойчивость и переходит в гель (при pH>7,5 гидрозоль термодинамически устойчив к коагуляции). Скорость гелеобразования максимальна при pH 5,5–6,0. Подбирая соответствующие условия и применяя спец. добавки (стабилизаторы), удается получить устойчивые высококонцентрир. золи. Гидрозоли кремнезема-связующие материалы и наполнители в керамич. изделиях, покрытиях, в формах для литья; универсальные носители катализаторов и светочувствит. слоев в фотоматериалах; сырье для получения адсорбентов, кварцевого стекла; поглотители паров и газов в пром. аппаратах; фильтры для очистки воды и минер. масел.
Лит.: Получение и применение гидрозолей кремнезема, под ред. Ю. Г. Фролова, М., 1979 (Труды МХТИ им. Д. И. Менделеева, в. 107); Айлер Р., Химия кремнезема, ч. 1–2, пер. с англ., М., 1982.
В. Б. Соколов
Значения в других словарях
- Кремниевые кислоты — Производные кремниевого ангидрида SiO2; очень слабые кислоты, мало растворимые в воде. В чистом виде были получены метакремниевая кислота H2SiO3 (точнее её полимерная форма H8Si4O12) и H2Si2O5. Большая советская энциклопедия
- КРЕМНИЕВЫЕ КИСЛОТЫ — КРЕМНИЕВЫЕ КИСЛОТЫ — слабые кислоты состава nSiO2·mH2O. В воде растворимы плохо. Природные кремниевые кислоты — опал, трепел, диатомит, кремень. Применяют в бумажной и текстильной промышленности. Большой энциклопедический словарь
