галогенфосфаты
ГАЛОГЕНФОСФАТЫ
соед. общей формулы (КО)nР(О)На13_n, где и = 1,2; R-орг. радикал; Hal-F, C1, Br (соед. с Hal = I неустойчивы). Молекулы имеют тетра-эдрич. структуру с атомом Р в центре; углы связей у Р составляют ~ 100°. Большинство Г. — жидкости (см. табл.) с резким запахом; раств. в органических растворителях. Полосы поглощения в ИК-спектрах для связей Р=О (смещаются в ближнюю область с увеличением мол. массы галогена), Р—О, Р—F, Р—С1 и Р—Br составляют соотв. 1260–1350, 740–800, 850–950, 550–630 и 350–450 см−1.
СВОЙСТВА ГАЛОГЕНФОСФАТОВ
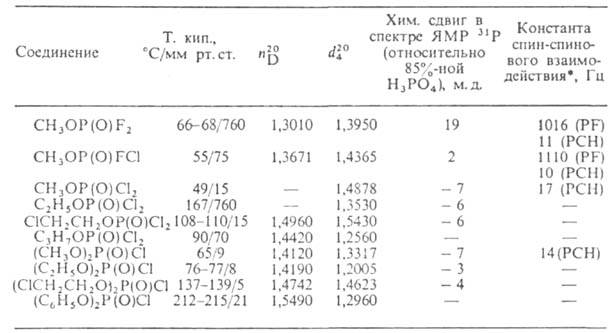
* В скобках приведены атомы, между которыми осуществляется взаимодействие.
Г. обычно активно взаимод. с нуклеофилами, напр.:
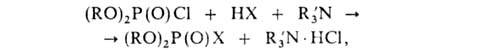
где X = OH, NR2'', R"O и др. С донорами протонов, кислотами Льюиса и солями некоторых металлов образуют комплексные соединения. При длит. нагревании разлагаются на кислоту и олефин; некоторые алкилдифторфосфаты (преим. с изоалкильными радикалами) неустойчивы даже при температуре ниже комнатной, напр.:
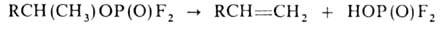
Диалкилгалогенфосфаты склонны к диспропорционированию и отщеплению AlkHal (последняя реакция характерна гл. обр. для метоксильных производных):
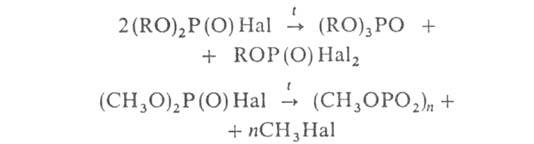
Г., содержащие метоксигруппы, с высокими скоростями алкилируют орг. основания:
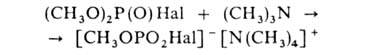
В промышленности Г. получают взаимод. оксигалогенидов Р со спиртами или фенолами (используют также их натриевые производные) либо гидрофосфитов с Cl2 (в лаб. практике вместо Cl2 обычно используют N-хлорсукцинимид). В препаративных целях применяют и др. методы, напр.:
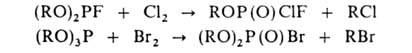
Г. — промежут. продукты в синтезе инсектицидов, пластификаторов, экстрагентов, огнестойких гидравлич. жидкостей и др. См. также Диизопропилфторфосфат, Метилдихлорфосфат.
Лит.: Пурдела Д., Вылчану Р., Химия органических соединений фосфора, пер. с рум., М., 1972, с. 486–512; Соrbridge D. E. С, в кн.: Topics in phosphorus chemistry, v. 6, N.Y.-[a.o.j, 1969,-p. 235–365.
Г. И. Дрозд
