галлия галогениды
ГАЛЛИЯ ГАЛОГЕНИДЫ
Физ. свойства некоторых Гг. приведены в таблице. Трихлорид GaCl3 — бесцветные кристаллы с триклинной решеткой [а — 0,694 нм, b = 0,684 нм, с = 0,682нм, α 119,5°, р 90,8°, 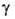 118,8°, z=l (Ga2Cl6), пространственная группа PI]. Молекулы димерны. Хорошо раств. в воде; из солянокислых растворов экстрагируется в виде HGaCl4 эфиром, бутилацетатом, трибутилфосфатом и др. орг. растворителями; образует моногидрат (т. пл. 44,4 °C); гигроскопичен. Является сильной кислотой Льюиса. Получают GaCl3 хлорированием Ga при 80–200 °C с послед. перегонкой, ректификацией, а также зонной плавкой. Применяют его для получения Ga высокой чистоты и синтеза др. соединений Ga, а также как катализатор полимеризации; наполнитель нейтринных ловушек.
118,8°, z=l (Ga2Cl6), пространственная группа PI]. Молекулы димерны. Хорошо раств. в воде; из солянокислых растворов экстрагируется в виде HGaCl4 эфиром, бутилацетатом, трибутилфосфатом и др. орг. растворителями; образует моногидрат (т. пл. 44,4 °C); гигроскопичен. Является сильной кислотой Льюиса. Получают GaCl3 хлорированием Ga при 80–200 °C с послед. перегонкой, ректификацией, а также зонной плавкой. Применяют его для получения Ga высокой чистоты и синтеза др. соединений Ga, а также как катализатор полимеризации; наполнитель нейтринных ловушек.
СВОЙСТВА ГАЛОГЕНИДОВ ГАЛЛИЯ
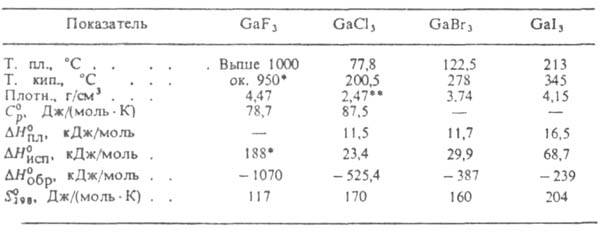
* Температура и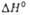 возгонки. ** Плотность жидкого 2,0536 г/см3.
возгонки. ** Плотность жидкого 2,0536 г/см3.
Трифторид GaP3 — бесцветные кристаллы; не раств. в воде; образует тригидрат (растворимость в H2O 4,1% по массе при 25 °C). Не взаимод. с разб. минеральными кислотами, разлагается растворами щелочей. На воздухе выше 200 °C образует GaOF, затем Ga2O3. Получают фторированием Ga, Ga2O3 или др. соединений Ga.
Трибромид GaBr3 — белые кристаллы, трииодид GaI3-желтые; по свойствам подобны GaCl3. Получают действием паров соответствующего галогена на нагретый Ga.
Моногалогениды GaHal образуются при взаимодействии паров GaHal3 с Ga; при конденсации GaF и GaCl диспропорционируют на Ga и соотв. GaF3 и GaCl3. Для GaBr т. пл. 158 °C (с разл.), для Gal 270 °C (с разл.)
Дигалогениды [тетрагалогеногаллаты(III) галлия(1)] Ga2Hal4, или GaI[GaIII Hal4], образуются при взаимодействии Ga с GaHal3 (Hal = Cl, Br, I). Дихлорид Ga2Cl4-белые кристаллы; т. пл. 175 °C, т. кип. 595 °C; плотн. 2,4173 г/см3; р 2,22Ом∙см (20 °C); диамагнитен. Для дибромида Ga2Br4 т. пл. 166 °C, т. кип. 462 °C. Для дииодида Ga2I4 т. пл. 211 °C, т. кип. 469 °C
Известны также Ga3Br7 (т. разл. 81 °C) и Ga3Cl7 (т. пл. 87 °C), имеющие строение GaI[Ga2IIIHaI7], и Ga4Hal6, или Ga2I[Ga2IIIHal6] (Hal = Cl, Br).
Лит. см. при ст. галлий.
П. И. Федоров
