аминокислоты
АМИНОКИСЛОТЫ
органические кислоты, содержащие одну или несколько аминогрупп. В зависимости от природы кислотной функции А. подразделяют на аминокарбоновые, например H2N(CH2)5COOH, аминосульфоновые, например H2N(CH2)2SO3H, аминофосфоновые, например H2NCH[Р(О)(OH)2]2, и аминоарсиновые, например H2NC6H4AsO3H2. Согласно правилам ИЮПАК, название
А. производят от названия соответствующей кислоты; взаимное расположение в углеродной цепи карбоксильной и аминной групп обозначают обычно цифрами, в некоторых случаях — греч. буквами. Однако, как правило, пользуются тривиальными названиями А.
Структура и физические свойства. По физ. и ряду хим. свойств А. резко отличаются от соответствующих кислот и оснований (см. табл. 1 и 2). Они лучше раств. в воде, чем в органических растворителях; хорошо кристаллизуются; имеют высокую плотность и исключительно высокие температуры плавления (часто разложения). Эти свойства указывают на взаимод. аминных и кислотных групп, вследствие чего А. в твердом состоянии и в растворе (в широком интервале pH) находятся в цвиттер-ионной форме. Например, для глицина кислотно-основное равновесие:
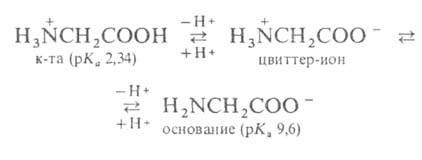
Взаимное влияние групп особенно ярко проявляется у α- аминокислот, где обе группы находятся в непосредств. близости, а также у о- и n-аминобензойных кислот, где их взаимод. передается через систему сопряженных связей. Благодаря электроноакцепторным свойствам группы —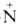 H3 резко усиливается кислотность карбоксильных групп, напр. pKа глицина 2,34, тогда как уксусной кислоты 4,75,
H3 резко усиливается кислотность карбоксильных групп, напр. pKа глицина 2,34, тогда как уксусной кислоты 4,75, 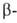 аланина 3,6. Аминогруппа подвергается взаимокомпенсируемому влиянию электроноакцепторной карбонильной группы и электронодонорного отрицательно заряженного атома кислорода, в результате чего, напр., основность аминогрупп аминоуксусной и n-аминобензойной кислот мало отличается от основности соотв. этиламина и анилина. Аминогруппа А. ионизирована в несколько меньшей степени, чем карбоксильная группа, и водный раствор А. имеет слабокислый характер. Значение pH, при котором концентрация катионов А. равна концентрации анионов, наз. изоэлектрич. точкой (рI). Все А. в изоэлектрич. точке имеют минимум растворимости (в растворах кислот и щелочей растворимость возрастает). Вблизи рI растворы А. обладают миним. буферным действием, а вблизи рК каждой функц. группы-максимальным.
аланина 3,6. Аминогруппа подвергается взаимокомпенсируемому влиянию электроноакцепторной карбонильной группы и электронодонорного отрицательно заряженного атома кислорода, в результате чего, напр., основность аминогрупп аминоуксусной и n-аминобензойной кислот мало отличается от основности соотв. этиламина и анилина. Аминогруппа А. ионизирована в несколько меньшей степени, чем карбоксильная группа, и водный раствор А. имеет слабокислый характер. Значение pH, при котором концентрация катионов А. равна концентрации анионов, наз. изоэлектрич. точкой (рI). Все А. в изоэлектрич. точке имеют минимум растворимости (в растворах кислот и щелочей растворимость возрастает). Вблизи рI растворы А. обладают миним. буферным действием, а вблизи рК каждой функц. группы-максимальным.
Табл. 1 — СВОЙСТВА L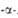 АМИНОКИСЛОТ
АМИНОКИСЛОТ
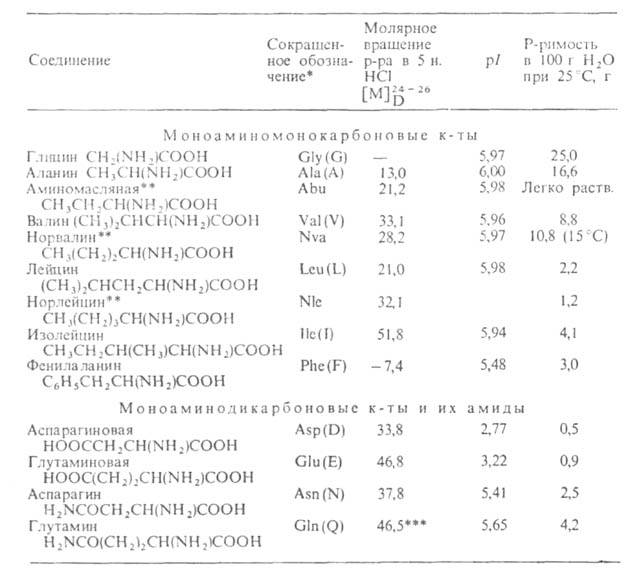
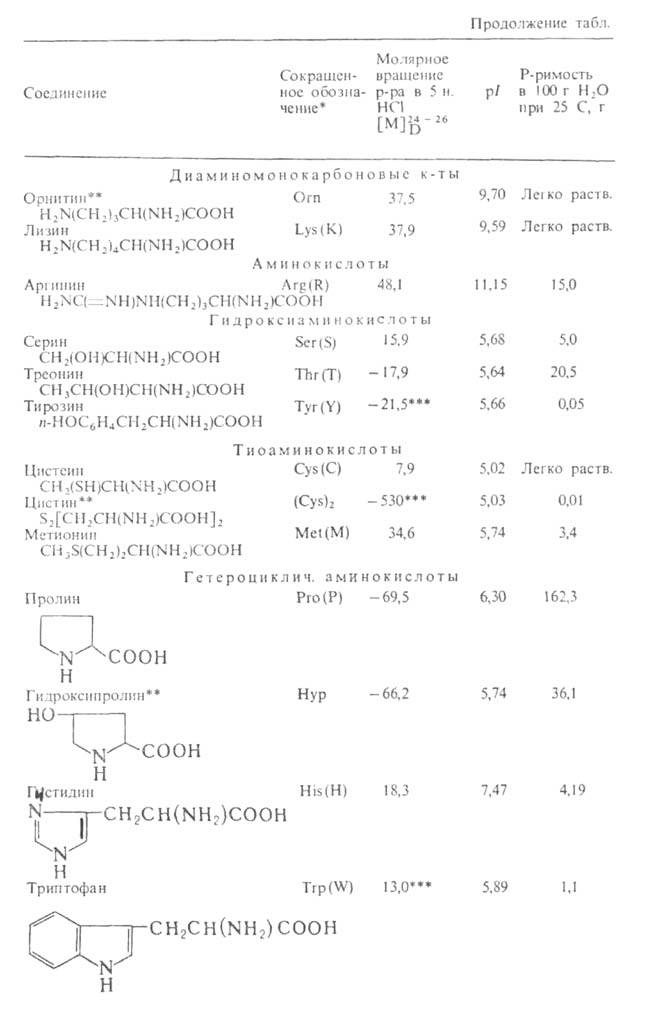
* В скобках дается однобукв. обозначение А., рекомендуемое ИЮПАК. ** Некодируемые А.к.: остальные кодируются генетич. кодом. *** Раствор в 1 н. HCl.
Табл. 2 — СВОЙСТВА АМИНОКИСЛОТ
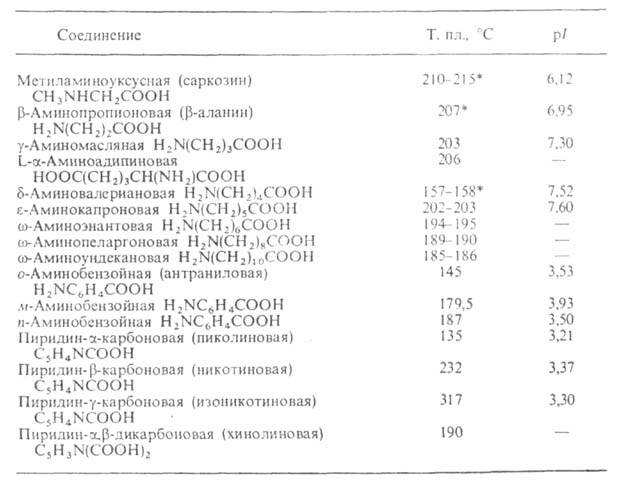

Цвиттер-ионная структура А. подтверждается их большим дипольным моментом (не менее 50∙10−30 Кл∙м), а также полосой поглощения 1610–1550 см −1 в ИК-спектре твердой А. или ее раствора.
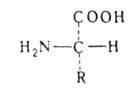
Все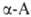 ., кроме аминоуксусной (глицина), имеют асимметрии, α-углеродный атом и существуют в виде двух энантиомеров. За редким исключением прир.
., кроме аминоуксусной (глицина), имеют асимметрии, α-углеродный атом и существуют в виде двух энантиомеров. За редким исключением прир.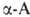 . относятся к L-ряду (S-конфигурация) и имеют след. пространств. строение:
. относятся к L-ряду (S-конфигурация) и имеют след. пространств. строение:
При переходе от нейтральных растворов к кислым для А. L-ряда увеличивается положит. вращение, для D-ряда-отрицательное. Гидроксипролин, треонин, изолейцин имеют два асимметрич. атома и образуют по две пары диастереомеров. Оптич. активность А. сильно зависит от длины волны поляризованного света (дисперсия оптич. вращения). Как правило, А. более устойчивы к рацемизации, чем их производные. Повышенной конфигурационной стабильностью отличаются N-бензилоксикарбонильные производные А.
Расщепление рацематов А. на оптич. антиподы производят затравочной кристаллизацией их солей с арилсульфокислотами или кристаллизацией диастереомерных солей ацильных производных А. с оптически активными основаниями или солей эфиров А. с оптически активными кислотами. Часто используют энантиоселективный гидролиз ацилами-нокислот ацилазами или гидролиз эфиров А. эстеразами, причем ферменты атакуют в первую очередь L-A. Перспективно расщепление рацематов лигандообменной хроматографией. Хроматографию используют также для анализа энантиомерного состава А.
Химические свойства. Реакции по карбоксильным группам А., аминогруппа которых защищена ацилированием или солеобразованием, протекают аналогично превращениям карбоновых кислот. А. легко образуют соли, сложные эфиры, амиды, гидразиды, азиды, тиоэфиры, галогенангидриды, смешанные ангидриды и т. д. Эфиры А. под действием натрия или магнийорг. соед. превращаются в аминоспирты. При сухой перегонке в присутствии Ba(OH)2 А. декарбоксилируются.
Реакции аминогрупп А. аналогичны превращениям аминов. А. образуют соли с минер. кислотами и пикриновой кислотой, легко ацилируются хлорангидридами кислот в водно-щелочном растворе (реакция Шоттена — Баумана) и алкилируются алкилгалогенидами. Метилиодид и диазометан превращают А. в бетаины . С формалином А. дают мегилольные или метиленовые производные, а в присутствии муравьиной кислоты или каталитически активированного H2-N,N-диметиламинокислоты. Под действием HNO2 ароматич. аминогруппы диазотируются, а алифатические замещаются на гидроксил. При обработке эфиров А. изоцианатами и изотиоцианатами образуются производные мочевины и тиомочевины. При нагр. с содой или при одноврем. воздействии алкоголята и CO2 А. дают соли или эфиры N-карбоксипроизводных А., а при использовании CS2-аналогичные дитиокарбаматы.
. С формалином А. дают мегилольные или метиленовые производные, а в присутствии муравьиной кислоты или каталитически активированного H2-N,N-диметиламинокислоты. Под действием HNO2 ароматич. аминогруппы диазотируются, а алифатические замещаются на гидроксил. При обработке эфиров А. изоцианатами и изотиоцианатами образуются производные мочевины и тиомочевины. При нагр. с содой или при одноврем. воздействии алкоголята и CO2 А. дают соли или эфиры N-карбоксипроизводных А., а при использовании CS2-аналогичные дитиокарбаматы.
Реакции с одноврем. участием групп NH2 и COOH наиб. характерны для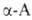 ., которые способны образовывать устойчивые 5-членные гетероциклы. С ионами переходных металлов (Cu, Zn, Ni, Co, Pb, Ag, Hg, Cr)
., которые способны образовывать устойчивые 5-членные гетероциклы. С ионами переходных металлов (Cu, Zn, Ni, Co, Pb, Ag, Hg, Cr) 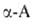 . образуют прочные хелатные комплексы, что используется в комплексонах и в комплексообразующих ионообменных смолах на основе аминокарбоновых и аминофосфоновых кислот. При взаимодействии с фосгеном
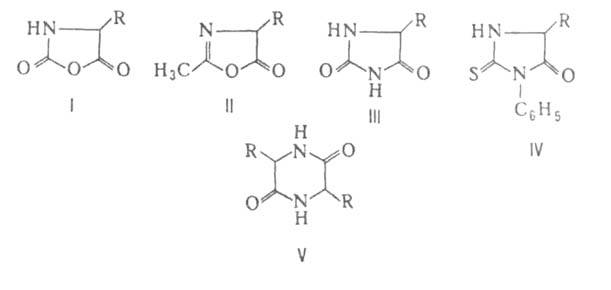
. образуют прочные хелатные комплексы, что используется в комплексонах и в комплексообразующих ионообменных смолах на основе аминокарбоновых и аминофосфоновых кислот. При взаимодействии с фосгеном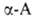 . превращаются в циклич. ангидриды N-карбоксиаминокислот (формула I), а при нагр. с уксусным ангидридом или ацетилхлоридом — в азлактоны (II); нагревание А. с мочевиной или обработка изоцианатами дает гидантоины (III), а при использовании
. превращаются в циклич. ангидриды N-карбоксиаминокислот (формула I), а при нагр. с уксусным ангидридом или ацетилхлоридом — в азлактоны (II); нагревание А. с мочевиной или обработка изоцианатами дает гидантоины (III), а при использовании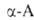 ., и особенно легко их эфиры, при нагр. превращаются в 2,5-пиперазиндионы, или дикетопиперазины (V).
., и особенно легко их эфиры, при нагр. превращаются в 2,5-пиперазиндионы, или дикетопиперазины (V).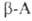 . при нагр. дезаминируются и образуют
. при нагр. дезаминируются и образуют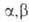 -ненасыщенные кислоты,
-ненасыщенные кислоты, 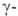 и
и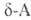 . отщепляют воду и образуют 5- и 6-членные лактамы.
. отщепляют воду и образуют 5- и 6-членные лактамы.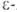 Аминокапроновая кислота при нагр. образует в осн. полиамид и лишь частично превращ. в капролактам, что характерно и для А. с большим числом метиленовых звеньев между функц. группами. Бетаины
Аминокапроновая кислота при нагр. образует в осн. полиамид и лишь частично превращ. в капролактам, что характерно и для А. с большим числом метиленовых звеньев между функц. группами. Бетаины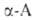 . при нагр. могут обратимо превращ. в эфиры диметиламинокислот, напр.:
. при нагр. могут обратимо превращ. в эфиры диметиламинокислот, напр.: 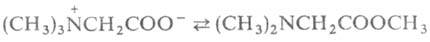 . При элиминировании триметиламина оетаины
. При элиминировании триметиламина оетаины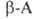 . превращ. в ненасыщ. кислоты,
. превращ. в ненасыщ. кислоты, 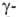 и
и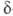 -бетаины — в циклич. лактоны. При окислении
-бетаины — в циклич. лактоны. При окислении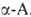 . образуют альдегиды с укороченной углеродной цепочкой. Из-за положит. заряда на четвертичном атоме N бетаины не образуют солей со щелочами. По аналогичной причине аминосульфоновые и аминофосфоновые кислоты не образуют солей с кислотами.арилизотиоцианатовтиогидантоины (IV).
. образуют альдегиды с укороченной углеродной цепочкой. Из-за положит. заряда на четвертичном атоме N бетаины не образуют солей со щелочами. По аналогичной причине аминосульфоновые и аминофосфоновые кислоты не образуют солей с кислотами.арилизотиоцианатовтиогидантоины (IV).
Анализ. Обычно анализ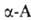 . основан на взаимод. с нингидрином, в результате которого А. расщепляется до альдегида, CO2 и NH3, a NH3 образует с нингидрином фиолетовый краситель. Для количеств. определения измеряют объем выделившегося CO2 или, чаще, фотометрируют образующийся краситель. Последний метод используется в автоматич. хроматографах, позволяющих разделять на сульфокатионитах и количественно анализировать сложные смеси аминокислот и пептидов. Еще более чувствителен флуоресцентный анализ продуктов реакции А. с о-фталевым диальдегидом. Быстро развивается лигандообменный хроматографический анализ А. и пептидов на силикагельных сорбентах в присутствии ионов меди. Бумажная и тонкослойная хроматография чаще используются для качественного анализа. Измерение объема N2, выделяющегося при дезаминировании А. азотистой кислотой, а также титрование А. щелочью в избытке формалина (методы Ван Слайка и Сёренсена ) сохранили лишь историческое значение.
. основан на взаимод. с нингидрином, в результате которого А. расщепляется до альдегида, CO2 и NH3, a NH3 образует с нингидрином фиолетовый краситель. Для количеств. определения измеряют объем выделившегося CO2 или, чаще, фотометрируют образующийся краситель. Последний метод используется в автоматич. хроматографах, позволяющих разделять на сульфокатионитах и количественно анализировать сложные смеси аминокислот и пептидов. Еще более чувствителен флуоресцентный анализ продуктов реакции А. с о-фталевым диальдегидом. Быстро развивается лигандообменный хроматографический анализ А. и пептидов на силикагельных сорбентах в присутствии ионов меди. Бумажная и тонкослойная хроматография чаще используются для качественного анализа. Измерение объема N2, выделяющегося при дезаминировании А. азотистой кислотой, а также титрование А. щелочью в избытке формалина (методы Ван Слайка и Сёренсена ) сохранили лишь историческое значение.
Получение.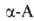 . получают галогенированием карбоновых кислот или эфиров в α-положение с послед. заменой галогена на аминогруппу при обработке амином, аммиаком или фталимидом калия (по Габриелю).
. получают галогенированием карбоновых кислот или эфиров в α-положение с послед. заменой галогена на аминогруппу при обработке амином, аммиаком или фталимидом калия (по Габриелю).
По Штреккеру — Зелинскому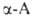 . получают из альдегидов:
. получают из альдегидов:
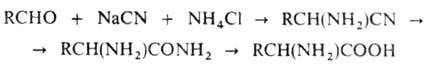
Этот метод позволяет также получать нитрилы и амиды соответствующих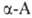 . По сходному механизму протекает образование α-аминофосфоновых кислот по реакции Кабачника — Филдса, напр.:
. По сходному механизму протекает образование α-аминофосфоновых кислот по реакции Кабачника — Филдса, напр.:
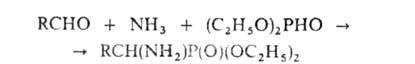
В этой реакции вместо альдегидов м. б. использованы кетоны, а вместо диалкилфосфитов — диалкилтиофосфиты, кислые эфиры алкил(арил)фосфонистых кислот RP(OH)OR и диарилфосфиноксиды Ar2НРО. Таким путем получен широкий набор комплексонов.
Альдегиды и кетоны или их более активные производные — кетзли служат исходными соед. для синтеза α-А. с увеличением числа углеродных атомов на две единицы. Для этого их конденсируют с циклич. производными аминоуксусной кислоты — азалакгонами, гидантоинами, тиогидантоинами, 2,5-пиперазиндионами или с ее медными или кобальтовыми хелатами, напр.:
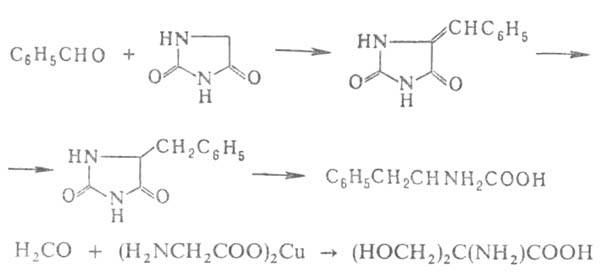
Удобные предшественники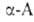 .-аминомалоновый эфир и нитроуксусный эфир. К их α-углеродным атомам можно предварительно ввести желаемые радикалы методами алкилирования или конденсации. α-Кетокислоты превращ. в
.-аминомалоновый эфир и нитроуксусный эфир. К их α-углеродным атомам можно предварительно ввести желаемые радикалы методами алкилирования или конденсации. α-Кетокислоты превращ. в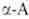 . гидрированием в присутствии NH3 или гидрированием их оксимов или гидразонов.
. гидрированием в присутствии NH3 или гидрированием их оксимов или гидразонов.
Некоторые L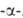 А. ввиду сложности синтеза и разделения оптич. изомеров получают микробиол. способом (лизин, триптофан, треонин) или выделяют из гидролизатов прир. белковых продуктов (пролин, цистин, аргинин, гистидин). Перспективны смешанные химически-ферментативные способы синтеза, напр.:
А. ввиду сложности синтеза и разделения оптич. изомеров получают микробиол. способом (лизин, триптофан, треонин) или выделяют из гидролизатов прир. белковых продуктов (пролин, цистин, аргинин, гистидин). Перспективны смешанные химически-ферментативные способы синтеза, напр.:
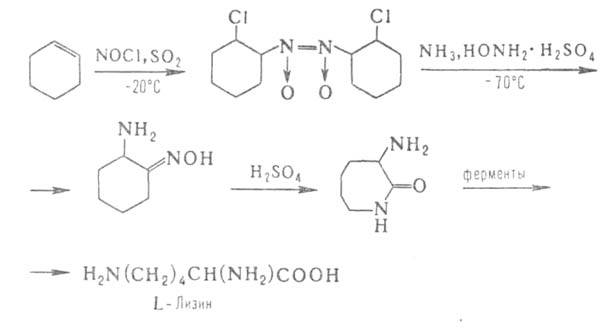
α- Аминосульфоновые кислоты получают при обработке аммиаком продуктов присоединения NaHSO3 к альдегидам:
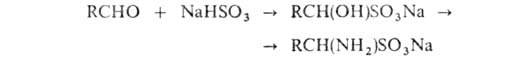
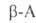 . синтезируют присоединением NH3 или аминов к
. синтезируют присоединением NH3 или аминов к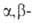 ненасыщенным кислотам, а также по методу Родионова — конденсацией альдегидов с малоновой кислотой в присутствии NH3:
ненасыщенным кислотам, а также по методу Родионова — конденсацией альдегидов с малоновой кислотой в присутствии NH3:
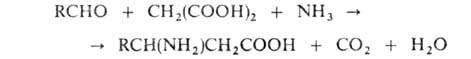
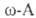 . получают гидролизом соответствующих лактамов (напр.,
. получают гидролизом соответствующих лактамов (напр., 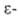 капролактама), которые образуются в результате перегруппировки Бекмана из оксимов циклич. кетонов под действием H2SO4.
капролактама), которые образуются в результате перегруппировки Бекмана из оксимов циклич. кетонов под действием H2SO4.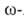 Аминоэнантовую,
Аминоэнантовую, 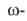 аминопеларгоновую и
аминопеларгоновую и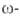 аминоундекановую кислоты синтезируют из
аминоундекановую кислоты синтезируют из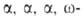 тетрахлоралканов путем их гидролиза конц. H2SO4 до
тетрахлоралканов путем их гидролиза конц. H2SO4 до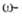 хлоралкановых кислот с послед. аммонолизом:
хлоралкановых кислот с послед. аммонолизом:
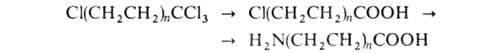
Исходные тетрахлоралканы получают теломеризациеи этилена с CCl4.
Ароматич. А. синтезируют восстановлением нитробензойных кислот или окислением толуидинов после предварит. бензоилирования аминогруппы. Антраниловую кислоту получают из фталевого ангидрида:
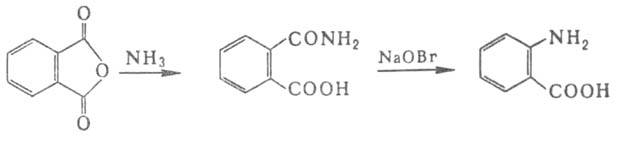
Для синтеза ., меченных изотопами 15N и 14С, обычно пользуются методами Габриеля и Штреккера соответственно. Меченные 3Н А. получают из ненасыщ. предшественников.
., меченных изотопами 15N и 14С, обычно пользуются методами Габриеля и Штреккера соответственно. Меченные 3Н А. получают из ненасыщ. предшественников.
Сульфаниловая кислота образуется при нагр. сульфата анилина до 180 °C. Ее мета-изомер получают сульфированием нитробензола с послед. восстановлением нитрогруппы.
Применение. Наиб. интерес представляют 20 L А. (аланин, аргинин, аспарагин и др.), входящих в состав белковых молекул. Смеси L-A., а также индивидуальные А. (напр., метионин) применяют в медицине для парэнтерального питания больных с заболеваниями пищеварит. и др. органов, при нарушениях обмена веществ и др.; лизин, метионин, треонин, триптофан — в животноводстве для обогащения кормов; глутамат натрия и лизин — в пищ. промышленности.
А. (аланин, аргинин, аспарагин и др.), входящих в состав белковых молекул. Смеси L-A., а также индивидуальные А. (напр., метионин) применяют в медицине для парэнтерального питания больных с заболеваниями пищеварит. и др. органов, при нарушениях обмена веществ и др.; лизин, метионин, треонин, триптофан — в животноводстве для обогащения кормов; глутамат натрия и лизин — в пищ. промышленности.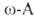 . и их лактамы служат для пром. производства полиамидов.
. и их лактамы служат для пром. производства полиамидов.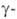 Аминомасляная кислота (аминалон) — медиатор в центр. нервной системе, применяется как лекарственное средство при сосудистых заболеваниях головного мозга. Ароматич. А. используют в синтезе красителей и лекарственных средств. На основе аминокарбоновых и аминофосфоновых кислот синтезируют селективные комплексоны, комплексообразующие иониты, лигандообменные сорбенты, ПАВ.
Аминомасляная кислота (аминалон) — медиатор в центр. нервной системе, применяется как лекарственное средство при сосудистых заболеваниях головного мозга. Ароматич. А. используют в синтезе красителей и лекарственных средств. На основе аминокарбоновых и аминофосфоновых кислот синтезируют селективные комплексоны, комплексообразующие иониты, лигандообменные сорбенты, ПАВ.
Лит.: Гринштейн Дж., ВиницМ., Химия аминокислот и пептидов, пер. с англ., [М.], 1965; Шредер Э., Любке К., Пептиды, пер. с англ., т. 1–2, М., 1967–69; Кабачник М.И. [и др.], "Успехи химии", 1968, т. 37, в. 7, с. 1161–91; Химия полипептидов, пер. с англ., М., 1977. См. также лит. при ст. белки.
В. А. Даванков
Значения в других словарях
- аминокислоты — -лот, мн. (ед. аминокислота, -ы, ж.). Органические вещества, входящие в состав всех белковых веществ животных и растительных организмов. Малый академический словарь
- Аминокислоты — Класс органических соединений, объединяющих в себе свойства кислот и аминов, т. е. содержащих наряду с карбоксильной группой —COOH аминогруппу —NH2. В зависимости от положения аминогруппы относительно карбоксильной группы различают α-, β-, γ- и др. А. Большая советская энциклопедия
- аминокислоты — АМИНОКИСЛОТЫ, органические (карбоновые) кислоты, содержащие наряду с карбоксильной группой (СООН) одну или неск. аминогрупп (NH2); осн. структурная часть молекулы белков. Ветеринарный энциклопедический словарь
- аминокислоты — АМИНОКИСЛОТЫ Класс органических соединений, содержащих карбоксильные и аминогруппы. Основные структурные единицы молекул белков, определяющие их биологическую специфичность. (Терминология спорта. Толковый словарь спортивных терминов, 2001) Словарь спортивных терминов
- аминокислоты — АМИНОКИСЛОТЫ, органич. (карбоновые) к-ты, содержащие, как правило, одну или две аминогруппы ( — NH2). В зависимости от расположения аминогруппы относительно карбоксила различают α, β, γ и т. д. А. Все природные белки построены из 20 α-А. (специфич. Сельскохозяйственный словарь
- аминокислоты — АМИНОКИСЛОТЫ — органические кислоты, содержащие одну или две аминогруппы (NH2) и карбоксильные группы (—СООН), определяющие их амфотерные свойства и образование специфических пептидных связей при соединении их между собой в макромолекулы белка. Ботаника. Словарь терминов
- аминокислоты — Органические (карбоновые) кислоты, содержащие, как правило, одну или две аминогруппы (— NH2). В зависимости от положения аминогруппы в углеродной цепи по отношению к карбоксилу различают а-, b-, y-и т. д. А. в природе широко распространены a -А. Биологический энциклопедический словарь
- аминокислоты — Низкомолекулярные органические соединения, содержащие одну или две карбоксильные группы (—СООН) и одну или две аминогруппы (—NH2). Аминокислоты широко представлены в клетках и тканях живых организмов. Биология. Современная энциклопедия
- Аминокислоты — I Аминокислоты (синоним аминокарбоновые кислоты) органические соединения, молекулы которых содержат аминогруппы (NH2-группы) и карбоксильные группы (СООН-группы); являются элементами, из которых построены пептиды и белки. Известно около 200 природных... Медицинская энциклопедия
- аминокислоты — АМИНОКИСЛОТЫ -лот; мн. (ед. аминокислота, -ы; ж.). Органические вещества, сочетающие свойства кислот и оснований (являются основным элементом построения всех белков животных и растительных организмов). Толковый словарь Кузнецова
- Аминокислоты — Название, употребляемое в последнее время в некоторых руководствах органической химии взамен названия "амидокислоты", что более правильно, ибо в этих соединениях NH2-группа замещает не кислотный гидроксил, как в амидах, а алкогольный, как в аминах. Энциклопедический словарь Брокгауза и Ефрона
- аминокислоты — аминокислоты мн. Органические соединения, обладающие свойствами кислот и щелочей и являющиеся основным элементом растительных и животных белков. Толковый словарь Ефремовой
- аминокислоты — Органические кислоты, содержащие группу NH2 Большой словарь иностранных слов
- АМИНОКИСЛОТЫ — АМИНОКИСЛОТЫ — класс органических соединений, содержащих карбоксильные (-COOH) и аминогруппы (-NH2); обладают свойствами и кислот, и оснований. Большой энциклопедический словарь
- аминокислоты — АМИНОКИСЛОТЫ, от, ед. аминокислота, ы, ж. (спец.). Класс органических соединений, обладающих свойствами и кислот, и оснований. | прил. аминокислотный, ая, ое. Толковый словарь Ожегова
