фенилизоцианат
ФЕНИЛИЗОЦИАНАТ C6H5N=C=O
мол. м. 119,12; бесцветная жидкость с резким запахом; т. пл. −32,3 °C, т. кип. 161,7 °C, 48 °C/1O мм рт. ст.; d204 1,0956; n20D 1,5368; давление пара 4,5∙102 Па (30 °C); 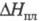 105 кДж/кг;
105 кДж/кг; 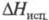 323 кДж/кг (165 °C); Cp 1,51 кДж/(кг∙ К) (200 °C); μ 7,52∙10−30 Кл∙м. Хорошо раств. в большинстве апротонных растворителей.
323 кДж/кг (165 °C); Cp 1,51 кДж/(кг∙ К) (200 °C); μ 7,52∙10−30 Кл∙м. Хорошо раств. в большинстве апротонных растворителей.
Ф. обладает свойствами ароматич. изоцианатов. При взаимодействии со спиртами образует соответствующие кристаллич. фенил-уретаны C6H5NCOOR, под действием воды разлагается:
С 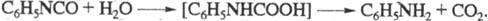
аммиаком Ф. образует N-фенилмочевину, с анилином -N,N-дифенилмочевину, с диметиламином — N,N-диметил-N'-фенилмочевину (гербицид фенурон): C6H5N = C = O + NH(CH3)2 C6H5NHCON(CH3)2. При взаимодействии с карбоновыми кислотами превращается в смешанный ангидрид, который может распадаться до симметричного ангидрида и анилина:
C6H5NHCON(CH3)2. При взаимодействии с карбоновыми кислотами превращается в смешанный ангидрид, который может распадаться до симметричного ангидрида и анилина:
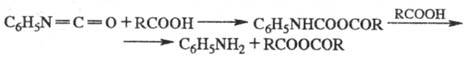
При действии H2SO4 Ф. превращается в сульфаниловую кислоту: C6H5NCO + H2SO4 [C6H5NHCOSO3H]
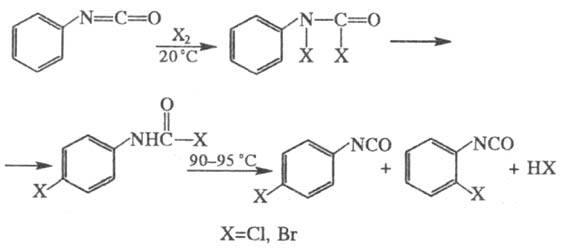
[C6H5NHCOSO3H] n-NH2C6H5SO3H. С галогенами дает дигалогенпроизводные, которые при нагр. перегруппировываются в смесь орто- и пара- замещенных Ф.:
n-NH2C6H5SO3H. С галогенами дает дигалогенпроизводные, которые при нагр. перегруппировываются в смесь орто- и пара- замещенных Ф.:
Гидрирование Ф. в присутствии Ni при 190 °C приводит к смеси анилина, N-метиланилина, дифенилмочевины, CH4 и CO2; LiAlH4 восстанавливает Ф. до N-метиланилина (выход 70–90%). В присут. триалкилфосфинов при 10 °C Ф. образует димер, в присутствии оснований (CH3COOK, CH3ONa, Na2CO3 и др.) — тример.
Ф. в бензоле при 20–25 °C катализирует дегидратацию и декарбоксилирование гидроксииминокислот в нитрилы (выход более 90%): HON = CHC6H4COOH  C6H5CN + CO2 + H2O; в присутствии следов триэтиламина — дегидратацию нитроалканов до нитрилоксидов.
C6H5CN + CO2 + H2O; в присутствии следов триэтиламина — дегидратацию нитроалканов до нитрилоксидов.
В промышленности Ф. получают фосгенированием анилина. Пре-паративно синтезируют обработкой фенилдиазонийхлорида KOCN в присутствии Cu или взаимод. дифенилмочевины с фосгеном в хлорнафталине (150 °C, выход 70–80%).
Ф. применяют в синтезе уретанов, дисперсных красителей, гербицида фенурона, используют для идентификации спиртов, фенолов и др. гидроксисоединений.
T. всп. 51 °C, т. воспл. 645 °C. Раздражает слизистые оболочки дыхат. путей и глаз.
Лит.: Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 654, 694; Горбатенко В. И., Журавлев E. 3., Самарай Л. И., Изоцианаты. Методы синтеза и физико-химические свойства алкил , арил- и гетерилизоциана-тов, К., 1987; Ullmann's Encyklopadie, 4 Aufl., Bd 13, Weinheim, 1977, S. 348.
С. И. Диденко
Значения в других словарях
- Фенилизоцианат — См. Фенилкарбимид. Энциклопедический словарь Брокгауза и Ефрона
