углерода сульфоксид
УГЛЕРОДА СУЛЬФОКСИД (сульфидоксид углерода, сероксид углерода, карбонилсульфид) COS
мол. м. 60,076; бесцветный газ со слабым запахом; молекула линейна, длина связи С — О 0,116 нм, C-S 0,156 нм, μ 2,40∙10−30 Кл∙м; т. пл. −138,82 °C, т. кип. −50,24 °C; плотн. 1,073 г/дм3 (0 °C), 1,24 г/см3 ( −87 °C); C0p 41,5 Дж/(моль∙К); ΔHисп 18,5 кДж/моль, ΔHпл 4,73 кДж/моль, ΔH0обр −142,4 кДж/моль; 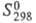 231,5 Дж/(моль∙К); уравнение температурной зависимости давления пара lg p (мм рт. ст.) = -1003,9/Т+ 7,383 (193 < Т< 223). Твердый У. с. кристаллизуется в ромбоэдрич. решетке (а — 0,408 нм, α = 95,97° при −196 °C, Z=1, пространственная группа R3m). При нагревании У. с. разлагается до CO и S, диспропорционирует на CO2 и CS2. Растворимость У. с., мл в 100 мл: в воде — 54, этаноле — 800. Хорошо раств. в CS2. У. с. легко воспламеняется, сгорая до CO2 и SO2. Образует соли типа
231,5 Дж/(моль∙К); уравнение температурной зависимости давления пара lg p (мм рт. ст.) = -1003,9/Т+ 7,383 (193 < Т< 223). Твердый У. с. кристаллизуется в ромбоэдрич. решетке (а — 0,408 нм, α = 95,97° при −196 °C, Z=1, пространственная группа R3m). При нагревании У. с. разлагается до CO и S, диспропорционирует на CO2 и CS2. Растворимость У. с., мл в 100 мл: в воде — 54, этаноле — 800. Хорошо раств. в CS2. У. с. легко воспламеняется, сгорая до CO2 и SO2. Образует соли типа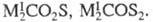
У. с. получают взаимод. NH4NCS с водным раствором H2SO4 или CO с парами S при 350 °C. У. с. используют в производстве ускорителей вулканизации, фунгицидов, гербицидов, для получения тиокарбаминовых кислот и их солей, а также для получения мочевины.
У. с. взрывоопасен и токсичен (поражает центр, нервную систему); ПДК в воздухе рабочей зоны 10,0 мг/м3, в атм. воздухе 0,1 мг/м3. КПВ 26,5 — 11,9% по объему.
И. Н. Один
