серин
СЕРИН (2-амино-3-гидроксипропионовая кислота, β-гидроксиаланин, Ser, S) HOCH2CH(NH2)СООН
мол. м. 105,09; бесцветные кристаллы. Для L-изомера т. пл. 228 °C (с разл.), 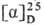 + 14,45° (конц. 0,5 г в 100 мл 5,6 н. HCl). Для D- и D, L-C. т. пл. соотв. 228 °C и 246 °C (с разл.); т. возг. для D, L- и L-C. 150 °C/10−4 мм рт. ст.; раств. в воде, не раств. в этаноле и диэтиловом эфире. При 25 °C рКa 2,21 (COOH), 9,15 (NH2); pI 5,68. L-C. имеет сладковатый вкус.
+ 14,45° (конц. 0,5 г в 100 мл 5,6 н. HCl). Для D- и D, L-C. т. пл. соотв. 228 °C и 246 °C (с разл.); т. возг. для D, L- и L-C. 150 °C/10−4 мм рт. ст.; раств. в воде, не раств. в этаноле и диэтиловом эфире. При 25 °C рКa 2,21 (COOH), 9,15 (NH2); pI 5,68. L-C. имеет сладковатый вкус.
С. обладает свойствами аминокислот и спиртов. О-Ацилирование С. осуществляют в нейтральной или кислой среде, N-ацилирование — в сильно щелочной. О-Ацилсерин может претерпевать О,N-ацильную перегруппировку. При энергичном восстановлении (напр., при действии HI и Р) С. переходит в аланин. При нагр. со щелочами С. распадается с образованием пировиноградной кислоты; при периодатном окислении образует формальдегид, NH3 и глиоксиловую кислоту; с формальдегидом образует 1,3-оксазолидин-4-карбо-новую кислоту. В синтезе пептидов гидроксигруппу С. защищают бензильной или трет-бутильной группами.
Остаток L-C. встречается во всех организмах в составе молекул белков, особенно много их в фиброине шелка; остаток С. входит также в молекулу фосфатидилсерина. Активность ряда ферментов (трипсин, химотрипсин, холин-эстераза) связана со специфич. реакц. способностью гидроксигруппы остатка С., входящего в структуру их активных центров.
С. — кодируемая заменимая аминокислота, образуется в организме в результате трансаминирования и послед. дефосфорилирования 3-фосфопировиноградной кислоты, участвует в биосинтезе триптофана и серосодержащих аминокислот, обратимо расщепляется на глицин и формальдегид, претерпевает дезаминирование, превращаясь в пировиноградную кислоту. Из С. в организме синтезируются этанол-амин и холин.
Синтез С. осуществляют гидроксигалогенированием и послед. аминированием акриловой кислоты или гидроксимети-лированием ацетамидомалонового эфира и послед. гидролизом продукта реакции, напр.:
HCHO + CH3С(O)NHCH(COOC2H5)2 : : CH3C(O)NHC(CH2OH)(COOC2H5)2 : С.
В спектре ПМР С. в D2 О хим. сдвиги протонов (в м. д.) у α-атома С составляют 3,846, у β-атома-3,989 и 3,95. Характерная цветная реакция на С. — действие йодной кислоты и реактива Несслера.
С. впервые выделен Э. Крамером в 1865 из шелка. Мировое производство L-C. ок. 130 т/год (1989). В.В.Баев.
Значения в других словарях
- Серин — Α-амино-β-оксипропионовая кислота, HOCH2CH (NH2) COOH, природная аминокислота. Существует в виде 2 оптически-активных — L- и D- и рацемической — DL-форм. Почти все белки содержат L-C. Большая советская энциклопедия
- серин — орф. серин, -а (хим.) Орфографический словарь Лопатина
- серин — Заменимая аминокислота. Содержится почти во всех белках. Богаты С. фиброин (до 16%) и серицин (до 40%) шёлка. Участвует в биосинтезе глицина, серусодержащих аминокислот (метионина, цистеина), боковой цепи триптофана, а также сфинголипидов и этаноламина. Биологический энциклопедический словарь
- СЕРИН — СЕРИН (НОСН2СН(NH2)COOH), белая кристаллическая АМИНОКИСЛОТА, встречающаяся в белках. Научно-технический словарь
- Серин — Заменимая в питании человека аминокислота (α-амино-β-окси-пропионовая кислота), входящая в состав белков (в т.ч. активных центров многих ферментов) и некоторых фосфатидов; промежуточный продукт биосинтеза цистеина и глицина. Медицинская энциклопедия
- СЕРИН — СЕРИН — алифатическая аминокислота CH2(OH)CH(NH2)COOH. Входит в состав белков и некоторых сложных липидов. Играет важную роль в проявлении каталитической активности многих расщепляющих белки ферментов (т. н. сериновых протеаз). Большой энциклопедический словарь
- Серин — C3H7NO3 — представляет α-амидоэтиленмолочную кислоту (оксиаланин) CH2OH—CHNH2—COOH; образуется он в качестве одного из продуктов распада под влиянием кипячения с разведенной серной кислотой так наз. шелкового клея (см. Серицин). Энциклопедический словарь Брокгауза и Ефрона
