окислительно-восстановительные ионообменные смолы
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ИОНООБМЕННЫЕ СМОЛЫ (редокс-иониты, электроноионообменники)
содержат группы, способные как к ионному обмену (подобно др. ионообменным смолам), так и к обратимому окислительно-восстановит. превращению в растворах окислительно-восстановит. систем. Указанные реакции могут протекать одновременно или независимо друг от друга. В зависимости от способа получения различают след. редокс-иониты (Р.-и.): синтетич., на основе ионообменных сорбентов и адсорбционные. В первых окислительно-восстановит. группа химически (необратимо) связана с полимерной матрицей (каркасом) смолы. Наиб. известны синтетические Р.-и. полимеризац. типа на основе сополимера стирола с дивинилбензолом; их получают арилированием хлорметилир. сополимера гидрохиноном, бензохиноном, диметоксибензолом или их производными с послед. сульфированием или аминированием (введение соотв. катионо- или анионообменных групп), напр.:
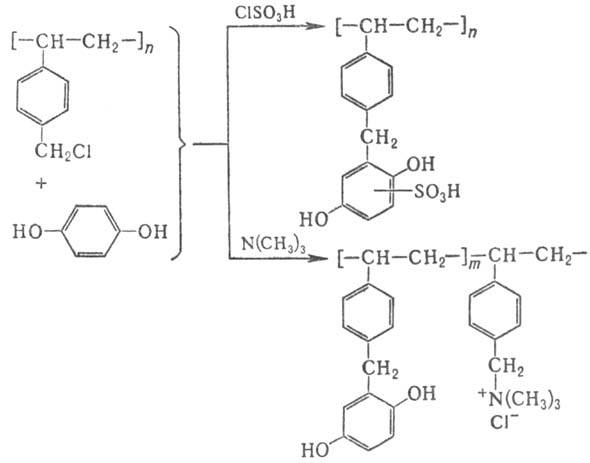
Из синтетических Р.-и. поликонденсац. типа наиб. распространены гидрохинон-фенол-формальдегидные; получены Р.-и. из фенола, формальдегида и многоядерных ароматич. дигидроксисоед., а также др. Недостатки этих Р.-и. — пониж. термостойкость и невысокие кинетич. характеристики из-за нерегулярности структуры.
Р.-и. на основе ионообменных сорбентов получают обработкой последних растворами солей переходных металлов или орг. соединений, обладающих окислительно-восстановит, свойствами; напр., катиониты насыщают ионами Fe2+, Sn2+, Ce3+, Ti3+ , Cu + , Cr3+ , метиленовым синим, метилвиолетом, фуксином, аниониты -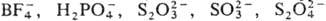 ,
, 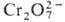 , тимолфталеином, гидрохиноном, дигидрохлоранилом. Ионы, участвующие в окислительно-восстановит. превращениях, связаны с полимерной матрицей ионными или координац. связями. Существ. недостаток таких Р.-и.-переход этих ионов в раствор вследствие гидролиза.
, тимолфталеином, гидрохиноном, дигидрохлоранилом. Ионы, участвующие в окислительно-восстановит. превращениях, связаны с полимерной матрицей ионными или координац. связями. Существ. недостаток таких Р.-и.-переход этих ионов в раствор вследствие гидролиза.
Наиб. практич. значение имеют адсорбционные Р.-и., в которых редокс-соед. расположены в порах или на поверхности ионообменного носителя (на практике — обычная ионообменная смола) и химически не связаны с ним. Синтез осуществляют в три стадии: 1) обработка катионита раствором соли переходного металла (на практике-соль Cu) для перевода в солевую форму, напр.:
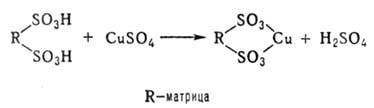
2) восстановление поглощенного носителем иона до своб. металла, который остается в порах носителя:
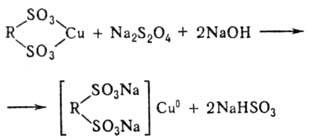
3) замена щелочного металла в носителе на H+ (т. е. перевод носителя в H+ — форму):
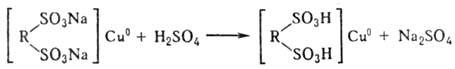
Многократным повторением первых двух стадий можно получить Р.-и., обладающие высокой окислительно-восстановит. емкостью; последняя соответствует концентрации редокс-групп (мг-экв.), участвующих в обратимом обмене электронами с водным раствором, в 1 г сухого Р.-и. По мере окисления металла его ионы не переходят в раствор, а поглощаются H+ формой носителя. Регенерирует такой Р.-и. по-следоват. обработкой щелочным агентом и кислотой (стадии 2 и 3).
Применяют преим. адсорбционные Р.-и. для подготовки воды в паросиловых энергетич. установках с целью одновременного удаления растворенного O2 и деионизации (либо умягчения), для удаления следов O2 из технол. воды, а также в медицине, биохимии, аналит. химии и т. д.
Лит.: Кассиди Г. Дж., Кун К. А., Окислительно-восстановительные полимеры (Редоксполимеры), пер. с англ., Л., 1967; Кожевников А. В., Электроно-ионообменники, Л., 1972; Кравченко Т. А., Николаев Н. И., Кинетика и динамика процессов в редоксидах, М., 1982; Иониты в химической технологии, под ред. Б. П. Никольского и П. Г. Романкова, Л., 1982.
В. Б. Каргман
