диффузионный потенциал
ДИФФУЗИОННЫЙ ПОТЕНЦИАЛ
разность потенциалов на границе двух соприкасающихся растворов электролитов. Обусловлен тем, что скорости переноса катионов и анионов через границу, вызванного различием их электрохим. потенциалов в растворах 1 и 2, различны. Наличие Д. п. может вызывать погрешность при измерениях электродного потенциала, поэтому Д. п. стремятся рассчитать или устранить. Точный расчет невозможен из-за неопределимости коэф. активности ионов, а также отсутствия сведений о распределении концентраций ионов в пограничной зоне между соприкасающимися растворами. Если в контакте находятся растворы одного и того же z, z — зарядного электролита (z — число катионов, равное числу анионов) разл. концентраций и можно считать, что числа переноса анионов и катионов, соотв. t+ и t_, не зависят от их активности, а коэф. активности анионов и катионов равны между собой в обоих растворах, то Д. п.
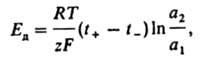
где a1 и а2 — средние активности ионов в растворах 1 и 2, Т — абс. температура, R — газовая постоянная, F — постоянная Фарадея. Имеются и др. приближенные формулы для определения Д. п. Снизить Д. п. до малой величины во мн. случаях можно, разделив растворы 1 и 2 "солевым мостиком" из концентрир. раствора соли, катионы и анионы которой имеют примерно равные числа переноса (KCl, NH4NO3 и др.).
Лит.: Феттер К., Электрохимическая кинетика, пер. с нем., М., 1967, с. 70–76; Ротинян А. Л., Тихонов К. И., Шошина И. А., Теоретическая электрохимия. Л., 1981, с. 131–35.
А. Д. Давыдов
