двойной электрический слой
ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ
тонкий поверхностный слой из пространственно разделенных электрич. зарядов противоположного знака, образующийся на границе двух фаз. Поскольку пространств. разделение зарядов всегда сопровождается возникновением электрич. разности потенциалов, Д. э.с. можно рассматривать как своеобразный микроконденсатор, расстояние между обкладками которого определяется молекулярными размерами. Образование Д.э.с. оказывает существенное влияние на скорость электродных процессов, адсорбцию ионов и нейтральных молекул, устойчивость дисперсных систем, смачиваемость, коэф. трения и др. свойства межфазных границ. В биол. системах процессы образования и разрушения Д. э. с. на клеточных мембранах сопровождают распространение электрич. импульсов вдоль нервных и мышечных волокон. Наиб. детально строение Д. э. с. изучено на границе между металлич. электродом и раствором электролита. При погружении металлич. электрода М в раствор электролита, содержащий ионы этого металла М+ (потенциалопределяющие ионы), устанавливается электрохим. равновесие, сопровождаемое выравниванием электрохим. потенциалов этих ионов в кристаллич. решетке металла и в растворе. Если первоначально электрохим. потенциал ионов М+ в металле 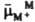 был больше электрохим. потенциала этих ионов в растворе
был больше электрохим. потенциала этих ионов в растворе 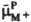 , то в процессе выравнивания этих величин некоторое количество ионов М+ переходит из металла в раствор и поверхность металла заряжается отрицательно. Притянутые к ней кулоновскими силами катионы из раствора (не обязательно М+) образуют положит. обкладку Д. э. с. Возникающая при этом электрич. разность потенциалов препятствует дальнейшему переходу ионов М+ из металла в раствор, что и приводит к установлению электрохим. равновесия. Если первоначально
, то в процессе выравнивания этих величин некоторое количество ионов М+ переходит из металла в раствор и поверхность металла заряжается отрицательно. Притянутые к ней кулоновскими силами катионы из раствора (не обязательно М+) образуют положит. обкладку Д. э. с. Возникающая при этом электрич. разность потенциалов препятствует дальнейшему переходу ионов М+ из металла в раствор, что и приводит к установлению электрохим. равновесия. Если первоначально 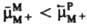 , то при установлении электрохим. равновесия часть ионов М+ из раствора переходит на металл, заряжая его поверхность положительно. Отрицат. обкладку Д. э.с. в этом случае составляют притянутые к поверхности металла анионы раствора. Путем подбора концентрации потенциалопределяющих ионов в растворе можно добиться такой ситуации, что условие
, то при установлении электрохим. равновесия часть ионов М+ из раствора переходит на металл, заряжая его поверхность положительно. Отрицат. обкладку Д. э.с. в этом случае составляют притянутые к поверхности металла анионы раствора. Путем подбора концентрации потенциалопределяющих ионов в растворе можно добиться такой ситуации, что условие 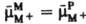 не требует перехода ионов М+ из металла в раствор или наоборот. В этом случае заряд поверхности металла равен нулю, а его потенциал, измеренный относительно к.-л. электрода сравнения, наз. потенциалом нулевого заряда. Условия положительно заряженной, отрицательно заряженной и незаряженной поверхности металла можно осуществить и в том случае, если в растворе электролита нет потенциалопределяющих ионов. Для этого необходимо внести в раствор кроме данного металлич. электрода М к.-л. вспомогат. электрод и подсоединить оба электрода к внеш. источнику постоянного напряжения. В зависимости от величины и знака напряжения источника можно произвольно изменять заряд q поверхности металла М. При q > 0 ионную обкладку Д. э. с.образуют притянутые из раствора анионы, при q < 0 — катионы. При потенциале нулевого заряда, когда q = 0, ионный Д.э.с. отсутствует, но разность потенциалов на границе раствор|металл (гальвани-потенциал) не равна нулю, т. к. на этой границе существуют т. наз. адсорбционный и электронный Д.э.с. Адсорбц. Д.э.с. связан с некулоновской (специфической) адсорбцией ионов или полярных молекул. Так, напр., на границе ртуть|водный раствор KI при q = 0 донорно-акцепторное взаимод. приводит к специфич. адсорбции анионов I−, которые уже вследствие кулоновского взаимод. притягивают эквивалентное количество катионов К+. При этом электрич. центры анионов I− оказываются ближе к поверхности ртути, чем электрич. центры катионов К+, и пространств. разделение зарядов ведет к образованию адсорбц. Д. э. с., отрицат. обкладка которого обращена в сторону металла. Полярные молекулы растворителя или растворенных нейтральных веществ, как правило, адсорбируются на электроде таким образом, что средняя нормальная к поверхности составляющая дипольного момента не равна нулю. Ориентиров. адсорбция диполей поэтому также приводит к образованию адсорбц. Д.э.с. Например, при адсорбции молекул бутилового спирта из водного раствора на незаряженной поверхности ртути гидрофобные углеводородные радикалы C4H9, несущие положит. заряд диполя, ориентированы в сторону поверхности, а гидрофильные OH-группы, на которых сосредоточен отрицат. заряд, ориентированы в сторону раствора. Адсорбц. Д.э.с. может образоваться также и при адсорбции неполярных частиц, если их донорно-акцепторное взаимод. с электродом сопровождается возникновением наведенного дипольного момента (напр., при адсорбции на электродах атомов Н или О). Электронный Д.э.с. обусловлен квантовомех. свойствами электронов в металлах и полупроводниках. Согласно совр. моделям металла как электронного газа и ионного остова электронный Д.э.с. связывают с тем, что электронный газ несколько выходит за пределы ионного остова, что и приводит к пространств. разделению зарядов. При этом своей положит. обкладкой Д. э. с. обращен к металлу, отрицательной — к контактирующей с металлом фазе (раствору или газу). В полупроводниках из-за малого количества носителей тока (электронов в зоне проводимости и "дырок" в валентной зоне) при наложении внеш. напряжения возникает их неравномерное пространств. распределение в поверхностном слое, которое рассматривают как электронный Д. э. с. внутри полупроводниковой фазы. В общем случае Д. э. с., вызванные разными причинами, накладываются друг на друга, что приводит к весьма сложной структуре границы раздела между электродом и раствором. Возникновение Д. э. с. на границе непроводящего твердого тела с раствором связано либо с адсорбцией, либо с взаимод. поверхностных ионогенных групп твердого тела с молекулами растворителя. Так, напр., кристаллы AgI, полученные по реакции KI + AgNO3 → AgI + KNO3, в растворах с избытком KI адсорбируют ионы I− и заряжаются отрицательно, в растворах с избытком AgNO3 адсорбируют ионы Ag+ и заряжаются положительно. При этом к заряженной поверхности AgI под действием электростатич. сил притягиваются ионы противоположного знака, образующие ионную обкладку Д.э.с. С другой стороны, взаимод. поверхностных ионогенных групп разл. оксидов с ионами H3O+ , OH− и молекулами воды в зависимости от pH раствора может приводить либо к положит., либо к отрицат. заряжению поверхности оксида.
не требует перехода ионов М+ из металла в раствор или наоборот. В этом случае заряд поверхности металла равен нулю, а его потенциал, измеренный относительно к.-л. электрода сравнения, наз. потенциалом нулевого заряда. Условия положительно заряженной, отрицательно заряженной и незаряженной поверхности металла можно осуществить и в том случае, если в растворе электролита нет потенциалопределяющих ионов. Для этого необходимо внести в раствор кроме данного металлич. электрода М к.-л. вспомогат. электрод и подсоединить оба электрода к внеш. источнику постоянного напряжения. В зависимости от величины и знака напряжения источника можно произвольно изменять заряд q поверхности металла М. При q > 0 ионную обкладку Д. э. с.образуют притянутые из раствора анионы, при q < 0 — катионы. При потенциале нулевого заряда, когда q = 0, ионный Д.э.с. отсутствует, но разность потенциалов на границе раствор|металл (гальвани-потенциал) не равна нулю, т. к. на этой границе существуют т. наз. адсорбционный и электронный Д.э.с. Адсорбц. Д.э.с. связан с некулоновской (специфической) адсорбцией ионов или полярных молекул. Так, напр., на границе ртуть|водный раствор KI при q = 0 донорно-акцепторное взаимод. приводит к специфич. адсорбции анионов I−, которые уже вследствие кулоновского взаимод. притягивают эквивалентное количество катионов К+. При этом электрич. центры анионов I− оказываются ближе к поверхности ртути, чем электрич. центры катионов К+, и пространств. разделение зарядов ведет к образованию адсорбц. Д. э. с., отрицат. обкладка которого обращена в сторону металла. Полярные молекулы растворителя или растворенных нейтральных веществ, как правило, адсорбируются на электроде таким образом, что средняя нормальная к поверхности составляющая дипольного момента не равна нулю. Ориентиров. адсорбция диполей поэтому также приводит к образованию адсорбц. Д.э.с. Например, при адсорбции молекул бутилового спирта из водного раствора на незаряженной поверхности ртути гидрофобные углеводородные радикалы C4H9, несущие положит. заряд диполя, ориентированы в сторону поверхности, а гидрофильные OH-группы, на которых сосредоточен отрицат. заряд, ориентированы в сторону раствора. Адсорбц. Д.э.с. может образоваться также и при адсорбции неполярных частиц, если их донорно-акцепторное взаимод. с электродом сопровождается возникновением наведенного дипольного момента (напр., при адсорбции на электродах атомов Н или О). Электронный Д.э.с. обусловлен квантовомех. свойствами электронов в металлах и полупроводниках. Согласно совр. моделям металла как электронного газа и ионного остова электронный Д.э.с. связывают с тем, что электронный газ несколько выходит за пределы ионного остова, что и приводит к пространств. разделению зарядов. При этом своей положит. обкладкой Д. э. с. обращен к металлу, отрицательной — к контактирующей с металлом фазе (раствору или газу). В полупроводниках из-за малого количества носителей тока (электронов в зоне проводимости и "дырок" в валентной зоне) при наложении внеш. напряжения возникает их неравномерное пространств. распределение в поверхностном слое, которое рассматривают как электронный Д. э. с. внутри полупроводниковой фазы. В общем случае Д. э. с., вызванные разными причинами, накладываются друг на друга, что приводит к весьма сложной структуре границы раздела между электродом и раствором. Возникновение Д. э. с. на границе непроводящего твердого тела с раствором связано либо с адсорбцией, либо с взаимод. поверхностных ионогенных групп твердого тела с молекулами растворителя. Так, напр., кристаллы AgI, полученные по реакции KI + AgNO3 → AgI + KNO3, в растворах с избытком KI адсорбируют ионы I− и заряжаются отрицательно, в растворах с избытком AgNO3 адсорбируют ионы Ag+ и заряжаются положительно. При этом к заряженной поверхности AgI под действием электростатич. сил притягиваются ионы противоположного знака, образующие ионную обкладку Д.э.с. С другой стороны, взаимод. поверхностных ионогенных групп разл. оксидов с ионами H3O+ , OH− и молекулами воды в зависимости от pH раствора может приводить либо к положит., либо к отрицат. заряжению поверхности оксида.
Методы изучения. Для исследования Д. э. с. используют в осн. три группы методов. Во-первых, адсорбц. методы, которые основаны на том, что образование Д.э.с. связано с адсорбцией разл. компонентов раствора и вызывает изменение их концентрации. В частности, адсорбц. методы широко используют для изучения Д.э.с., образованного на мелкодисперсных частицах в коллоидных системах. Во-вторых, методы, основанные на электрокапиллярных явлениях. Их сущность состоит в том, что образование Д. э. с. уменьшает работу, необходимую для создания новой поверхности раздела фаз, и тем самым приводит к зависимости межфазного натяжения от потенциала электрода. Применение электрокапиллярных методов ограничено границами раздела между жидкими фазами, на которых возможно непосредственное измерение межфазного натяжения; для твердых электродов эти методы дают лишь качеств. информацию о строении Д. э. с. В-третьих, методы, регистрирующие количество электричества, затраченного на создание определенного заряда электрода (заряжение Д. э. с.). Сюда относятся разл. гальваностатич. и потенциостатич. импульсные методы, а также метод измерения электрич. емкости Д. э. с. с помощью синусоидального переменного тока (см. импедансный метод). Для успешного применения этих методов необходимо, чтобы все подведенное к электроду электричество затрачивалось только на заряжение Д.э.с. и не расходовалось на электрохим. реакции. Электроды, удовлетворяющие этому требованию, наз. идеально поляризуемыми. Сведения о строении Д. э. с. на границе раствор|изолятор можно получить на основе изучения электрокинетических явлений. Д.э.с. изучают также с помощью оптич. методов (эллипсометрия, разл. варианты электроотражения света, комбинационное рассеяние в адсорбц. слое и др.). На основе указанных методов можно определить заряд поверхности электрода q, его зависимость от потенциала электрода Е, потенциал нулевого заряда Eq = 0, электрич. емкость Д. э. с., равную дq/дE, а также поверхностные избытки (адсорбции) разл. компонентов раствора в зависимости от Е (или q) и их объемной концентрации.
Современная теория Д.э.с., основной вклад в развитие которой внесли работы Г. Гельмгольца (1879), Ж. Гуи (1910), Д. Чапмена (1913), О. Штерна (1924) и Д. Грэма (1947–58), базируется на след. модели ионной обкладки Д. э. с. Благодаря тепловому движению ионы, адсорбировавшиеся на электроде только под действием кулоновских сил, распределяются у поверхности подобно молекулам газа в земной атмосфере и образуют диффузную часть Д.э.с. Границей диффузной части является т. наз. внеш. плоскость Гельмгольца х2 (рис.), до которой могут дойти электрич. центры ионов, участвующих в тепловом движении. Между внеш. плоскостью Гельмгольца и поверхностью металла располагается плотная часть Д. э. с., для которой характерна диэлектрич. проницаемость существенно меньшая, чем в объеме раствора. В плотном слое локализуется дипольный Д. э. с., образованный ориентированными диполями растворителя и орг. растворенного вещества. Кроме того, в плотную часть Д.э.с. входят специфически адсорбирующиеся ионы; при этом их электрич. центры образуют т. наз. внутр. плоскость Гельмгольца х1.
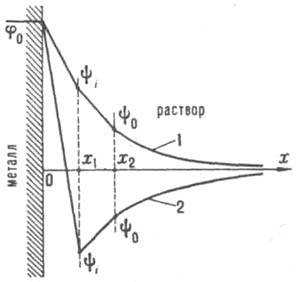
Схема распределения потенциала в двойном электрическом слое: 1 — при |q1| < |q|; 2 — при |q1| > |q|
В силу электронейтральности границы раздела плотность заряда q на электроде компенсируется зарядами специфически адсорбиров. ионов (q1) и ионов, находящихся в диффузной части Д. э. с. (q2): q= -q1-q2. Теория Д.э.с. позволяет связать величины q и q1, с электрич. разностями потенциала в плотной и диффузной частях Д.э.с. Так, падение потенциала в плотной части Д.э.с. описывается уравнением: yu = q/K02 + q1К12, где К02 и Kl2 — интегральные емкости соотв. всего плотного слоя и пространства между внутр. и внеш. плоскостями Гельмгольца. Падение потенциала в диффузном слое (потенциал внеш. плоскости Гельмгольца) в растворе 1,1-валентного электролита с концентрацией с равно: 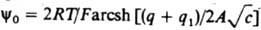 , где
, где 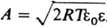 , ε0 — диэлектрич. постоянная, ε — диэлектрич. проницаемость растворителя, a R, Т и F — соотв. газовая постоянная, температура и число Фарадея. Потенциал внутр. плоскости Гельмгольца рассчитывают по формуле: yi = (q + λq1)/Kl2 + y0, где λ [ 1 — коэф., характеризующий дискретность специфически адсорбиров. ионов. Если |q1| > |q|, то говорят, что произошла "перезарядка поверхности" специфически адсорбиров. ионами. В этом случае потенциалы y0 и yi, имеют знак, противоположный знаку общего скачка потенциала в ионном Д. э. с. j0 = yu + y0 (см. рис., кривая 2). Для развития теории дипольного Д.э.с., связанного с адсорбцией молекул растворителя, успешно используется зависимость емкости К02 от q. Теоретич. расчеты электронного Д.э.с. пока крайне противоречивы; с целью упрощения принято считать, что скачок потенциала в электронном Д. э. с. металла не зависит от q и потому не вносит вклада в наблюдаемые эффекты. Изучение свойств и строения Д. э. с. имеет большое значение для понимания и усовершенствования таких практически важных процессов, как электролиз, электроосаждение металлов, электрохим. реакции в хим. источниках тока, коррозия металлов, коагуляция в коллоидных системах, флотация, ионный обмен и др.
, ε0 — диэлектрич. постоянная, ε — диэлектрич. проницаемость растворителя, a R, Т и F — соотв. газовая постоянная, температура и число Фарадея. Потенциал внутр. плоскости Гельмгольца рассчитывают по формуле: yi = (q + λq1)/Kl2 + y0, где λ [ 1 — коэф., характеризующий дискретность специфически адсорбиров. ионов. Если |q1| > |q|, то говорят, что произошла "перезарядка поверхности" специфически адсорбиров. ионами. В этом случае потенциалы y0 и yi, имеют знак, противоположный знаку общего скачка потенциала в ионном Д. э. с. j0 = yu + y0 (см. рис., кривая 2). Для развития теории дипольного Д.э.с., связанного с адсорбцией молекул растворителя, успешно используется зависимость емкости К02 от q. Теоретич. расчеты электронного Д.э.с. пока крайне противоречивы; с целью упрощения принято считать, что скачок потенциала в электронном Д. э. с. металла не зависит от q и потому не вносит вклада в наблюдаемые эффекты. Изучение свойств и строения Д. э. с. имеет большое значение для понимания и усовершенствования таких практически важных процессов, как электролиз, электроосаждение металлов, электрохим. реакции в хим. источниках тока, коррозия металлов, коагуляция в коллоидных системах, флотация, ионный обмен и др.
Лит.: Дамаскин Б. Б., Петрий О. А., Введение в электрохимическую кинетику, 2 изд., М., 1983; Comprehensive treatise of electrochemistry, ed. by J.O'M. Bockris, B.E. Conway and E. Yeager, v. I, N. Y.-L, 1980.
Б. Б. Дамаскин
Значения в других словарях
- ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ — Совокупность электрич. зарядов противоположных знаков, распределённых вдоль границы соприкосновения двух фаз. В образовании Д. э. с. могут принимать участие эл-ны, ионы и ориентированные полярные (обладающие собств. дипольным моментом) молекулы. Так... Физический энциклопедический словарь
- Двойной электрический слой — Два весьма близких друг к другу слоя электрических зарядов разного знака, но с одинаковой поверхностной плотностью, возникающие на границе раздела двух фаз. Д. э. с. в целом электронейтрален. При пересечении Д. э. Большая советская энциклопедия
- ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ — ДВОЙНОЙ ЭЛЕКТРИЧЕСКИЙ СЛОЙ — образован двумя близкими друг к другу слоями электрических зарядов противоположного знака, но одинаковой поверхностной плотности. Возникает на границе раздела двух фаз. Большой энциклопедический словарь
