вольтамперометрия
ВОЛЬТАМПЕРОМЕТРИЯ
совокупность электрохим. методов исследования и анализа, основанных на изучении зависимости силы тока в электролитич. ячейке от потенциала погруженного в анализируемый раствор индикаторного микроэлектрода, на котором реагирует исследуемое электрохимически активное (электроактивное) вещество. В ячейку помещают помимо индикаторного вспомогат. электрод со значительно большей поверхностью, чтобы при прохождении тока его потенциал практически не менялся (неполяризующийся электрод). Разность потенциалов индикаторного и вспомогат. электродов Е описывается уравнением Е = U — IR, где U — поляризующее напряжение, R-сопротивление раствора. В анализируемый раствор вводят в большой концентрации индифферентный электролит (фон), чтобы, во-первых, уменьшить величину R и, во-вторых, исключить миграционный ток, вызываемый действием электрич. поля на электроактивные вещества (устар. — деполяризаторы). При низких концентрациях этих веществ омическое падение напряжения IR в растворе очень мало. Для полной компенсации омического падения напряжения применяют потенциостатирование и трехэлектродные ячейки, содержащие дополнительно электрод сравнения. В этих условиях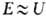
В качестве индикаторных микроэлектродов используют стационарные и вращающиеся — из металла (ртуть, серебро, золото, платина), углеродных материалов (напр., графит), а также капающие электроды (из ртути, амальгам, галлия). Последние представляют собой капилляры, из которых по каплям вытекает жидкий металл. В. с использованием капающих электродов, потенциал которых меняется медленно и линейно, наз. полярографией (метод предложен Я. Гейровским в 1922). Электродами сравнения служат обычно электроды второго рода, напр. каломельный или хлоросеребряный (см. электроды сравнения). Кривые зависимости I =f(E) или I =f(U) (вольтамперограммы) регистрируют спец. приборами — полярографами разных конструкций.
Вольтамперограммы, полученные с помощью вращающегося или капающего электрода при монотонном изменении (линейной развертке) напряжения, имеют вид, схематически представленный на рисунке. Участок увеличения тока наз. волной. Волны м. б. анодными, если электроактивное вещество окисляется, или катодными, если оно восстанавливается. Когда в растворе присутствуют окисленная (Ох) и восстановленная (Red) формы вещества, достаточно быстро (обратимо) реагирующие на микроэлектроде, на вольтамперограмме наблюдается непрерывная катодно-анодная волна, пересекающая ось абсцисс при потенциале, соответствующем окислительно-восстановит. потенциалу системы Ox/Red в данной среде. Если электрохим. реакция на микроэлектроде медленная (необратимая), на вольтамперограмме наблюдаются анодная волна окисления восстановленной формы вещества и катодная волна восстановления окисленной формы (при более отрицат. потенциале). Образование площадки предельного тока на вольтамперограмме связано либо с ограниченной скоростью массопереноса электроактивного вещества к поверхности электрода путем конвективной диффузии (предельный диффузионный ток, Id), либо с ограниченной скоростью образования электроактивного вещества из определяемого компонента в растворе. Такой ток наз. предельным кинетическим, а его сила пропорциональна концентрации этого компонента.
Форма волны для обратимой электрохим. реакции описывается уравнением:
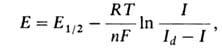
где R — газовая постоянная, Т — абс. температура, E1/2-потенциал полуволны, т. е. потенциал, соответствующий половине высоты волны (Id/2; см. рис.). Значение E1/2 характерно для данного электроактивного вещества и используется для его идентификации. Когда электрохим. реакции предшествует адсорбция определяемого вещества на поверхности электрода, на вольтамперограммах наблюдаются не волны, а пики, что связано с экстремальной зависимостью адсорбции от потенциала электрода. На вольтамперограммах, зарегистрированных при линейном изменении (развертке) потенциала со стационарным электродом или на одной капле капающего электрода (устар. — осциллографич. полярограмме), также наблюдаются пики, нисходящая ветвь которых определяется обеднением приэлектродного слоя раствора электроактивным веществом. Высота пика при этом пропорциональна концентрации электроактивного вещества. В полярографии предельный диффузионный ток (в мкА), усредненный по времени жизни капли, описывается уравнением Ильковича:
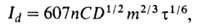
где n-число электронов, участвующих в электрохим. реакции, С-концентрация электроактивного вещества (мМ), D-eгo коэф. диффузии (см2/с), 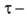 время жизни ртутной капли (с), m-скорость вытекания ртути (мг/с).
время жизни ртутной капли (с), m-скорость вытекания ртути (мг/с).
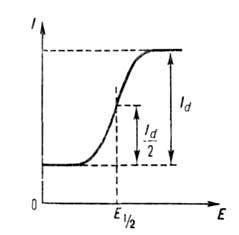
Вольтамперограмма, получаемая с помощью вращающегося дискового электрода.
В В. с вращающимся дисковым электродом предельный диффузионный ток рассчитывают по уравнению:
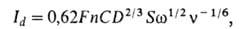
где S — площадь поверхности электрода (см2), 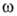 -круговая частота вращения электрода (рад/с), v-кинематич. вязкость раствора (см2/с), F-число Фарадея (Кл/моль).
-круговая частота вращения электрода (рад/с), v-кинематич. вязкость раствора (см2/с), F-число Фарадея (Кл/моль).
Циклич. В. (В. с относительно быстрой треугольной разверткой потенциала) позволяет изучать кинетику и механизм электродных процессов путем наблюдения на экране осциллографич. трубки с послесвечением одновременно вольтамперограмм с анодной и катодной разверткой потенциала, отражающих, в частности, и электрохим. реакции продуктов электролиза.
Ниж. граница определяемых концентраций Cн в методах В. с линейной разверткой потенциала составляет 10−5–10−6 М. Для ее снижения до 10−7–10−8 М используют усовершенствованные инструментальные варианты — переменно-токовую и дифференциальную импульсную В.
В первом из этих вариантов на постоянную составляющую напряжения поляризации налагают переменную составляющую небольшой амплитуды синусоидальной, прямоугольной (квадратноволновая В.), трапециевидной или треугольной формы с частотой обычно в интервале 20–225 Гц. Во втором варианте на постоянную составляющую напряжения поляризации налагают импульсы напряжения одинаковой величины (2–100 мВ) длительностью 4–80 мс с частотой, равной частоте капания ртутного капающего электрода, или с частотой 0,3–1,0 Гц при использовании стационарных электродов. В обоих вариантах регистрируют зависимость от U или Е переменной составляющей тока с фазовой или временной селекцией. Вольтамперограммы при этом имеют вид первой производной обычной вольтамперометрич. волны. Высота пика на них пропорциональна концентрации электроактивного вещества, а потенциал пика служит для идентификации этого вещества по справочным данным.
Пики разл. электроактивных веществ, как правило, лучше разрешаются, чем соответствующие вольтамперометрич. волны, причем высота пика в случае необратимой электрохим. реакции в 5–20 раз меньше высоты пика в случае обратимой реакции, что также обусловливает повыш. разрешающую способность этих вариантов В. Например, необратимо восстанавливающийся кислород практически не мешает определению мн. электроактивных веществ методом переменно-токовой В. Пики на переменно-токовых вольтамперограммах отражают не только электрохим. реакции электроактивных веществ, но и процессы адсорбции — десорбции неэлектроактивных веществ на поверхности электрода (пики нефарадеевского адмиттанса, устар. — тенсамметрич. пики).
Для всех вариантов В. используют способ снижения Cн, основанный на предварительном электрохим., адсорбц. или хим. накоплении определяемого компонента раствора на поверхности или в объеме стационарного микроэлектрода, с последующей регистрацией вольтамперограммы, отражающей электрохим. реакцию продукта накопления. Эту разновидность В. наз. инверсионной (устар. название инверсионной В. с накоплением на стационарном ртутном микроэлектроде — амальгамная полярография с накоплением). В инверсионной В. с предварит. накоплением Cн достигает 10−9–10−11 М. Миним. значения Cн получают, используя тонкопленочные ртутные индикаторные электроды, в т. ч. ртутно-графитовые, состоящие из мельчайших капелек ртути, электролитически выделенных на подложку из специально обработанного графита.
Для фазового и элементного анализа твердых тел используют инверсионную В. с электроактивными угольными электродами (т. наз. минерально-угольными пастовыми электродами). Их готовят из смеси угольного порошка, исследуемого порошкообразного вещества и инертного связующего, напр. вазелинового масла. Разработан вариант этого метода, который дает возможность проводить анализ и определять толщину металлич. покрытий. В этом случае используют спец. устройство (прижимная ячейка), позволяющее регистрировать вольтамперограмму, пользуясь каплей фонового электролита, нанесенного на исследуемую поверхность.
В. применяют: для количеств. анализа неорг. и орг. веществ в очень широком интервале содержаний — от 10−10 % до десятков %; для исследования кинетики и механизма электродных процессов, включая стадию переноса электрона, предшествующие и последующие хим. реакции, адсорбцию исходных продуктов и продуктов электрохим. реакций и т. п.; для изучения строения двойного электрич. слоя, равновесия комплексообразования в растворе, образования и диссоциации интерметаллич. соединений в ртути и на поверхности твердых электродов; для выбора условий ампераметрического титрования и др.
Лит.: Гейровский Я., КутаЯ., Основы полярографии, пер. с чеш., М., 1965; Га л юс 3., Теоретические основы электрохимического анализа, пер. с польск., М., 1974; Каплан Б. Я., Импульсная полярография, М., 1978; Брайнина Х. 3., Нейман Е. Я., Твердофазные реакции в электроаналитической химии, М., 1982; Каплан Б. Я., Пац Р. Г., Салихджанова Р. М.-Ф., Вольтамперометрия переменного тока, М., 1985.
Б. Я. Каплан, О. А. Сангина
Значения в других словарях
- вольтамперометрия — орф. вольтамперометрия, -и Орфографический словарь Лопатина
- ВОЛЬТАМПЕРОМЕТРИЯ — ВОЛЬТАМПЕРОМЕТРИЯ — совокупность электрохимических методов количественного и качественного анализа, основана на определении зависимости между силой тока и напряжением поляризации при электролизе раствора или расплава изучаемого вещества. Большой энциклопедический словарь
