Мицунобу реакция
МИЦУНОБУ РЕАКЦИЯ
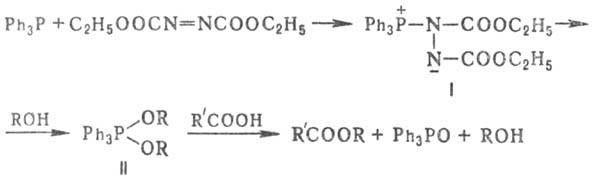
межмол. дегидратация с участием спиртов и кислотных компонентов под действием реагента Мицунобу-диэтилового эфира азодикарбоновой кислоты (ДЭАД) и трифенилфосфина:
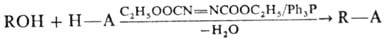
Кислотные компоненты — карбоновые кислоты, их имиды и N-гидроксиимиды, фенолы, оксимы, моно- и диэфиры фосфорной кислоты, соед. с активир. метиленовой группой. Реакцию обычно проводят при температуре ≤ 20 °C, добавляя ДЭАД к смеси спирта, кислотного компонента и Ph3P в безводном апротонном растворителе (эфир, ТГФ, гексаметапол).
Незатрудненные спирты реагируют по механизму SN2 с обращением конфигурации, напр.:
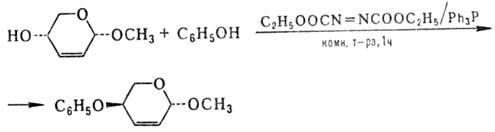
В реакции спиртов с карбоновыми кислотами образуются сложные эфиры с выходами 35–90%; в случае диолов осн. продукт-моноэфиры, причем этерификация проходит пре-им. по первичной группе ОН; выходы простых эфиров фенолов достигают 90–95%; циклич. имиды образуют с выходами 60–90% продукты N-алкилирования, напр.:
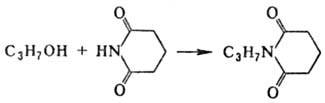
Ациклич. имиды дают продукты N- и О-алкилирования. Соед. с активир. группами CH2 вступают в М.р. с образованием продуктов С- или О-алкилирования, напр.:
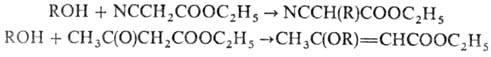
М. р. протекает обычно через стадию образования из Ph3P и ДЭАД бетаина (формула I), который при реакции со спиртом превращ. в фосфоран (II). Последний, взаимодействуя с кислотным компонентом, дает продукт реакции и трифенил-фосфиноксид, напр.:
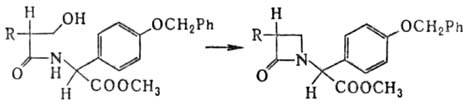
При наличии в соед. достаточно подвижного атома водорода при благоприятном взаимном структурном расположении может происходить внутримолекулярная дегидратация; напр., из гидроксикислот м. б. получены лактоны, из соед. с пептидной группой-лактамы:
Модификация М.р. — превращ. спиртов в соответствующие галогениды (F, Cl, Br, I) или цианиды под действием реагента Мицунобу и галогенида (цианида) Li; выход 50–95%.
Благодаря мягким условиям реакции, М.р. применяют в синтезе и превращениях прир. соед. (нуклеозидов, углеводов, стероидов, макроциклов), аминов и аминокислот определенной структуры, для обращения конфигурации исходного спирта.
Реакция предложена О. Мицунобу в 1967.
Лит.: Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 74–75; Mitsunobu О., "Synthesis", 1981, № 1, р. 1–28; Grochwski E. [а.о.], "J. Amer. Chem. Soc.", 1982, v. 104, № 24, p. 6876–77; Marx K.-H. [a.o.], "Lieb. Ann.", 1984, № 3, S. 476–82; Manna S., Flack J. R., Mioskowski Ch., "Synthetic Communs", 1985, v. 15, № 8, p. 663–68.
К. В. Вацуро
