Триптофан
Триптофа́н
Β-(β-индолил)-α-аминопропионовая кислота, одна из важнейших природных аминокислот (См. Аминокислоты).
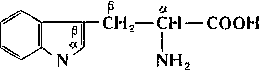
Существует в виде оптически активных L- и D- и рацемической DL-формы. В небольших количествах L-T. входит в состав гаммаглобулинов (См. Гамма-глобулины), Фибриногена, Казеина и др. белков.
L-T. — незаменимая аминокислота; суточная потребность взрослого человека в ней составляет 0,25 г, детей до 7 лет — около 1 г. Биосинтез Т. у микроорганизмов и растений осуществляется конденсацией аминокислоты Серина с Индолом, катализируемой ферментом триптофансинтазой. (Биосинтез Т. у кишечной палочки использовали для доказательства коллинеарности Гена и кодируемой им полипептидной цепи, когда положение каждой аминокислоты в полипептидной цепи определяется особым участком гена.) В организмах различных животных L-T. подвергается сложным превращениям, образуя ряд жизненно важных соединений: из продуктов распада L-T. у млекопитающих и человека образуются Никотиновая кислота и Серотонин; у насекомых — пигменты глаз (оммохромы), у растений — Гетероауксин, Индиго, ряд алкалоидов и др. При гнилостных процессах в кишечнике из Т. образуются Скатол и индол. При нормальном распаде в организме 6 из 11 атомов углерода Т. включаются в Трикарбоновых кислот цикл через ацетил- и ацетоацетилкофермент А: остальные 5 — превращаются в CO2. Врождённое отсутствие у человека окисляющего Т. фермента — триптофан-пирролазы приводит к слабоумию. Нарушения обмена Т. у человека могут служить показателями ряда тяжёлых заболеваний (туберкулёз, рак, диабет). Причиной функциональных и органических расстройств у человека и животных может быть также дефицит Т. в пище и кормах, связанный с недостаточным содержанием его во многих природных белках. Пищевая ценность многих белков можно повысить добавкой синтетического Т., получаемого химическим синтезом из акрилонитрила, аммиака, цианистого водорода и фенилгидразина. Разрабатываются методы ферментативного синтеза Т. из индола, пировиноградной кислоты и аммиака.
Лит.: Браунштейн А. Е., Биохимия аминокислотного обмена, М., 1949; Майстер А., Биохимия аминокислот, пер. с англ., М., 1961; Ленинджер А., Биохимия, пер. с англ., М., 1974; Сафонова Э. Н., Беликов В. М., Успехи в области синтеза и производства α-аминокислот, «Успехи химии», 1974, т. 43, в. 9.
Э. Н. Сафонова.
Значения в других словарях
- триптофан — орф. триптофан, -а Орфографический словарь Лопатина
- триптофан — ТРИПТОФАН [2-амино-3-(3-индолил)пропионовая кислота, β-(3-индолил)-α-аминопропионовая кислота, β-3-индолилаланин, Trp, W] мол. м. 204,22; бесцветные кристаллы; т. пл. D,L-T. 283–285 °C; для D-T. т. пл. (концентрация 1 г в 100 мл воды), для L-T. Химическая энциклопедия
- триптофан — Незаменимая аминокислота. В небольших кол-вах содержится во мн. природных белках. Участвует в образовании никотиновой к-ты и серотонина (у млекопитающих, в т. Биологический энциклопедический словарь
- ТРИПТОФАН — ТРИПТОФАН (аминокислота, C13H10O2N2). Впервые выделена в 1902 г. Необходима для синтеза никотиновой кислоты (витамина РР). Животные не могут синтезировать триптофан, поэтому необходимое количество его должно быть получено с пищей. Научно-технический словарь
- Триптофан — Незаменимая в питании человека моноаминомонокарбоновая гетероциклическая аминокислота; входит в состав многих белков (например, глобулинов сыворотки крови, казеина) и участвует в процессе биосинтеза никотиновой кислоты и серотонина. Медицинская энциклопедия
- триптофан — ТРИПТОФАН -а; м. Одна из аминокислот, входящая в состав гамма-глобулина, казеина и других белков. Добавки триптофана к белкам. Толковый словарь Кузнецова
- ТРИПТОФАН — ТРИПТОФАН — гетероциклическая аминокислота. Входит в состав гамма-глобулинов, казеина и других белков. Используется клетками млекопитающих для биосинтеза никотиновой кислоты (витамин РР) и серотонина, насекомыми — пигмента глаз... Большой энциклопедический словарь
