Лёгочное сердце
Легочное сердце (cor pulmonale) — патологическое состояние, характеризующееся гиперфункцией миокарда правых отделов сердца вследствие легочной артериальной гипертензии, обусловленной патологией бронхолегочного аппарата, сосудов легких или торако-диафрагмальными нарушениями; проявляется признаками повышения работы правого желудочка сердца, его гипертрофией и (или) дилатацией, постепенным или быстрым формированием правожелудочковой сердечной недостаточности. Данное определение отражает современную тенденцию, направленную на раннюю клиническую диагностику легочного сердца на стадии уже обнаруживаемой гиперфункции правого желудочка, но еще до появления достоверных клинических признаков увеличения его массы или расширения полости, т.е. тех последствий гиперфункции, которые являются единственными критериями морфологического диагноза и положены в основу определения Л. с., предложенного Комитетом экспертов ВОЗ (1961). К легочному сердцу не относят гипертрофию и дилатацию правого желудочка при поражениях легких и легочной гипертензии, являющихся вторичными по отношению к первичной патологии левых отделов сердца или врожденным порокам сердца и крупных сосудов.
Патологические изменения сердца при хронических заболеваниях легких были описаны французским врачом Лаэннеком (R. Th. Н. Laennec) в 1819 г. и привлекали внимание клиницистов разных стран. Из отечественных ученых в 19 в. проблему Л.с. изучали Г.И. Сокольский (1838), Э.И. Изаксон (1870), С.П. Боткин (1886), а в 20 в. крупным вкладом в учение о Л.с. стали труды Б.Е. Вотчала, определившие современные подходы к классификации, патогенезу, ранней диагностике и принципам лечения легочного сердца. Термин «легочное сердце» в СССР стал широко использоваться с 60-х гг. 20 в., вытеснив понятие «легочно-сердечная недостаточность», которое относится лишь к декомпенсированному Л.с., но до сих пор иногда применяется как синоним термина «легочное сердце», что принципиально неверно. По замечанию Б.Е. Вотчала (1964), ограничить понятие только стадией недостаточности кровообращения — значит опоздать с диагностикой изменений сердца, лежащих в основе этой недостаточности.
Во второй половине 20 в. доля Л.с. в структуре всех органических поражений сердца в развитых странах значительно возросла в связи с нарастанием частоты хронических неспецифических заболеваний легких. Если в 20—30-е гг. она составляла не более 1%, то в 50—60-х гг. этот показатель увеличился, по разным данным, до 6—9%, причем у больных с сердечной недостаточностью Л.с. как ее причина обнаруживалось в 30% случаев, т.е. примерно с такой же частотой, как клапанные пороки сердца, и лишь несколько реже, чем ишемическая болезнь сердца и гипертоническая болезнь вместе взятые. При хронических заболеваниях бронхолегочного аппарата и поражении сосудов легких Л.с. наряду с дыхательной недостаточностью относится к основным причинам инвалидизации и смерти больных.
Классификация. В зависимости от причин легочной артериальной гипертензии выделяют следующие формы Л.с.: васкулярную (вследствие поражения легочных сосудов), бронхолегочную (при бронхиальной обструкции и поражениях паренхимы легких) и торакодиафрагмальную.
Различают острое Л.с. (возникает за несколько часов или дней), подострое Л.с. (развивается за недели, месяцы) и хроническое Л.с. (обычно осложняет многолетнее течение болезней органов дыхания с длительным существованием дыхательной недостаточности).
В зависимости от нарушений сердечной деятельности традиционно выделяют стадию компенсированного Л.с. (проявляется только гипертрофией правого желудочка) и стадию декомпенсации Л.с. (определяется со времени появления признаков правожелудочковой сердечной недостаточности). Для хронического Л.с., ранняя диагностика которого особенно актуальна, предлагают различать три стадии. I стадия характеризуется преходящей легочной артериальной гипертензией (см. Гипертензия малого круга кровообращения) и признаками напряженной деятельности правого желудочка, которые выявляются только инструментальными методами. Для II стадии характерны признаки гипертрофии правого желудочка сердца обычно на фоне устойчивой легочной артериальной гипертензии. Ill стадия соответствует декомпенсации Л.с. — правожелудочковой сердечной недостаточности, которая всегда сочетается со стабильной дыхательной недостаточностью, что в определенной мере оправдывает использование для характеристики данной стадии Л.с. термина «легочно-сердечная недостаточность».
Этиология. Острое Л.с. чаще всего бывает васкулярным, в подавляющем большинстве случаев причиной его развития является тромбоэмболия легочного ствола, его главных ветвей или крупных легочных артерий. К значительно более редким и потому менее известным практическим врачам причинам острого Л.с. (что приводит к несвоевременной его диагностике) относятся вентильный пневмоторакс, пневмомедиастинум, астматический статус, распространенная массивная острая пневмония со значительным цианозом, газовая или жировая эмболия легочных артерий.
Подострое Л.с. также чаще бывает васкулярным, но возможны варианты подострого развития бронхолегочного и торакодиафрагмального Л.с. Оно развивается при повторных мелких тромбоэмболиях легочных артерий, системных васкулитах с поражением сосудов легких, при первичной легочной артериальной гипертензии, диффузном бронхиолите, тяжелом течении бронхиальной астмы, лимфогенном карциноматозе легких, быстро прогрессирующем течении фиброзирующего альвеолита (синдром Хаммена — Рича), массивных плевральных выпотах (при мезотелиоме плевры).
Хроническое Л.с. развивается на фоне медленно прогрессирующей дыхательной недостаточности при хронических бронхолегочных заболеваниях и как торакодиафрагмальная форма при резко выраженном кифозе, кифосколиозе, массивном фибротораксе, пикквикском синдроме. Самыми частыми причинами хронического Л.с. (в 80—90% случаев) являются хронические неспецифические заболевания легких, особенно сопровождающиеся выраженными нарушениями бронхиальной проходимости (прежде всего хронический обструктивный бронхит и бронхиальная астма). К относительно редким причинам хронического Л.с. относятся хроническая Горная болезнь, нарушения дыхания в связи с поражением дыхательных мышц или их нервного аппарата (например, при полиомиелите, миастении).
Патогенез. Гиперфункция правого желудочка, приводящая к его гипертрофии, во всех случаях Л.с. обусловлена легочной артериальной гипертензией, а на начальных этапах формирования Л.с. она частично связана также с рефлекторным повышением сердечного выброса в ответ на повышение работы дыхания и развивающуюся при дыхательной недостаточности гипоксию тканей. Последняя играет существенную патогенетическую роль в развитии дистрофии миокарда (усугубляет его дистрофию от гиперфункции), с которой связаны дилатация правого желудочка сердца и формирование декомпенсации Л.с. Обоснование патогенетической терапии Л.с. зависит от понимания природы гипоксии и, особенно артериальной гипертензии в малом круге кровообращения, всегда обусловленной при Л.с. повышением сопротивления кровотоку в сосудах легких, но патогенез этого повышения при отдельных формах Л.с. неодинаков.
При васкулярной форме, т.е. в большинстве случаев острого и подострого Л.с., сопротивление кровотоку в артериях малого круга кровообращения возрастает преимущественно за счет органического сужения общего просвета легочных сосудов вследствие закупорки их эмболами (например, при тромбоэмболии), опухолевой или воспалительной инфильтрации стенок, облитерации их просвета (при системных васкулитах). Лишь в начальных стадиях развития первичной легочной артериальной гипертензии, а также при горной болезни ведущее значение имеет функциональная гипертония сосудов легких, которая впоследствии дополняется органическим сужением артерий за счет гипертрофии и склероза их стенок, развития атеросклероза в крупных легочных артериях и легочном стволе. В первые часы после тромбоэмболии легочных артерий функциональный компонент (генерализованная гипертоническая реакция легочных артерий) дополняет органическое сужение сосудистого русла, что выражается особенно высокой в эти часы легочной артериальной гипертензией, быстро приводящей к перенапряжению правого желудочка, его дилатации и нередко декомпенсации.
При бронхолегочной и торакодиафрагмальной формах Л.с. органическое сужение просвета легочных сосудов также может играть определенную патогенетическую роль. Оно возможно за счет облитерации, микротромбоза и сдавления сосудов в зонах воспаления, склеротического или опухолевого процессов в легких, а при заболеваниях, протекающих с рестриктивной дыхательной недостаточностью (легочных фиброзах, пикквикском синдроме), также вследствие снижения, способности легких к растяжению и спадения сосудов в фиброзированных нерастяжимых сегментах легких. Однако в большинстве случаев при этих формах Л.с. ведущее значение имеют функциональные механизмы формирования легочной артериальной гипертензии, связанные с нарушениями механики дыхания, вентиляции альвеол и гипоксией. Наиболее полно они представлены в патогенезе хронического легочного сердца при бронхообструктивных поражениях легких. К основным из этих механизмов относятся следующие.
1. Повышение внутригрудного, в т.ч. внутриальвеолярного, давления на выдохе, пропорциональное степени бронхиальной обструкции как по величине, так и по длительности действия за счет удлинения выдоха (если продолжительность выдоха увеличивается в 3 и более раз по сравнению с продолжительностью вдоха, то повышенное внутригрудное давление действует 16 и более часов в сутки). Создаваемая в результате прироста давления компрессия внутригрудных образований неодинаково действует на кровь в крупных артериях (тем более в камерах сердца) и в тонкостенных капиллярах легкого, которые сдавливаются легче. Т.к. последние имеют, кроме того, большую площадь, а работа давления пропорциональна площадям, то в системе малого круга кровообращения создается подобие гидравлического пресса: чтобы преодолеть силу, сдавливающую легочные капилляры, правый желудочек должен поднять давление в легочном стволе не на величину этой силы, а на значительно большую величину, что достигается повышением внутрижелудочкового давления, требующим дополнительных энергетических затрат.
2. Рефлекторное сужение легочных артерий в ответ на снижение рО2 в альвеолярном газе (рефлекс Эйлера — Лильестранда). При бронхиальной обструкции с характерной для нее вентиляционной недостаточностью (см. Дыхательная недостаточность) оно играет ведущую роль в повышении сопротивления кровотоку, что требует усиленной работы правого желудочка на преодоление сопротивления кровотоку путем повышения давления в желудочке и легочном стволе. Этот механизм не связан с фазами дыхания, его роль в существенной мере зависит от степени неравномерности вентиляции альвеол, определяющей число невентилируемых участков легких с выключенным кровотоком.
3. Повышение сердечного выброса, возникающее в ответ на гипоксию при любом типе дыхательной недостаточности, а при бронхиальной обструкции обусловленное прежде всего значительным повышением работы дыхательных мышц, на обеспечение которой при тяжелых степенях обструкции (например, при астматическом статусе) может расходоваться до 80% всего поглощаемого кислорода. Т.к. повышение внутригрудного давления препятствует венозному притоку крови в правый желудочек (этим объясняется феномен «капельного» сердца при выраженной эмфиземе легких), то увеличение сердечного выброса при значительной бронхиальной обструкции достигается возрастанием в основном не ударного объема, а частоты сердечных сокращений.
4. Рост сопротивления кровотоку за счет повышения вязкости крови вследствие компенсаторного эритроцитоза при гипоксии; этот механизм участвует в формировании легочной артериальной гипертензии при любом типе дыхательной недостаточности, проявляющейся выраженным цианозом.
Каждый из перечисленных механизмов развития легочной артериальной гипертензии имеет свои особенности патогенеза, связанные с конкретной формой патологии органов дыхания. В частности, при поражениях легочной паренхимы развитие и выраженность сосудистых реакций в малом круге кровообращения зависят от нарушения продукции и нейтрализации в легких различных вазоактивных субстанций (гепарина, кининов, простагландинов и др.).
Раннее развитие дистрофии миокарда правого желудочка (Являющейся непременной составной частью патогенеза Л.с.) определяется тем, что гиперфункция правого желудочка осуществляется в патологических условиях энергообеспечения работы сердца. Кроме дефицита кислорода, обусловленного дыхательной недостаточностью, имеет значение также снижение в мышце правого желудочка нутритивного кровотока в связи с укорочением диастолы, сопутствующим тахикардии, и повышением внутрижелудочкового давления. Последнее затрудняет отток крови из тебезиевых вен, через которые в норме в полость правого желудочка изливается около 40% коронарной крови, орошающей желудочек. У ряда больных развитие дистрофии миокарда в существенной мере связано с интоксикацией из очагов хронической инфекции в дыхательных путях или паренхиме легких; имеются данные об участии в развитии дистрофии также аутоиммунных процессов.
Патологическая анатомия. При подостром и хроническом Л.с. увеличивается масса миокарда правого желудочка сердца (развивается гипертрофия) и в той или иной степени возрастает объем правых отделов органа. Степень гипертрофии определяют при помощи раздельного взвешивания сердца или по увеличению толщины стенки правого желудочка у его основания (в норме она составляет примерно 3,3—4,9 мм). Диагностическая ценность последнего показателя снижается по мере дилатации правого желудочка, сопровождающейся истончением его стенки. Изменение в сторону преобладания массы миокарда правого желудочка (в норме отношение массы правого желудочка к массе левого составляет 1: 2) дает основание для установления диагноза Л.с. только в случаях, когда определяется патология органов дыхания или сосудов легких и отсутствуют первичные заболевания сердца, приводящие к гипертрофии правого желудочка. Острое Л.с. характеризуется резким расширением правого желудочка и истонченном стенки; гипертрофия развиться не успевает. Миокард правого желудочка при остромЛ.с, дряблый, с выраженным глинистым оттенком; микроскопически выявляются жировая дистрофия, фрагментация мышечных волокон, отек интерстиция, контрактурные изменения кардиомиоцитов, диапедезные кровоизлияния. В большом круге кровообращения определяется острое застойное полнокровие органов.
Хроническое Л.с. может иметь различные анатомические характеристики в зависимости от особенностей основного заболевания, наличия и степени компенсаторных возможностей миокарда (компенсированное Л.с. или в стадии декомпенсации). В одних случаях (чаще при необструктивных формах патологии легких) выявляются гипертрофия трабекулярного аппарата и расширение желудочка при некотором утолщении стенки, удлинение вначале приносящего, а позже и выносящего тракта, что в совокупности характерно для перегрузки правого желудочка как давлением, так и объемом. Такой тип гипертрофии определяется, например, при первичной легочной артериальной гипертензии (рис. 1). В других случаях преобладают признаки перегрузки желудочка давлением: гипертрофия самой стенки, иногда резко выраженная, при умеренной гипертрофии трабекулярного аппарата. Толщина стенки правого желудочка может превосходить толщину стенки левого. Верхушка сердца формируется за счет миокарда правого желудочка, а не левого, как в норме.
В стадии компенсации хронического Л.с. мышца правого желудочка упругая, розового цвета; форма желудочка сохранена. При декомпенсированном Л.с. мышца дряблая, желтоватого цвета, форма желудочка изменена; отмечаются признаки хронического застойного полнокровия в органах. Микроскопически при хроническом Л.с. определяются гипертрофия мышечных волокон, огрубение стромы, утолщение эндокарда, дистрофические изменения кардиомиоцитов, нарастающие в период декомпенсации легочного сердца.
Клинические проявления. Признаки острого Л.с. при тромбоэмболии легочных артерий сочетаются с другими ее симптомами, прежде всего тахипноэ (до 30—40 и более дыханий в 1 мин), падением АД вплоть до Коллапса, нарастающим «пепельным» диффузным Цианозом, которые в большинстве случаев появляются в первые минуты после возникновения у больного внезапной боли в груди, ощущения нехватки воздуха либо обморока или других вариантов начальных проявлений тромбоэмболии (см. Тромбоэмболия легочных артерий (Тромбоэмболия лёгочных артерий)). В зависимости от калибра пораженного сосуда выраженность проявлений острого Л.с. колеблется от обнаруживаемых преимущественно только по изменениям ЭКГ до многосимптомной клинической картины, включающей острое развитие правожелудочковой сердечной недостаточности (если в ближайшие минуты не наступает смерть от асистолии или фибрилляции желудочков сердца). Характерны расширение границ относительной и абсолютной тупости сердца, тахикардия, резкое усиление и акцент II тона над легочным стволом (иногда его расщепление), раздвоение I тона сердца; могут выслушиваться Галопа ритм, маятникообразный ритм (систола и диастола по длительности не различимы). Возможна Экстрасистолия; в редких случаях развивается Мерцательная аритмия. При прогрессирующей недостаточности правого желудочка повышается венозное давление, набухают шейные вены, появляется акроцианоз, увеличивается печень, при этом из-за быстрого растяжения ее капсулы нередко возникают сильные боли в правом подреберье, которые иногда дают основание подозревать острый живот. Аналогично проявляется острое Л.с. при клапанном пневмотораксе и астматическом статусе, но правожелудочковая недостаточность при этом развивается медленнее, чаще отмечается экстрасистолия, АД имеет тенденцию к повышению.
Подострое Л.с. проявляется в основном так же, как хроническое Л.с., но для него характерно более раннее появление симптомов гипертрофии, а затем и декомпенсации правого желудочка на фоне значительно более выраженной легочной артериальной гипертензии. В отличие от большинства случаев хронического Л.с. при подостром Л.с., особенно васкулярном, признаки расширения полости правого желудочка сердца отмечаются на самых ранних стадиях развития, но на этих стадиях оно связано, в основном, с тоногенной, а не миогенной дилатацией, как при остром легочном сердце.
Хроническое Л.с. развивается исподволь, и длительное время его клинические признаки не выделяются на фоне преобладающих проявлений основного заболевания и трудно отличимы от симптомов дыхательной недостаточности. Среди жалоб больных к относительно ранним проявлениям хронического Л.с. могут быть отнесены ощущение сердцебиений в виде повышенной частоты ударов сердца и появление утомляемости при физических нагрузках, которые при той же степени дыхательной недостаточности больной раньше переносил удовлетворительно. Поздними жалобами являются сердцебиение с ощущением силы ударов, а также боли в груди, особенно приступы загрудинных болей, напоминающие стенокардию, — так называемая легочная грудная жаба, или стенокардия Кача. Последнюю связывают с перерастяжением стенок легочного ствола (аналогично происхождению аорталгии), т.к. она наблюдается только при высоких степенях легочной артериальной гипертензии. Однако в ряде случаев не исключены истинные приступы стенокардии (Стенокардия), проявления которой могут иметь особенности в связи с ишемией миокарда не левого, а правого желудочка. К наиболее поздним относятся жалобы больных, соответствующие периоду декомпенсации Л.с. Значительно снижается переносимость физических нагрузок, ухудшается аппетит, больные ощущают тяжесть либо растирание, иногда болезненность в правом подреберье (или в эпигастральной области), которые вначале появляются во время или сразу после нагрузки, затем также после еды, а в последующем ощущаются постоянно; появлению периферических отеков предшествует Никтурия — больные отмечают снижение дневного диуреза при увеличении мочеотделения ночью.
К самым ранним из выявляемых врачебным исследованием объективных симптомов хронического Л.с. относится тахикардия на фоне аускультативных признаков гипертензии малого круга кровообращения и напряженной деятельности правого желудочка сердца. Отмечаются усиление и акцент II тона сердца над легочным стволом (если его выслушиванию не препятствует оттеснение сердца от грудной стенки при выраженной эмфиземе легких) и нередко повышение громкости, иногда расщепление I тона сердца над мечевидным отростком или нижней частью грудины.
Развитие гипертрофии правого желудочка вначале определяется только инструментальными методами, но постепенно формируются ее клинические признаки, которые на поздних стадиях дополняются симптомами дилатации правого желудочка и его недостаточности. Нередко, особенно при развитии хронического Л.с, у детей и лиц молодого возраста, формируется выбухание передней грудной стенки («сердечный горб»), при осмотре и пальпации определяется сотрясение передней грудной стенки при каждом сокращении сердца — сердечный толчок (его следует отличать от усиленного верхушечного толчка, характерного для гипертрофии левого желудочка), перкуторно выявляется расширение границ абсолютной сердечной тупости. Эти симптомы могут отсутствовать при выраженной эмфиземе легких, но в таких случаях хорошо определяется, как правило, пальпаторный симптом гипертрофии и напряженной деятельности правого желудочка — его усиленная пульсация в подложечной области, ощущаемая как сильные упругие удары в подушечки пальцев, которые подводят под мечевидный отросток параллельно плоскости грудины. По мере нарастания гипертензии малого круга кровообращения и дилатации правых отделов сердца границы относительной сердечной тупости расширяются вверх и вправо от грудины (признак дилатации правого предсердия), появляются аускультивные признаки относительной трикуспидальной недостаточности — ослабление I тона сердца и систолический шум над основанием мечевидного отростка, усиливающийся на высоте вдоха. В некоторых случаях, чаще всего при первичной легочной артериальной гипертензии, во II межреберье слева от грудины выслушивается диастолический шум относительной недостаточности клапана легочного ствола (шум Грэма Стилла). Декомпенсация правого желудочка сердца проявляется патологическим повышением венозного давления, акроцианозом, набуханием шейных вен, увеличением печени, периферическими отеками.
Диагноз. Острое Л.с. распознается по характерным клиническими симптомам. Однако его следует предполагать и при недостаточно четких клинических проявлениях во всех случаях, когда имеются предпосылки к его развитию — тромбоэмболия легочных артерий, клапанный пневмоторакс, затяжной астматический статус. Диагноз на догоспитальном этапе может быть подтвержден данными срочно произведенной электрокардиографии, а в стационаре также рентгенологическим исследованием грудной клетки, которое позволяет уточнить как диагноз основного заболевания, так и признаки острой гипертензии малого круга кровообращения, а также расширение правых отделов сердца и путей оттока из правого желудочка. Электрокардиографическая диагностика острого Л.с. при тромбоэмболии легочных артерий основывается на характерных для него признаках перегрузки правых отделов сердца, наиболее типичные из которых представлены на рис. 2. В сравнении с исходной ЭКГ (до тромбоэмболии) электрическая ось сердца отклоняется вправо, переходная зона в грудных отведениях смещается влево (что соответствует повороту сердца вокруг продольной оси по часовой стрелке), часто появляются глубокие зубцы SI и QIII (так называемый синдром SIQIII); увеличивается амплитуда зубцов R (или появляются зубцы R') в отведениях aVR, V, и зубцов S в левых грудных отведениях; сегмент ST в отведении III часто смещается вверх, а в отведениях I и правых грудных — вниз от изолинии; зубец Т в III отведении может стать отрицательным; зубец Р в отведениях II и III становится высоким, иногда заостренным (так называемая Р-pulmonale), возрастает амплитуда его положительной фазы в отведении V1. При клапанном пневмотораксе и астматическом статусе на формирование изменений ЭКГ существенно влияет анатомическое смещение сердца, которое при пневмотораксе обусловлено смещением средостения, а при астматическом статусе — оттеснением сердца вниз вследствие острого вздутия легких (формируется так называемый S-тип ЭКГ).
Диагноз хронического Л.с. устанавливается при обнаружении у больного с хронической дыхательной недостаточностью признаков гипертрофии правого желудочка, а в ранних стадиях — его гиперфункции при исключении их связи с первичной патологией сердца. Наиболее затруднен ранний диагноз, обоснование которого сводится, по существу, к выявлению легочной артериальной гипертензии и связанной с ней гиперфункции правого желудочка инструментальными методами, которые применяют, в основном, в стационаре. Обычно используют косвенные методы оценки давления в легочном стволе — измерение фазы изометрического расслабления правого желудочка, скорости движения задней створки клапана легочного ствола, амплитуды систолической волны правого предсердия и др. Для этого применяют кинетокардиографию (Кинетокардиография), реографию (Реография), эхокардиографию (Эхокардиография) и другие неинвазивные методы исследования сердца. Относительно рано напряженную деятельность правых отделов сердца можно выявить с помощью векторкардиографии (Векторкардиография), особенно предсердной: повышенная нагрузка на правое предсердие проявляется отключением вправо и увеличением площади петли Р векторкардиограммы.
В условиях поликлинического обследования больного обоснование диагноза хронического Л.с. становится реальным, когда гипертрофия правого желудочка может быть обнаружена по изменениям ЭКГ или рентгенологически, либо на более поздних стадиях по характерным клиническим признакам, описанным выше. Электрокардиографическая диагностика хронического Л.с. основывается как на прямых признаках гипертрофии правого желудочка, так и на косвенных. К последним относятся, в частности, отрицательные зубцы Т в отведениях V1—V3 и изменения соотношения амплитуд зубцов R и S в грудных отведениях, отражающие, в основном, ротационные сдвиги. Начальные изменения ЭКГ характеризуются отклонением электрической оси сердца в полувертикальное, вертикальное положение или вправо, сдвигом переходной зоны влево и признаками отклонения верхушки сердца назад. По мере нарастания легочной артериальной гипертензии постепенно увеличивается амплитуда зубца Р во II и III отведениях, изменяется их конфигурация вплоть до формирования типичных Р-pulmonale. Изменения желудочковых комплексов при разных формах бронхолегочной патологии неоднородны. В зависимости от преимущественных изменений амплитуды зубцов R и S в грудных отведениях выделяют три типа изменений ЭКГ при гипертрофии правого желудочка (рис. 3): R-тип, характеризующийся высоким зубцом R в отведении V1(R > S). Без выраженного зубца S в левых грудных отведениях; RSR', проявляющийся наличием в отведении V1 зубца R'(при R ≤ S); S-тип, при котором глубокий зубец S определяется в большинстве отведений ЭКГ, включая левые грудные, а в отведениях V1—V3 желудочковый комплекс может приобретать форму QS или зубец R имеет малую амплитуду. Прямыми признаками гипертрофии при отсутствии блокады правой ножки пучка Гиса являются зубец R в отведении V1 более 7 мм или в сумме с зубцом S в отведении V1 более 10,5 мм, желудочковый комплекс формы QR в отведении V1. В большинстве случаев относительно ранняя электрокардиографическая диагностика хронического Л.с., особенно при эмфиземе легких, основывается на косвенных признаках, но высокую достоверность она приобретает при сочетании их хотя бы с одним прямым признаком гипертрофии.
Рентгенологические исследования позволяют диагностировать хроническое Л.с. и наблюдать за динамикой его развития как в стационаре, так и в поликлинике. В начальных стадиях Л.с. у больных с выраженной эмфиземой легких при рентгенографии и рентгеноскопии в прямой и косых проекциях отмечаются относительно небольшие размеры сердца, но уже можно выявить признаки гипертрофии путей оттока от правого желудочка: выбухание легочного конуса в прямой и правой косой проекциях; в выраженных случаях выступающая по левому контуру вторая дуга легочного конуса может имитировать «митральную» конфигурацию сердца; отмечается расширение легочного ствола и его крупных ветвей, которое часто сочетается с сужением более мелких разветвлений (симптом «ампутации» корня) и обеднением периферического сосудистого рисунка легких (рис. 4). Это особенно отчетливо обнаруживается на томограммах легких. В последующих стадиях развития Л.с. рентгенологически определяется прогрессирующее увеличение правого желудочка за счет гипертрофии, а затем и дилатации. При значительном расширении правого желудочка он может оттеснять левый желудочек кзади и становиться краеобразующим как по правому, так и по левому контуру сердца. При рентгенокимографии отмечаются увеличение амплитуды сокращений и расширение зон пульсации правого желудочка и легочного ствола. В стадии декомпенсации сердца тень его расширяется вправо главным образом за счет дилатации правого предсердия; на рентгенокимограммах зона пульсации правого предсердия расширена, зубцы правого желудочка деформированы, амплитуда его пульсации снижена.
Дифференциальный диагноз с гипертрофией правого желудочка при первичной патологии сердца является непременным условием диагноза Л.с. и обычно не труден. В редких случаях поздней диагностики хронического Л.с. (в стадии декомпенсации с кардиомегалией) необходимо его дифференцировать с пороками сердца, дилатационной кардиомиопатией, кардиосклерозом в исходе ишемической болезни сердца. Клинически в пользу Л.с. свидетельствует резко выраженный цианоз, т.к. декомпенсация Л.с. наступает обычно при высокой степени дыхательной недостаточности с уровнем гипоксемии, который практически никогда не наблюдается при первичной патологии сердца. Исключением являются веноартериальные шунты при врожденных дефектах перегородок сердца и патологических соустьях между аортой и легочным стволом. В этих случаях ингаляция больным 100% кислорода не приводит к уменьшению гипоксемии и цианоза, который при дыхательной недостаточности в тех же условиях резко уменьшается или исчезает. Тщательное рентгенологическое исследование и эхокардиография при всех вышеуказанных болезнях сердца позволяют выявить гипертрофию или дилатацию его левых отделов, при клапанных пороках на эхокардиограммах определяются изменения пораженных клапанов, а с помощью допплер-эхокардиографии могут быть установлены патологические потоки крови через дефекты перегородок.
При остром Л.с. трудности диагностики нередко связаны с недостаточно тщательной дифференциальной диагностикой с основным заболеванием. Так, резкая боль в груди при пневмотораксе или тромбоэмболии легочных артерий может быть расценена как стенокардия, а сочетание болей в груди с коллапсом при тромбоэмболии легочных артерий и появление на ЭКГ в III отведении глубокого зубца Q со смещением вверх сегмента ST и инверсией зубца Т часто расцениваются как проявления инфаркта миокарда задней стенки; резкие боли в животе, связанные с быстрым растяжением капсулы печени при декомпенсации острого Л.с., иногда интерпретируются как печеночные колики или симптом острого аппендицита. Все эти трудности врач должен учитывать при недостаточно типичных проявлениях тромбоэмболии легочных артерий, т.к. ее диагностика относится к ургентной, требующей немедленных действий врача. В пользу тромбоэмболии (и против стенокардии и инфаркта миокарда) свидетельствуют нетипичные для стенокардии (Стенокардия) локализация и иррадиация болей в груди, их резистентность к нитроглицерину, тахипноэ (более 50 дыханий в 1 мин), появление диффузного цианоза (синюшность языка), наличие среди изменений ЭКГ не только глубокого зубца QIII, но и глубокого SI, смещение переходной зоны влево, повышение вольтажа зубца Р во II и III отведениях. При подозрении на Острый живот необходима консультация хирурга, но при этом учитывают, во-первых, что острые боли в животе и лейкоцитоз могут быть проявлением острого легочного сердца при тромбоэмболии легочных артерий и, во-вторых, что острая патология органов брюшной полости не объясняет наличие резкой одышки, цианоза, тахикардии, изменения тонов сердца, набухания шейных вен и других симптомов, относящихся к острому легочному сердцу.
В процессе ведения больных с хроническим Л.с. раннее выявление декомпенсации правого желудочка сердца часто связано с дифференциальной диагностикой сердечной и дыхательной недостаточности, т.к. последняя, особенно при бронхиальной обструкции, проявляется рядом сходных симптомов вплоть до развития периферических отеков (вследствие гипоксии почек, надпочечников). При этом учитывают следующие основные различия: повышение венозного давления и набухание шейных вен при бронхиальной обструкции связаны с экспираторным повышением внутригрудного давления и исчезают на вдохе, в то время как при правожелудочковой недостаточности шейные вены в период вдоха не спадаются; преимущественное проявление диффузного цианоза на кистях, стопах может имитировать акроцианоз за счет сердечной недостаточности, но в отличие от последней при диффузном цианозе кисти рук остаются теплыми; опущение края печени на 2—5 см ниже края ребер за счет эмфиземы легких не сочетается с изменением ее размеров при перкуссии по Курлову, как это происходит у больных с увеличением печени вследствие недостаточности правого желудочка, при которой нередко определяется также гепатоюгулярный рефлюкс (давление на выступающий край печени ладонью приводит к набуханию шейных вея); отеки при сердечной недостаточности развиваются постепенно, им предшествует никтурия, введение строфантина приводит к увеличению диуреза, в то время как отеки, которые связывают только с дыхательной недостаточностью, появляются на фоне тяжелой гипоксии, не уменьшаются после применения сердечных гликозидов и исчезают после устранения гипоксии, например путем оксигенобаротерапии (строго говоря, это не исключает связи отеков с сердечной недостаточностью, возникающей вследствие гипоксии миокарда и исчезающей после ее устранения).
Лечение и профилактика. Больные с острым Л.с. подлежат экстренной госпитализации, т.к. эффективное лечение, предотвращающее смертельный исход, возможно только в стационаре и должно начинаться как можно раньше. На месте и в процессе транспортировки больному необходимо создать максимальный двигательный покой, по возможности обеспечить ингаляцию кислорода и оказать первую помощь по основному заболеванию (см. Бронхиальная астма, Пневмоторакс, Тромбоэмболия легочных артерий (Тромбоэмболия лёгочных артерий)), например при тромбоэмболии легочных артерий ввести гепарин. Целесообразна госпитализация больных в многопрофильную больницу, где при необходимости может быть произведено срочное оперативное вмешательство, например в случае тромбоэмболии легочного ствола или его крупных ветвей (эмболэктомия) или в связи с клапанным пневмотораксом. При астматическом статусе больных направляют в отделение реанимации или палаты интенсивной терапии пульмонологического отделения.
Лечение и вторичная профилактика подострого и хронического Л.с. совпадают в аспектах этиологической и патогенетической терапии, т.е. направленной главным образом на основное заболевание и механизмы развития легочной артериальной гипертензии. Все больные с подострым и хроническим Л.с. подлежат диспансеризации по основному заболеванию и должны постоянно наблюдаться участковым терапевтом, который назначает, контролирует и изменяет терапию, проводимую больному практически постоянно. Особое внимание уделяют ограничению физической нагрузки, т.к. каждое физическое усилие больного с Л.с. сопровождается не только дополнительным дефицитом обеспечения сердца кислородом, но и дополнительной гиперфункцией миокарда вследствие возрастания гипертензии в малом круге кровообращения. Поэтому при обострениях бронхолегочных заболеваний и выраженной дыхательной недостаточности должны быть исключены посещения больным поликлиники; его либо госпитализируют, либо посещают на дому врач и медсестра.
Этиологическая терапия Л.с. зависит от основного заболевания. Так, при хронических бронхитах и пневмонии применяют антибактериальные средства (в случае обострения инфекционного процесса), коррекцию нарушений иммунитета, закаливание по индивидуально подобранному режиму, физиотерапевтические методы воздействия на воспалительный процесс; при повторных тромбоэмболиях показана хирургическая операция или (и) длительное применение антикоагулянтов и других средств для лечения флеботромбоза или Тромбофлебита.
Патогенетическая терапия занимает центральное место в комплексном лечении больных с подострим и хроническим легочным сердцем. Она направлена на снижение легочной гипертензии и включает также применение средств, противодействующих факторам развития дистрофии миокарда. При хронических неспецифических заболеваниях легких первоочередной задачей является устранение или снижение степени дыхательной недостаточности как основы патогенеза легочной артериальной гипертензии. Улучшение проходимости бронхов достигается индивидуальным подбором средств, которые соответствуют механизму бронхиальной обструкции в данной фазе течения болезни и включают при необходимости противовоспалительные, антигистаминные, отхаркивающие средства, позиционный дренаж, бронхолитические средства (см. Дыхательная недостаточность). Следует помнить, что применение бронхолитиков из класса β-адреномиметиков при Л.с., особенно декомпенсированном, должно строго контролироваться, т.к. вызываемое ими повышение потребности миокарда в кислороде не всегда обеспечивается соответствующим снижением гипоксемии (при недостаточном улучшении вентиляции альвеол) и усугубляет прогрессирование гипоксической миокардиодистрофии. Это относится и к препаратам группы теофиллина, в т.ч. пролонгированного действия (теопек), хотя они имеют некоторые преимущества, непосредственно снижая давление в малом круге кровообращения. Индивидуальный выбор бронхолитического средства для больного с Л.с. затруднен в связи с необходимостью ориентации не только на наибольший бронхолитический эффект, но и на способ введения (ингаляционный, внутрь), дозу и частоту применения, которые должны быть подобраны таким образом, чтобы не возрастала частота сердечных сокращений. При тяжелой бронхиальной обструкции смешанного патогенеза (воспаление, аллергический отек слизистой оболочки бронхов, перибронхиальный пневмосклероз) бронхолитические средства часто подобрать не удается. Поэтому декомпенсированное Л.с. у больных с бронхиальной обструкцией является одним из ведущих показаний к постоянному применению больным преднизолона или других глюкокортикоидов, если последние улучшают бронхиальную проходимость; при компенсированном Л.с. вопрос о целесообразности их использования решается в каждом случае индивидуально. При рестриктивной дыхательной недостаточности у больных с фиброзирующим процессом на фоне иммунопатологического поражения легочной паренхимы (фиброзирующий альвеолит, саркоидоз), а также при подостром Л.с. у больных с легочными васкулитами глюкокортикоиды нередко являются основным средством лечения. Характер и эффективность воздействия на сосудистые факторы легочной артериальной гипертензии определяются основным заболеванием, фазой его течения и соотношением органических и функциональных причин сужения просвета сосудистого русла. При обострениях хронической пневмонии, сопровождающихся выпотом фибрина на стенках микрососудов, их тромбозом в зонах воспаления, а также при васкулярном Л.с. показан гепарин, который способствует снижению сопротивления кровотоку, улучшает диффузию газов, уменьшает степень дыхательной недостаточности. При гематокрите выше 50% у больных с компенсаторной полицитемией снижение сопротивления кровотоку может быть достигнуто улучшением реологических свойств крови, например с помощью кровопусканий (при декомпенсированном легочном сердце), введения реополиглюкина (например, при астматическом статусе), применения дезагрегантов. Вазоактивные средства, снижающие гипертонию легочных артериол, а тем самым и давление в малом круге кровообращения, показаны при всех формах Л.с., особенно при первичной легочной артериальной гипертензии, но лишь в тех случаях, когда их эффективность подтверждается объективными показателями снижения АД в легочном стволе, например уменьшением амплитуды и площади зубца Р на ЭКГ или петли Р векторкардиограммы, зарегистрированных при большом усилении сигнала. Из этих средств могут быть назначены папаверин, но-шпа (обычно мало эффективны), производные теофиллина (в т.ч. теопек), антагонисты кальция (фенигадин), нитросорбид. По некоторым данным, применение нитратов показано в основном при декомпенсированиом Л.с., а антагонистов кальция — на более ранних стадиях, когда положительный гемодинамический эффект нитратов незначителен, а вызываемое ими увеличение шунтирования крови в легочных артериовенозных анастомозах нередко усугубляет гипоксемию. Замедление процессов дистрофии в гиперфункционирующем миокарде у больных с легочным сердцем реально достигается только максимальным ограничением физической нагрузки и устранением гипоксемии с помощью кислородной терапии (Кислородная терапия). Вспомогательное значение имеет использование рибофлавина-мононуклеотида, пиридоксальфосфата и кокарбоксилазы при обострениях дыхательной недостаточности (особенно у больных с явным или латентным сахарным диабетом), фосфадена, рибоксина, метандростенолона, Последний особенно показан истощенным больным и при постоянном применении глюкокортикоидов.
Симптоматическая терапия (на фоне этиологического и патогенетического лечения) необходима при декомпенсации Л.с. В зависимости от степени недостаточности кровообращения больному назначают домашний, полупостельный или постельный режим. Показана диета, обогащенная белками, легко усваиваемыми жирами и витаминами (особенно А, В, С); ограничивают употребление поваренной соли, исключают продукты, вызывающие у больного метеоризм. Как и при сердечной недостаточности другого происхождения, применяют фенигидин, нитраты и другие вазодилататоры, мочегонные средства и сердечные гликозиды, но тактика использования последних при Л.с. отличается рядом существенных особенностей в связи с гипоксией миокарда, обусловленной дыхательной недостаточностью. Терапевтический эффект гликозидов не может реализоваться в условиях дефицита окислительного фосфорилирования, связанного с гипоксией, а вероятность токсического их действия на миокард при этом существенно повышается прежде всего из-за снижения содержания в кардиомиоцитах калия (гипокалигистия всегда сопутствует гипоксическому повреждению клеток). Поэтому при назначении сердечных гликозидов больным с Л.с. учитывают высокую опасность дигиталисной интоксикации не только в период насыщения, но и при постоянном применении уже подобранной поддерживающей дозы, которая может стать токсической в случае обострения дыхательной недостаточности и возрастания в связи с этим степени гипоксии миокарда. Основные особенности использования гликозидов состоят в следующем: 1) предпочтение отдают препарату, который имеет больший коэффициент суточной элиминации, что укорачивает период токсического действия после необходимой при этом отмены гликозида, например для внутривенного введения по неотложным показаниям коргликон лучше строфантина, для постоянного приема внутрь изоланид предпочтительнее дигоксина, а дигитоксин и лист наперстянки в порошке практически не применяют; 2) при сохранении принципа индивидуального дозирования для случаев первого применения препарата начальная доза коргликона не превышает 0,6 мл 0,06% раствора, строфантина К — 0,25 мл 0,05% раствора либо насыщение производится путем капельного введения этих препаратов под контролем ЭКГ; насыщение гликозидами для перорального применения проводят в темпе медленной дигитализации, т.е. суточная доза в первые дни приема для дигоксина не превышает 0,75 мг, для изоланида — 1,25 мг; 3) начальную дигитализацию в период резко выраженного обострения дыхательной недостаточности проводят только на фоне кислородной терапии и только путем капельного внутривенного введения коргликона или строфантина; переход на применение внутрь изоланида или дигоксина и определение их поддерживающей дозы осуществляют только после стабилизации дыхательной недостаточности на уровне, обычном для фазы ремиссии болезни у данного больного; 4) одновременное с коргликоном или строфантином введение β-адреномиметиков, эуфиллина, кофеина, а также растворов препаратов кальция недопустимо (опасность суммационного влияния на гетеротопный автоматизм с исходом в фибрилляцию желудочков); при необходимости сочетанной парентеральной терапии бронхолитиками, например эуфиллином, и сердечными гликозидами первым вводят эуфиллин и через 30—45 мин коргликон или строфантин капельно; 5) для постоянного применения в амбулаторных условиях рекомендуют только 2/3 суточной поддерживающей дозы гликозида, которая определена как индивидуальная после завершения периода насыщения; при этом больному рекомендуют самостоятельно отменять прием препарата до прихода врача во всех случаях усугубления дыхательной недостаточности (при обострениях бронхита, бронхиальной астмы и т.п.); 6) терапия сердечными гликозидами проводится на фоне использования препаратов калия (или калийсберегающих диуретиков), что особенно важно при дыхательной недостаточности высоких степеней.
Имеются данные о целесообразности при хроническом легочном сердце так называемой профилактической дигитализации, т.е. постоянного применения сердечных гликозидов со времени формирования четких клинических признаков гипертрофии правого желудочка сердца. Это отдаляет сроки его декомпенсации, наступающей обычно при стабильно тяжелой дыхательной недостаточности, когда лечение гликозидами чрезвычайно затруднено или невозможно и соответственно возрастает роль мочегонных средств. Выбор при дыхательной недостаточности оптимального мочегонного препарата по отклонениям рН, содержанию СО2 и электролитов в крови возможен только в условиях стационара. При применении мочегонных средств (Мочегонные средства) в условиях поликлиники исходят из опасности для больного с Л.с. повышенных потерь с мочой калия и учитывают возможность декомпенсации дыхательного ацидоза при использовании диакарба больными с гиперкапнией. Обычно назначают либо калийсберегающие мочегонные средства, либо фуросемид в сочетании со спиронолактоном, подбирая дозу и частоту применения по диурезу или, что лучше, по изменению массы тела больного, для чего больному рекомендуют приобрести напольные весы. Кровопускания (300—400 мл крови) при лечении больного дома показаны только при тяжелой степени сердечной недостаточности с высокой венозной гипертензией и наличии полицитемии (не чаще 1 раза за 2 нед.). К основным клиническим признакам, которые позволяют прогнозировать лечебный эффект кровопусканий, относится набухание шейных вен, сохраняющееся на входе в положении больного сидя в сочетании с красным (фиолетовым) оттенком цианоза лица.
Первичная профилактика Л.с. состоит в предупреждении и эффективном лечении болезней, при которых оно развивается.
Прогноз заболеваний, осложняющихся Л.с., всегда серьезный. Тромбоэмболия легочных артерий представляет непосредственную угрозу жизни больного, но если она не завершается смертельным исходом, то большинство признаков острого Л.с. регрессирует, как правило, в течение первой недели, а при эффективном лечении и в случаях поражения артерий некрупного калибра — в течение первых двух суток. Аналогична динамика острого Л.с. при пневмотораксе, астматическом статусе. В случае подострого Л.с. прогноз плохой как для трудоспособности больного (она резко ограничивается практически сразу), так и для жизни в ближайшие месяцы или 3—5 лет, что связано с неизлечимостью и прогрессирующим характером основных заболеваний (лимфогенный карциноматоз легких, первичная легочная артериальная гипертензия, прогрессирующий фиброзирующий альвеолит и др.). Развитие хронического Л.с. при хронических неспецифических заболеваниях легких носит прогрессирующий характер и ухудшает их прогноз. В редких случаях назначение тяжелым больным для постоянного применения глюкокортикоидов дает столь выраженное снижение степени дыхательной недостаточности и легочной артериальной гипертензии, что гиперфункция правого желудочка сердца резко снижается и в течение многих лет легочное сердце не прогрессирует.
Библиогр.: Основы пульмонологии, под ред. А.Н. Кокосова, с. 288, М., 1976; Рабкин И.X. Рентгеносемиотика легочной гипертензии, М., 1967; Руководство по внутренним болезням, под ред. Е.М. Тареева, т. 3, с. 335, М., 1964; Тихонов К.Б. Рентгенологическая симптоматика сердечной недостаточности, Л., 1985; Хронический бронхит и легочное сердце, под ред. Н.В. Пугова, Л., 1983; Цагарели З.Г. и Гогиашвили Л.Е. ункциональная морфология сердечно-легочного синдрома, Тбилиси, 1982, библиогр.
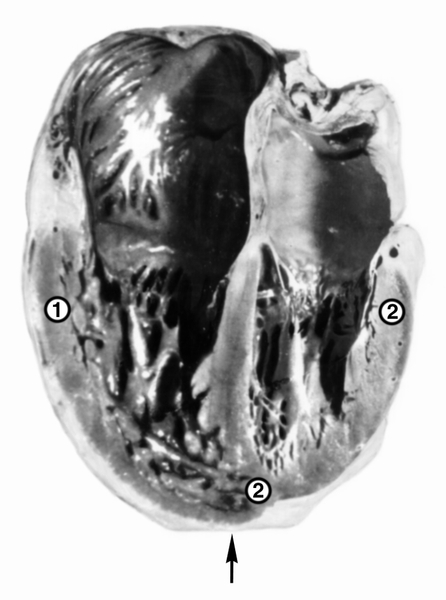
Рис. 1. Макропрепарат сердца при первичной легочной артериальной гипертензии: гипертрофия трабекул и стенки (1) правого желудочка, которая по толщине превышает стенку левого желудочка (2), расширение правых полостей сердца, верхушка сердца (указана стрелкой) сформирована правым желудочком.
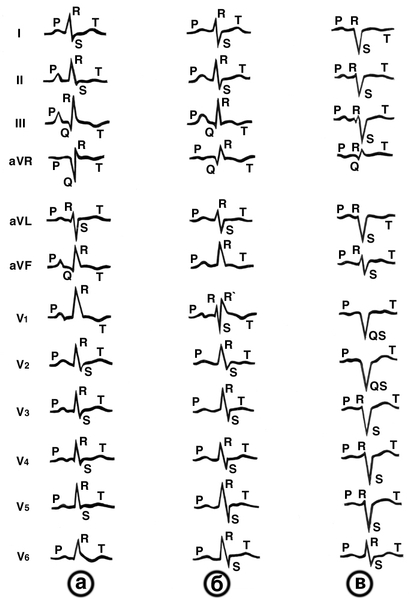
Рис. 3. Основные типы электрокардиограммы при хроническом легочном сердце: а — R-тип, определяется высокий зубец R в правых грудных, а также во II, III отведениях; б — RSR’-тип (по наличию зубца R’ в отведении V1), отмечаются увеличение зубца S при уменьшении зубца R в отведениях I, II и левых грудных, зубец R в отведении aVR; в — S-тип, определяются глубокие зубцы S во всех стандартных и грудных отведениях, желудочковый комплекс в отведениях V1 и V2 имеет форму QS.
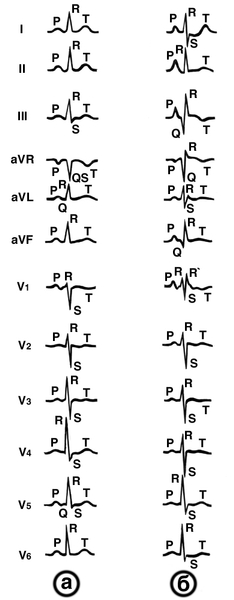
Рис. 2. Электрокардиограммы больной с тромбоэмболией легочной артерии: а — до тромбоэмболии (отклонений от нормы нет); б — через 12 часов после тромбоэмболии — картина острого легочного сердца; определяются синдром SIQIII, смещение переходной зоны влево (из отведения V3 в отведение V4), появление зубцов R и R’ в отведениях VR, V1 и зубцов S в левых грудных отведениях, инверсия зубца TIII, увеличение зубцов Р в отведениях II, III (Р3-pulmonale и положительной фазы зубца Р в отведении V1).
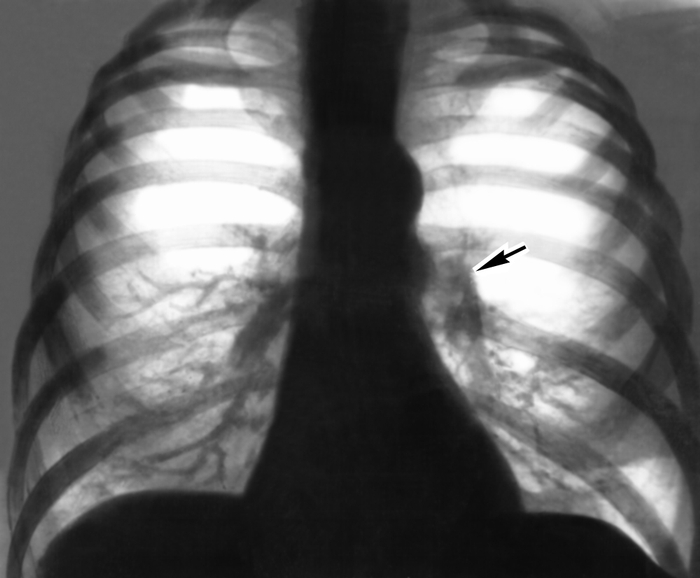
Рис. 4. Рентгенограмма органов грудной полости больного с эмфиземой легких и хроническими легочным сердцем (прямая проекция): сердце имеет относительно небольшие размеры, дуга легочного конуса (указана стрелкой) выбухает, корни расширены за счет крупных ветвей легочных артерий, периферический сосудистый рисунок легких обеднен.
