2,2-азо-бис-изобутиронитрил
2,2-АЗО-бис-ИЗОБУТИРОНИТРИЛ (динитрил азоизомасляной кислоты, порофор N) (CN)(CH3)2CN==NC(CH3)2(CN)
мол. м. 164,21; бесцветные кристаллы; т. пл. 105–106 °C (с разл.); очень плохо раств. в воде, плохо — в спирте и эфире. Растворимость А. (г на 100 г растворителя при 25 °C): в акрилонитриле-38, хлороформе-25, метиленхлориде-40, метилметакрилате-10.
Для А. наиб. характерно термич. разложение с элиминированием N2 и образованием цианоизопропильных радикалов (CH3)2C(CN). Реакция сопровождается рекомбинацией радикалов с образованием неустойчивого кетенимина (CH3)2C(CN)N==С==С(CH3)2 и тетраметилсукцинодинитрила (CH3)2C(CN)—(CN)C(CH3)2. Разложение происходит практически с постоянной скоростью, является реакцией первого порядка и мало зависит от природы растворителя. Константы скорости реакции (k*104, с −1) при 80 °C в ксилоле, уксусной кислоте, диметиланилине, додецилмеркаптане и изобутаноле соотв. равны 1,53; 1,52; 1,83; 1,46 и 1,72. Энергия активации (в ксилоле) 131 кДж/моль.
В промышленности А. получают из ацетонциангидрина:
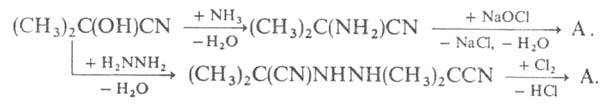
А. — один из важнейших инициаторов свободнорадикаль-ной полимеризации и теломеризации (напр., стирола, винилхлорида и винилиденхлорида, акрилатов и метакрила-тов, акрилонитрила, диенов), порообразователь в производстве пенопластов и пористых резин. Инициирование А. в отличие от бензоилпероксида не сопровождается окислением.
А. достаточно устойчив при 0-5 °C, но при более высоких температурах склонен к самовозгоранию. Взрывается от сильного удара или трения; т. самовоспл. паров 240 °C; ниж. КПВ пылевоздушной смеси 5,2 г/м3. При хранении А. защищают от прямых солнечных лучей и источников тепла.
Лит.: Прайер У., Свободные радикалы, пер. с англ., М., 1970; Девис Д., Перрет М., Свободные радикалы в органическом синтезе, пер. с англ., М., 1980.
С. К. Смирнов
