электрокристаллизация
ЭЛЕКТРОКРИСТАЛЛИЗАЦИЯ
образование и рост кристаллов в объеме раствора (расплава) или на поверхности электрода в результате протекания электрохим. реакции. Является фазовым переходом I рода. Имеет много общего с кристаллизацией из пара и раствора, но в отличие от этого процесса в условиях Э. происходит акт переноса заряда, который предшествует встраиванию атомов в места роста кристаллов или протекает одновременно с ним.
Различают гомогенную и гетерогенную электрохим. нуклеацию, т. е. зарождение кристаллов новой фазы. Первая имеет место, напр., при восстановлении ионов в объеме раствора с образованием коллоидных частиц, вторая — при восстановлении ионов на поверхности электрода. Зарождению кристаллов на поверхности электрода может предшествовать образование слоев адсорбир. атомов (адатомов) осаждаемого вещества, чаще всего металла. Возникновение моноатомных (иногда двух- и трехатомных) слоев происходит при электродных потенциалах, на неск. десятков мВ положительнее равновесного. Степень заполнения поверхности адсорбир. атомами влияет на скорость зарождения кристаллов новой фазы (число зародышей в единице объема, образующихся за единицу времени).
Зарождение кристаллов в условиях Э. требует превышения электрохим. потенциала системы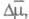 пропорционального перенапряжению
пропорционального перенапряжению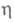 (см.. Поляризация);
(см.. Поляризация); 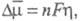 где n — число участвующих в реакции электронов; F — постоянная Фарадея. Нуклеация в объеме раствора или на поверхности инертного электрода начинается путем образования трехмерных зародышей, т. е. частиц, размеры которых соизмеримы по всем кристаллографич. направлениям. Для малых
где n — число участвующих в реакции электронов; F — постоянная Фарадея. Нуклеация в объеме раствора или на поверхности инертного электрода начинается путем образования трехмерных зародышей, т. е. частиц, размеры которых соизмеримы по всем кристаллографич. направлениям. Для малых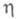 кинетика электрохим. нуклеации описывается классич. флуктуационной теорией, согласно которой в результате флуктуац. процессов присоединения и отрыва частиц в маточной среде возникает набор кластеров, распределенных по размерам (см. зарождение новой фазы). Частоты присоединения и отрыва частиц для электрохим. систем определяются величиной
кинетика электрохим. нуклеации описывается классич. флуктуационной теорией, согласно которой в результате флуктуац. процессов присоединения и отрыва частиц в маточной среде возникает набор кластеров, распределенных по размерам (см. зарождение новой фазы). Частоты присоединения и отрыва частиц для электрохим. систем определяются величиной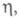 зависят от кривизны поверхности кластеров и адсорбционных характеристик. Вероятность возникновения кластера данного размера определяется законом распределения Больцмана, а кинетика — частотами присоединения и отрыва частиц. Кластер, присоединение атома к которому делает его устойчивым к дальнейшему росту при данном перенапряжении, наз. критич. зародышем, работа образования которого для гомогенного зарождения равна:
зависят от кривизны поверхности кластеров и адсорбционных характеристик. Вероятность возникновения кластера данного размера определяется законом распределения Больцмана, а кинетика — частотами присоединения и отрыва частиц. Кластер, присоединение атома к которому делает его устойчивым к дальнейшему росту при данном перенапряжении, наз. критич. зародышем, работа образования которого для гомогенного зарождения равна:
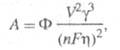
где Ф — фактор формы зародыша; V- молярный объем кристаллич. фазы; 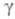 - уд. межфазная поверхностная энергия.
- уд. межфазная поверхностная энергия.
Соответственно скорость зарождения кристалла / при температуре Т описывается уравнением:
I = к ехр(-A/kT),
где k — постоянная Больцмана. Для систем с высокими значениями тока обмена (электроды из Ag, Pb, Hg) в небольших интервалах изменений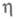 коэф. к остается постоянной величиной и наблюдается линейная зависимость lgI от
коэф. к остается постоянной величиной и наблюдается линейная зависимость lgI от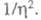 С ростом
С ростом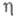 размер критич. зародыша уменьшается и при высоких
размер критич. зародыша уменьшается и при высоких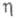 зародыш может состоять из единичных атомов. В этом случае использование значения
зародыш может состоять из единичных атомов. В этом случае использование значения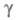 в уравнении для А становится некорректным, кинетика электрохим. нуклеации описывается атомистич. теорией, согласно которой скорость образования зародышей и число атомов в зародыше дискретно изменяются с ростом
в уравнении для А становится некорректным, кинетика электрохим. нуклеации описывается атомистич. теорией, согласно которой скорость образования зародышей и число атомов в зародыше дискретно изменяются с ростом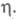 Число атомов в зародыше остается неизменным в некотором интервале значений
Число атомов в зародыше остается неизменным в некотором интервале значений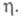
Критич. зародыши образуются на активных центрах поверхности электрода. Такими центрами м. б. поры в оксидной пленке, выходы винтовых дислокаций, вакансии, изломы на ступенях роста и др. энергетич. неоднородности поверхности. Число активных центров, участвующих в процессе электрохим. нуклеации, возрастает с увеличением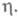 Вокруг возникшего и растущего кристалла образуются зоны экранирования ("дворики роста"), в которых нуклеации не происходит. Радиус зон экранирования уменьшается с ростом
Вокруг возникшего и растущего кристалла образуются зоны экранирования ("дворики роста"), в которых нуклеации не происходит. Радиус зон экранирования уменьшается с ростом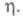 Постепенно происходит исчерпание числа свободных активных центров и прекращение зарождения новых кристаллов, наступает насыщение. Адсорбция примесей из раствора на электроде снижает число активных центров и, соотв., общее число зародышей. Стадия зарождения кристаллов определяет в конечном итоге осн. физ.-мех. свойства гальванич. покрытий, в т. ч. их пористость.
Постепенно происходит исчерпание числа свободных активных центров и прекращение зарождения новых кристаллов, наступает насыщение. Адсорбция примесей из раствора на электроде снижает число активных центров и, соотв., общее число зародышей. Стадия зарождения кристаллов определяет в конечном итоге осн. физ.-мех. свойства гальванич. покрытий, в т. ч. их пористость.
На атомногладкой грани кристалла его рост происходит путем образования двумерного критич. зародыша и его последующего разрастания. Возникновение двумерного зародыша требует определенного перенапряжения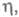 связанного с возникновением новой поверхности — ступени роста и, соотв., избыточной краевой энергии. Распространение растущего слоя по поверхности грани происходит тангенциально, путем присоединения атомов к местам роста (изломам на ступени). Такая Э. наблюдается на бездислокационных гранях монокристаллов Ag, полученных электролизом в капиллярах. При повышении
связанного с возникновением новой поверхности — ступени роста и, соотв., избыточной краевой энергии. Распространение растущего слоя по поверхности грани происходит тангенциально, путем присоединения атомов к местам роста (изломам на ступени). Такая Э. наблюдается на бездислокационных гранях монокристаллов Ag, полученных электролизом в капиллярах. При повышении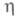 по грани распространяются многослойные "пакеты роста".
по грани распространяются многослойные "пакеты роста".
На гранях, имеющих выходы винтовых дислокаций и вследствие этого неисчезающую ступень, распространение слоев при Э. происходит в виде спирали, путем присоединения атомов к ступени роста. Грань (или ее часть) принимает форму пирамиды. Чем выше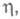 тем меньше угол при вершине пирамиды. Подобная Э. по дислокационному механизму не требует затраты энергии на образование двумерных критич. зародышей.
тем меньше угол при вершине пирамиды. Подобная Э. по дислокационному механизму не требует затраты энергии на образование двумерных критич. зародышей.
При высоких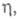 равных 5–10 kT (150–300 мВ), становится возможным "нормальный" рост кристаллов, т. е. прямое присоединение атомов к поверхности растущей грани в любой ее точке. Грани становятся шероховатыми, теряются такие свойства кристалла, как устойчивость роста грани и анизотропия скоростей роста по разл. кристаллографич. направлениям. В результате кристаллы приобретают округлую форму.
равных 5–10 kT (150–300 мВ), становится возможным "нормальный" рост кристаллов, т. е. прямое присоединение атомов к поверхности растущей грани в любой ее точке. Грани становятся шероховатыми, теряются такие свойства кристалла, как устойчивость роста грани и анизотропия скоростей роста по разл. кристаллографич. направлениям. В результате кристаллы приобретают округлую форму.
Кинетика Э. Фазовый переход ион в растворе → атом в кристаллич. решетке металла протекает через ряд стадий: разряд иона с образованием адатомов, их поверхностная диффузия к месту роста и встраивание в кристаллич. решетку. Каждая из стадий может определять скорость процесса. При низких перенапряжениях (< 30 мВ) для Cu и Ag скорость процесса определяется поверхностной диффузией, при более высоких перенапряжениях — стадией переноса заряда. Адатомы могут нести некоторый электрич. заряд вследствие частичного разряда ионов. Вероятность разряда иона непосредственно в месте роста или на поверхности грани с последующей диффузией адатомов к месту роста зависит от концентрации ионов в растворе, энергии их десольватации и энергии связи атомов в кристаллич. решетке. Предполагается, что преимущественный разряд ионов в месте роста может происходить при энергии сублинации (характеризующей энергию связи атомов в решетке) более 300 Дж/моль.
Формы роста кристаллов определяются относит. пересыщением раствора, которое в условиях Э. соответствует величине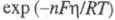 — 1(R — газовая постоянная), а также концентрацией разряжающихся ионов, условиями массопереноса, адсорбцией примесей. При малых плотностях тока через электрохим. ячейку и, соотв., низких перенапряжениях
— 1(R — газовая постоянная), а также концентрацией разряжающихся ионов, условиями массопереноса, адсорбцией примесей. При малых плотностях тока через электрохим. ячейку и, соотв., низких перенапряжениях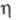 наблюдается рост единичных кристаллов, в частности нитевидных. Количество металла, выделяющегося на единице площади поверхности растущих граней при электролизе, сохраняется постоянным при разл. величинах силы тока и, соотв., общая площадь растущих граней подстраивается к заданной плотности тока. Быстро растущие грани кристаллов вырождаются в процессе роста, кристалл оказывается оформленным медленно растущими гранями. В отсутствие примесей кристаллы с гранецентрир. или объемноцентрир. кубич. решетками обычно оформлены гранями (111), (100), (110).
наблюдается рост единичных кристаллов, в частности нитевидных. Количество металла, выделяющегося на единице площади поверхности растущих граней при электролизе, сохраняется постоянным при разл. величинах силы тока и, соотв., общая площадь растущих граней подстраивается к заданной плотности тока. Быстро растущие грани кристаллов вырождаются в процессе роста, кристалл оказывается оформленным медленно растущими гранями. В отсутствие примесей кристаллы с гранецентрир. или объемноцентрир. кубич. решетками обычно оформлены гранями (111), (100), (110).
При малых концентрациях ионов в растворе массоперенос к растущей поверхности играет главенствующую роль в определении морфологии роста кристаллов при Э. Высокие плотности тока обеспечивают перенапряжение, достаточное для роста боковых граней нитевидного кристалла, на катоде возникают дендриты. Адсорбция и соосаждение примесей тормозят линейный рост кристаллов, вызывают искажение кристаллич. решетки и понижают устойчивость фронта роста граней, способствуют образованию на электроде соматоидных структур. При больших концентрациях соосаждающихся примесей (Р, В, S и др.) кристаллич. решетка оказывается предельно нарушенной, возникают системы аморфного строения — металлич. стекла.
Э. — уникальный метод для изучения механизма зарождения и роста кристаллов, т. к. позволяет изменять пересыщение в широких интервалах и по любой программе. Э. — основа многих электрохим. технологий, в т. ч. электролиза, гальванотехники. Осаждение металлов из разбавленных растворов в условиях роста дендритов используют для получения порошков Cu, Ni, Fe и др. (см. также электроосаждение).
Лит.: Горбунова К.М., Данков П.Д., "Успехи химии", 1948, т. 17, с. 710–32; Феттер К., Электрохимическая кинетика, пер. с нем., М., 1967; Каишев Р., Избранные труды, София, 1980; Данилов А.И., Полукаров Ю.М., "Успехи химии", 1987, т. 56, в. 7, с. 1082–1104.
Ю. М. Полукаров
Значения в других словарях
- Электрокристаллизация — Электроосаждение, кристаллизация металлов и сплавов на катоде при электролизе растворов и расплавов соответствующих солей. Рост кристаллов при Э. металлов имеет много общего с кристаллизацией (См. Большая советская энциклопедия
- электрокристаллизация — орф. электрокристаллизация, -и Орфографический словарь Лопатина
