фосфорорганические соединения
ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
содержат в молекулах атом P, связанный с орг. радикалами непосредственно или через гетероатом (О, S, N и др.). Первые Ф. с. (смесь метилфосфинов) получены в 1846 Л. Тенаром и И. Берцелиусом при метилировании фосфида Ca.
Классификация. Ф. с. можно классифицировать по количеству заместителей у атома P (координационному числу), которых м. б. от 1 до 6. Примеры соед. с разл. координационным числом атома P приведены в табл. 1.
Табл. 1 — ПРИМЕРЫ ФОСФОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С РАЗЛИЧНЫМИ КООРДИНАЦИОННЫМИ ЧИСЛАМИ АТОМА P
таблица в процессе добавления
По др. классификации, охватывающей наиболее распространенные Ф. с., выделяют фосфорсодержащие кислоты (см. также фосфора кислоты) и их производные (табл. 2), а также фосфины и родств. соединения.
Табл. 2 — НАЗВАНИЕ НЕКОТОРЫХ КИСЛОТ ФОСФОРА, ИХ ЭФИРОВ И СОЛЕЙ
таблица в процессе добавления
* Используются формулы таутомерных форм кислот с трехвалентным атомом P.
К Ф. с. второго типа относятся первичные RPH2, вторичные R2PH и третичные R3P фосфины, а также окисленные формы последних: фосфиноксиды R3PO, фосфинсульфиды R3PS (см. фосфиноксиды и фосфинсульфиды), фосфинселениды R3PSe, фосфазосоединения R3P = NR и фосфинал-килены R3P = CR2. Ко второму типу принадлежат также фосфониевые соединения 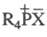 и фосфораны R5P.
и фосфораны R5P.
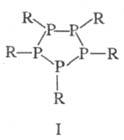
Известны также полифосфины и их производные [напр., дифосфины R2P — PR2, цик- лопентафосфины (формула I)] и металлокомплексы [напр., (RO)3P∙ CuBr, (R3P)3RhCl, R3PO∙ SnR4]. Во всех приведенных формулах радикалы R м. б. одинаковыми или различными.
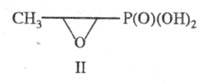
Распространение в природе. Разнообразные Ф. с. содержатся в живых организмах, где выполняют ответственные биол. функции. К ним, напр., относятся нуклеиновые кислоты, нуклеотиды, фосфаты моносахари-дов (напр., глюкозо-1- и глюкозо-6-фосфаты), нуклеозидмоноцик-лофосфаты (напр., аденозинмоно-фосфат циклический), разл. типы фосфолипидов и др. К прир. Ф. с. также относят производные фосфоновых кислот — антибиотик фосфомицетин (II), фосфорные аналоги 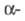 и β-аминокарбоновых кислот и пептиды на их основе.
и β-аминокарбоновых кислот и пептиды на их основе.
Физические свойства. Ф. с. могут быть газами, жидкостями или твердыми веществами. Для идентификации и изучения их свойств используют все осн. физ.-хим. методы, но в первую очередь — спектроскопию ЯMP31P. Величины хим. сдвигов определяются гл. обр. электроотрицательностями атомов, связанных с атомом P, и степенью обратного π-дативного взаимод. с ним. Сигналы ЯМР31Р располагаются в очень широкой области значений (неск. сотен м. д.) и проявляют при этом выраженную специфичность (рис.).
Химические свойства. 1. Таутомерия. Для гидрофосфорильных соединений и тиогидрофосфорильных соед. известен такой вид прототропии:
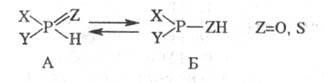
Как правило, равновесие сдвинуто в сторону формы А, однако при наличии сильных электроноакцепторных заместителей X и Y [напр., (CF3)2POH] — в сторону Б.
Циклич. средние фосфиты и амидофосфиты с протонодо-норной группой в боковой цепи могут частично или полностью превращаться в гидроспирофосфорановые формы:
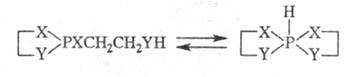
Тиокислоты фосфора характеризуются особым видом прототропии:
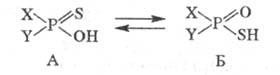
Увеличение электроноакцепторных свойств заместителей X и Y приводит к накоплению формы Б. В химии Ф. с. известны и фосфотропные процессы, напр.:
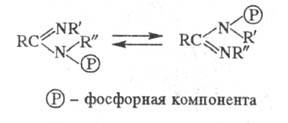
Если радикалы R и R' одинаковые, то процесс является вырожденным.
Особый вид таутомерии (псевдовращение) характерен для фосфоранов, которые способны обменивать у атома P заместители, занимающие аксиальные и экваториальные положения:
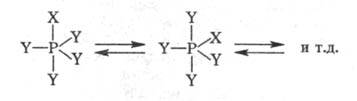
Принцип псевдовращения широко используют для объяснения механизмов реакций Ф. с.
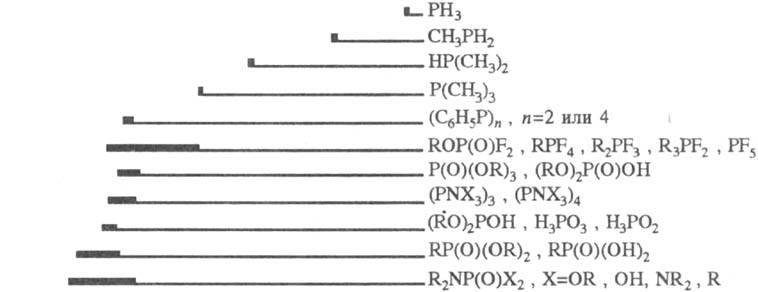
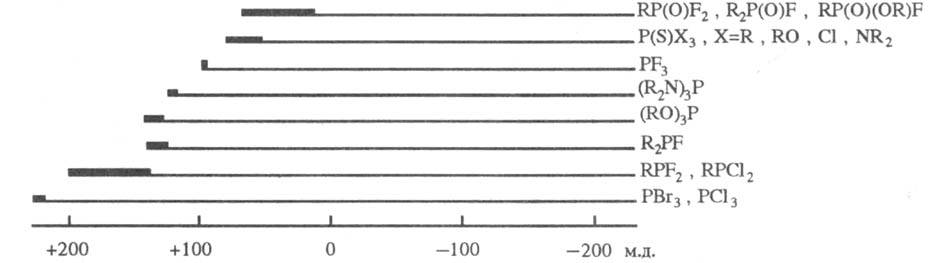
Области хим. сдвигов 31P фосфорорг. соед. относительно 85%-ной H3PO4; производные двухкоординационного P характеризуются хим. сдвигами в очень сильных полях (до 450 мд.).
2. Диспропорционирование. Производные пяти- и особенно трехвалентного P, в молекулах которых атомы P связаны с разл. электроноакцепторными группами, склонны к межмол. обмену этими группами, напр.:
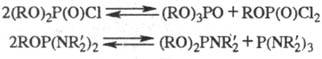
Диспропорционирование обычно катализируется кислотами. Наличие циклич. фрагментов в молекуле препятствует диспро-порционированию.
3. Фосфорилирование. С помощью Ф.с., в молекулах которых атом P связан с электроноакцепторной (уходящей) группой, можно вводить фосфорный остаток в состав нуклеофилов (осуществлять (расформирование). В качестве уходящих групп обычно выступают галогениды, алкокси-, тиоалкоксигруппы и др., напр.:

Кислоты также используют в качестве фосфорилирующих средств, однако, как правило, после предварит. активации, т. е. после превращения кислотного гидроксила в легкоуходящую группу, напр.:
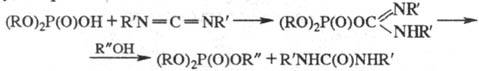
Производные кислот с трехвалентным атомом P проявляют более высокую фосфорилирующую активность, чем производные кислот с пятивалентным атомом P.
4. Важнейшие реакции производных трехвалентного P. Эти соед. легко окисляются, присоединяют атомы S, Se, Те, Hal, иминируются, алкилируются:
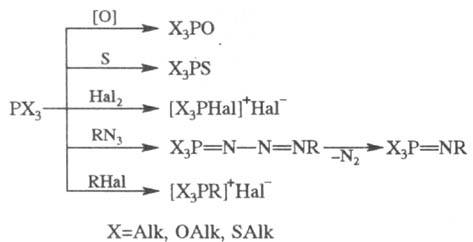
Если X = OAlk, SAlk, то первичный продукт взаимод. PX3 с RHal далее распадается с образованием фосфорильного (тиофосфорильного) соед. (Арбузова реакция):
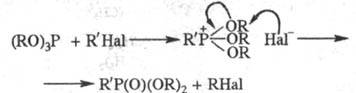
При взаимодействии средних фосфитов с a-галогенкарбонильными соед. может происходить как реакция Арбузова, так и иной процесс, приводящий к фосфовиниловым эфирам (Перкова реакция):

Многие производные трехвалентного P присоединяются к сопряженным диенам и другим 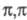 -сопряженным системам; образующиеся продукты могут выделяться как целевые вещества либо без выделения вступать в дальнейшие превращения, напр.:
-сопряженным системам; образующиеся продукты могут выделяться как целевые вещества либо без выделения вступать в дальнейшие превращения, напр.:
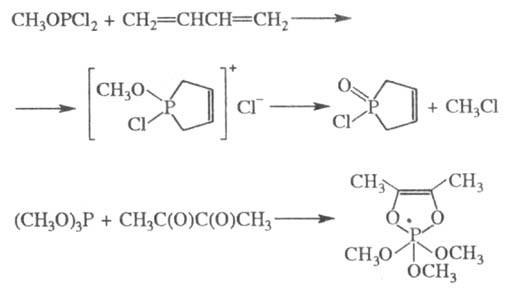
Соед. с трехвалентным атомом P легко образуют комплексы с производными переходных металлов, напр.:
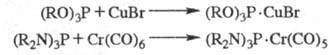
5. Важнейшие реакции производных пятивалентного P. Кислород фосфорильной группы в таких Ф. с. заменяется на серу под действием P2S5. В молекулах третичных фосфиноксидов он элиминируется при восстановлении трихлорсиланом:
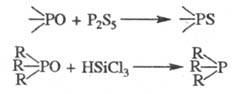
Сложные эфиры тионовых кислот при действии алкилгалогенидов или при нагр. претерпевают тион-тиольную перегруппировку:
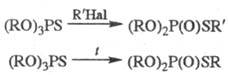
В большинстве фосфорильных соед. со связью С — P α-метиленовые протоны фосфорильной группы подвижны, что приводит к их депротонированию при действии сильных оснований. Образующиеся карбанионы при взаимодействии с альдегидами и кетонами образуют олефины (Корнера реакция):
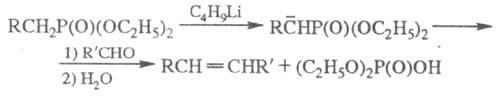
Подобная реакция происходит под действием фосфиналкиле-нов (Виттига реакция):

α -Гидроксифосфонаты при нагр. в присутствии оснований могут превращаться в фосфаты (фосфонатфосфатная перегруппировка):
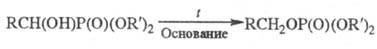
Фосфорильные соед. образуют комплексы с разл. переходными и непереходными металлами с участием кислорода фосфорильной группы. Устойчивость комплексов обычно сильно возрастает при хелатировании металла.
Получение Ф. с. Общий путь синтеза Ф. с. включает три последоват. стадии: 1) получение элементарного фосфора из минер. сырья; 2) превращение фосфора в неорг. производные (P4O10, PCl3, PCl5, POCl3); 3) получение Ф. с. взаимод. этих производных со спиртами, аминами, альдегидами, олефинами и др. Возможно также превращение фосфора в Ф. с., минуя неорг. производные (напр., путем взаимодействия элементарного P с алкилгалогенидами или спиртами).
Среди многочисленных способов синтеза конкретных Ф. с. (они приведены в статьях о группах соед.) выделяют методы, позволяющие получать соед. со связью С — P. Эти методы приведены ниже.
Фосфины и гидрофосфорильные (тиогидрофосфорильные) соед. в условиях гомолитич. реакций легко присоединяются к олефинам с образованием связи C-P:
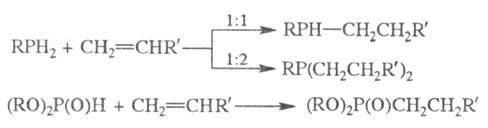
Эти же соед. в условиях гетеролитич. реакций присоединяются по связям C = O, C = N, C = S, C = C с образованием разнообразных функционализир. Ф. с.:
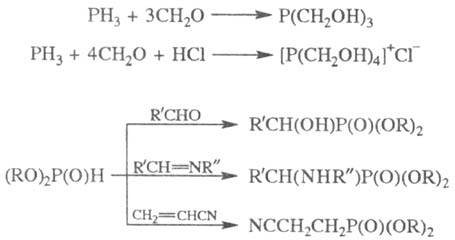
При алкилировании и арилировании средних эфиров кислот трехвалентного P образуется новая связь C-P (реакция Арбузова). Аналогично осуществляется реакция с использованием металлич. солей гидрофосфорильных соед. (Михаэлиса — Бек-кера реакция):

Этот синтез целесообразно проводить в условиях межфазного катализа. Галогенангидриды орг. кислот фосфора образуются при присоединении PCl5 и родственных веществ к непредельным соед.:

Эта реакция хорошо идет в случае использования виниловых эфиров.
При взаимодействии алканов или алкенов с PCl3 и кислородом образуются сложные смеси веществ, осн. компонентами которых являются дихлорангидриды фосфоновых кислот (см. также окислительное хлорфосфонирование):
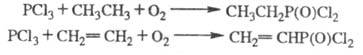
Ароматич. соед. легко фосфорилируются PCl3, P2S5 и др. электрофилами в условиях реакции Фриделя — Крафтса:
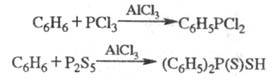
Алкилгалогениды в присуг. кислот Льюиса алкилируют PCl3 с образованием связи C-P (Клея — Киннера — Перрена реакция):
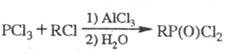
При нагр. белого или красного P с арил- или алкилгалогенидами образуется смесь хлорфосфинов. Вариант этой реакции, представляющий практич. значение,- алкилирование P в присутствии иода.
Связь C-P образуется также при взаимодействии галогенангидридов кислот фосфора с металлоорг. соед.; при этом один или неск. атомов галогена обмениваются на углеводородные радикалы:
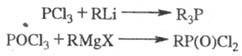
В некоторых случаях в эти реакции нуклеоф. замещения по атому P вступают и эфиры кислот фосфора.
Применение. Ф. с. широко используют в технике, сельском хозяйстве и медицине. Многие из них в качестве комплексонов и экстрагентов применяются при получении цветных и редких металлов; для борьбы с коррозией и отложением солей в техн. водах; в качестве стабилизаторов и пластификаторов полимеров; в качестве мономеров для ионообменных и термостабильных полимеров, присадок для смазочных масел и гидравлич. жидкостей. Многие Ф. с. — лек. средства, пестициды, фпотореагенты, ПАВ; некоторые фосфаты и фосфины, в т. ч. обладающие оптич. активностью, применяют для получения металлокомплексных катализаторов. Среди Ф. с. имеются отравляющие вещества.
• см. также фосфорсодержащие гетероциклы
Лит.: Кабачник М.И., Фосфорорганические вещества, М., 1967; Ни-фантьев Э.Е., Химия фосфорорганических соединений, М., 1971; Пурдела Д., Вылчану Р., Химия органических соединений фосфора, пер. с рум., М., 1972; Арбузов А.Е., Избранные труды по химии фосфорорганических соединений, М., 1976; Корбридж Д., Фосфор. Основы химии, биохимии, технологии, пер.с англ., М., 1982; Нифантьев Э.Е., Kухарева Т.С., Обзор монографий и обзоров по химии фосфорорганических соединений, М., 1989; S a s s е К., в кн.: Houben-Weyl, Methoden der organischen Cheniie, 4 Aufl., Bd 12/1, Bd 12/2, Stuttg., 1963–64; Organic phosphorus compounds, eds, G.M. Kosolapoff, L. Maier, v. 1–7, N.Y. — [a.o.], 1972–76; Dictionary of organo-phosphorus compounds, ed. R.S. Edmundson, L., 1988.
Э. Е. Нифантьев
Значения в других словарях
- Фосфорорганические соединения — Обширный класс органических соединений, содержащих в своём составе фосфор. Различают Ф. с., в молекулах которых фосфор непосредственно связан с углеродом, и Ф. Большая советская энциклопедия
- фосфорорганические соединения — ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, группа производных эфиров фосфорных кислот. Различают Ф. с. контактного и системного действия. Последние нестойки во внеш. среде, многие из них обладают высокой токсичностью для животных и человека (токсичность Ф. Ветеринарный энциклопедический словарь
- ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ — ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ — содержат в молекуле атом фосфора, связанный с углеродом, напр. триалкилфосфины R3P, кислоты типа RP(OH)2 (R — органический радикал). Большой энциклопедический словарь
