фиксирование фотографического изображения
ФИКСИРОВАНИЕ ФОТОГРАФИЧЕСКОГО ИЗОБРАЖЕНИЯ
закрепление проявленного изображения путем растворения оставшегося в слое галогенида Ag; вторая стадия получения видимого изображения при фотографич. процессе (о первой см. проявление фотографического изображения). Для фиксирования используют водные растворы (или пасты) соед., дающих с ионами Ag+ высокоустойчивые, хорошо растворимые комплексные ионы. К таким соед. относятся цианиды, рода-ниды, тиосульфаты, хлориды щелочных металлов и аммония. Хим. сущность фиксирования заключается в смещении равновесия растворимости AgHal в сторону его полного растворения. Взаимод. можно представить след. реакциями (в скобках указаны константы устойчивости комплексных ионов):
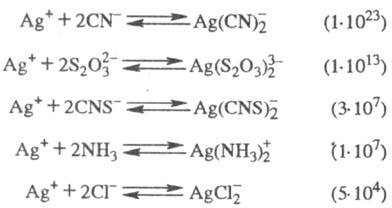
Чем больше константа устойчивости, тем при меньшей концентрации закрепляющего раствора (фиксажа) и с тем большей скоростью м. б. растворен галогенид Ag. Оптимальны в этом отношении растворы цианидов (KCN), но вследствие их токсичности в практич. работе применяют тиосульфаты (обычно Na2S2O3 × 5H2O). По назначению и составу фиксирующие растворы разделяют гл. обр. на простые, кислые, быстрые и дубящие (табл.).
СОСТАВ ФИКСИРУЮЩИХ РАСТВОРОВ*
таблица в процессе добавления
* В граммах в 1 л раствора. ** В мл.
Простой фиксаж вследствие гидролиза тиосульфат-иона имеет щелочную реакцию (рН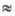 9); при длит. работе из фотослоя в него переходит некоторое количество проявителя, который восстанавливает в слое Ag, что приводит к образованию дихроической вуали на фиксируемом изображении. Поэтому наиб. применение получили кислые фиксирующие растворы с оптимальной кислотностью при pH
9); при длит. работе из фотослоя в него переходит некоторое количество проявителя, который восстанавливает в слое Ag, что приводит к образованию дихроической вуали на фиксируемом изображении. Поэтому наиб. применение получили кислые фиксирующие растворы с оптимальной кислотностью при pH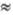 4. В более кислых растворах образуется большое количество тиосерной кислоты, разлагающейся с выделением S и SO2. Добавление сульфита Na регулирует кислотность раствора (по реакции SO2−3 + H+
4. В более кислых растворах образуется большое количество тиосерной кислоты, разлагающейся с выделением S и SO2. Добавление сульфита Na регулирует кислотность раствора (по реакции SO2−3 + H+ HSO−3), что дает возможность вводить в фиксаж для быстрого прекращения проявления такую относительно сильную кислоту как уксусная.
HSO−3), что дает возможность вводить в фиксаж для быстрого прекращения проявления такую относительно сильную кислоту как уксусная.
Кислый фиксаж может вовсе не содержать кислоты, если в раствор вводят пиросульфит К (устар. метабисульфит; K2S2O5). При этом в водном растворе протекают реакции:
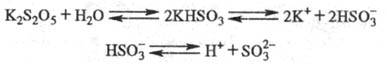
Для создания быстрого кислого фиксажа обычно берут смесь K2S2O5 и Na2SO3, имеющую в растворе высокую кислотно-основную буферную емкость при pH 5. Быстрый фиксаж обычно содержит NH4Cl, а дубящий — к.-л. дубитель, напр. алюмока-лиевые квасцы (см. дубление в фотографии). Иногда составляют комбинир. растворы, сочетающие свойства разл. фиксирующих растворов, напр. быстрый дубящий фиксаж.
5. Быстрый фиксаж обычно содержит NH4Cl, а дубящий — к.-л. дубитель, напр. алюмока-лиевые квасцы (см. дубление в фотографии). Иногда составляют комбинир. растворы, сочетающие свойства разл. фиксирующих растворов, напр. быстрый дубящий фиксаж.
В процессе фиксирования сначала образуется практически нерастворимая прозрачная бесцв. соль NaAgS2O3, не рассеивающая свет; хорошо растворимая соль образуется лишь на послед, стадиях при условии высокой концентрации Na2S2O3 в растворе:
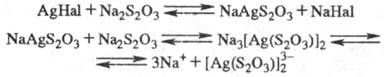
Если фиксирование прекратить на первой стадии, отфик-сированное изображение окажется недостаточно стабильным и не сможет сохраняться длит. время, т. к. NaAgS2O3, оставшись в слое, постепенно разлагается (особенно быстро в теплой и влажной атмосфере) по реакции 2NaAgS2O3 + 2H2O Ag2S + H2S+ 2NaHSO4, что ведет к образованию на изображении желтых и бурых пятен.
Ag2S + H2S+ 2NaHSO4, что ведет к образованию на изображении желтых и бурых пятен.
Отфиксированное изображение тщательно промывают в проточной (или часто сменяемой) воде. Недостаточная промывка даже хорошо отфиксированного изображения может привести при длит. хранении к появлению на нем бурых пятен.
Лит.: Кириллов Н.И., Основы процессов обработки кинофотоматериалов, М., 1977; Джеймс Т.Х., Теория фотографического процесса, пер. с англ., Л., 1980; Чибисов К.В., Общая фотография, М., 1984.
В. И. Шеберстов
