уксусный ангидрид
УКСУСНЫЙ АНГИДРИД (CH3CO)2O
мол. м. 102,09; бесцв. прозрачная подвижная жидкость с резким запахом; т. пл. −73,1 X т. кип. 139,6 °C: 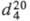 1,0820;
1,0820; 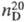 1,3906; tкрит 295,8 °C, ркриг 4,6 МПа; η 0,901 мПа∙с (20 °C), γ 32,65 мН/м (20 °C); μ 9,3∙10−30 Кл∙м;
1,3906; tкрит 295,8 °C, ркриг 4,6 МПа; η 0,901 мПа∙с (20 °C), γ 32,65 мН/м (20 °C); μ 9,3∙10−30 Кл∙м; 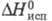 276,7 кДж/моль,
276,7 кДж/моль, 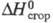 −1804,5 кДж/моль,
−1804,5 кДж/моль, 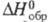 жидкости −624,42 кДж/моль, пара −576,1 кДж/моль;
жидкости −624,42 кДж/моль, пара −576,1 кДж/моль; 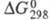 жидкости −489,14 кДж/моль, пара −477 кДж/моль. Раств. в бензоле, диэтиловом эфире, этаноле, CHCl3, CH3COOH, ТГФ, ограниченно — в холодной воде (12 г в 100 г воды), в горячей воде гидролизуется до уксусной кислоты (
жидкости −489,14 кДж/моль, пара −477 кДж/моль. Раств. в бензоле, диэтиловом эфире, этаноле, CHCl3, CH3COOH, ТГФ, ограниченно — в холодной воде (12 г в 100 г воды), в горячей воде гидролизуется до уксусной кислоты (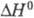 гидролиза −58,45 кДж/моль), гидролиз катализируют кислоты.
гидролиза −58,45 кДж/моль), гидролиз катализируют кислоты.
Обладает хим. свойствами ангидридов карбоновых кислот. С основаниями У. а. дает ацетаты, с HCl и COCl2 при 70–80 °C — ацетилхлорид, со спиртами — сложные эфиры, с тиолами — тиоэфиры, с H2S и Na2S — тиоуксусную кислоту, с аминами — амиды, с альдегидами в присутствии кислых катализаторов — диацетаты, с ароматич. альдегидами в присутствии CH3COOK -β-арилакриловые кислоты. У. а. ацетилирует целлюлозу, превращает высшие жирные кислоты в ангидриды, алифатич. и жир-ноароматич. кетоны в присуг. BF3- в β-дикетоны.
В промышленности У. а. получают разложением CH3COOH в присутствии триэтилфосфата (0,3% по массе) при 680–720 °C и давлении 26,2–52,4 кПа (степень конверсии 80–84%, селективность 87–91 %): 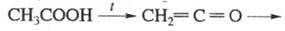
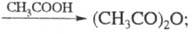 совместно с CH3COOH окислением ацетальдегида в присутствии меднокобальтового катализатора при 50–60 °C (степень конверсии ацетальдегида 16–18%, селективность по сумме продуктов 94–96%).
совместно с CH3COOH окислением ацетальдегида в присутствии меднокобальтового катализатора при 50–60 °C (степень конверсии ацетальдегида 16–18%, селективность по сумме продуктов 94–96%).
Перспективен метод получения У. а. карбонилированием метилацетата в присутствии гомог. родиевых катализаторов.
Используемые ранее методы получения У. а. взаимод. CH3COOH с COCl2 в присутствии AlCl3, а также разложением этилидендиацетата в присутствии ZnCl2 или фосфатов в настоящее время не применяют; метод получения термич. разложением ацетона при 680–740 °C при повыш. давлении применяют ограниченно.
В лаборатории У. а. получают взаимод. CH3COCl с безводным CH3COONa либо CH3COOH с неорг. ангидридами или галогенангидридами (SO2Cl2, SOCl2, COCl2, N2O4, POCl3).
У. а. используют как дегидратирующий и ацетилирующий агент в производстве ацетилцеллюлозы, винилацетата, диметил-ацетамида, лек. веществ (напр., ацетилсалициловой кислоты), красителей, душистых веществ и др.
Раздражает глаза и дыхат. пути, вызывает ожоги кожи. T. всп. 40 °C, т. самовоспл. 389 °C, КПВ 1,21–9,9% (по объему), ПДК в атм. воздухе 0,03 мг/м3.
Мировое производство 1,1–1,3 млн. т/год (1988).
Лит.: Kirk — Othmer encyclopedia, 3 ed., v. 1, N. Y., 1978, p. 151–61.
М. П. Муляева
Значения в других словарях
- Уксусный ангидрид — Ангидрид уксусной кислоты, (CH3CO)2O, бесцветная с резким запахом жидкость, растворимая в бензоле, эфире и др. органических растворителях; tkип 139,5 °С, плотность 1,082 г/см3 (20 °С). У. Большая советская энциклопедия
- УКСУСНЫЙ АНГИДРИД — УКСУСНЫЙ АНГИДРИД — (СН3СО)2О, бесцветная с резким запахом жидкость, tкип 139,9 °С. Применяют для ацилирования, напр. в производстве ацетилцеллюлозы, душистых и лекарственных веществ. Большой энциклопедический словарь
- Уксусный ангидрид — C4H6O3 = (СН3CO)2О — является представителем ангидридов органических жирных кислот формулы СnН2nО2. Он может быть получен в небольших количествах при действии фосфорного ангидрида на уксусную кислоту (Этар, Гал). Энциклопедический словарь Брокгауза и Ефрона
