триазины
ТРИАЗИНЫ
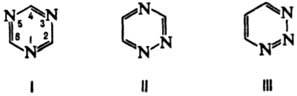
мол. м. 81,08. Различают: 1,3,5-Т., или симметричный (формула I); 1,2,4-Т., или несимметричный (II); 1,2,3-Т., или вицинальный (III).
1,3,5-Т. и его производные. Незамещенный 1,3,5-Т. — бесцветные кристаллы, т. пл. 86 °C, т. кип. 114 °C; хорошо раств. в этаноле, диэтиловом эфире; с кислотами образует соли. В отличие от своих более стабильных производных, неустойчив к действию нуклеофилов: водой легко гидролизуется в формиат аммония; амины вызывают раскрытие цикла с образованием формамидинов и др. соед.; если амин имеет еще к.-л. функц. группу, то вслед за размыканием кольца происходит рециклизация, напр.:
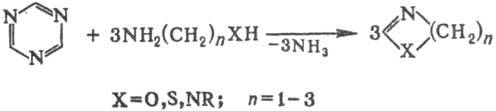
Аналогично при реакции 1,3,5-Т. с о-фенилендиамином получается бензимидазол, с 4,5-диаминопиримидином-пурин, с 4,5-диаминоурацилом-ксантин и т. п.; при действии N2H4∙HCl 1,3,5-Т. превращается в 1,2,4-триазол. С имино-эфирами или амидинами образует алкил(арил)производные 1,3,5-Т.:
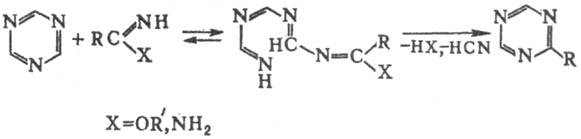
С соед., имеющими активированную группу CH2, 1,3,5-Т. реагирует с образованием замещенных пиримидина:
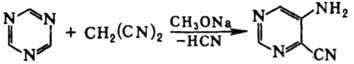
1,3,5-Т. и его производные вступают в диеновый синтез с диенофилами, содержащими электронодонорные заместители, напр.:
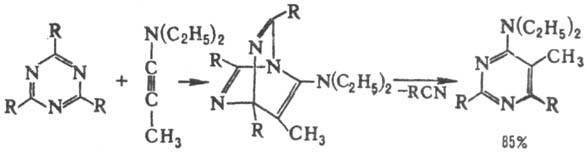
В реакции электроф. замещения 1,3,5-Т. и его производные вступают с трудом: сульфирование и нитрование не удаются вследствие раскрытия цикла; хлорирование до цианурхлорида (формула IV; R = С1) идет в жестких условиях (140–200 °C) с плохим выходом; при бромировании удается получить 2,4-дибром-1,3,5-Т., а также 1,2,4,6-тетрабром-1,2-дигидро-1,3,5-Т.
Общий способ получения 1,3,5-Т. и его наиб. важных 2,4,6-производных -циануровой кислоты (IV; R = ОН), циа-нурхлорида, меламина (IV; R = NH2) и др. — циклотримеризация соед., содержащих группу Cs=N, гл. обр. нитрилов:
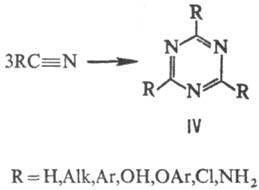
Условия реакции зависят от природы R: чаще всего она идет при нагр. и в присутствии катализаторов (напр., HCl и его комплексов с кислотами Льюиса, иногда оснований); при R = CH=CH2 или OH может идти самопроизвольно; при R = Alk необходимо давление до 100 МПа, однако введение в R электроотрицат. заместителей резко облегчает реакцию. Соед., имеющие две группы C=N, в условиях тримеризации могут образовывать разветвленные полимеры, содержащие триазиновые циклы.
Для формирования триазинового цикла м. б. также использованы соед. общей формулы RC(X)=NH (R = H, Alk, Ar; X = H, OC2H5, OCH2C6H5, Cl, NH2)-иминоэфиры, ами-дины, альдимины и др.; реакция может идти как с отщеплением НХ, так и без него (с образованием производных гексагидро-1,3,5-Т.).
Незамещенный 1,3,5-Т. обычно получают конденсацией CH3COONH4 с триэтилортоформиатом. Конденсацией аминов RNH2 (или алканоламинов) с CH2O синтезируют производные гексагидро-1,3,5-Т. (V), каталитич. тримеризацией изоцианатов RN=C=O-изоцианураты (VI):
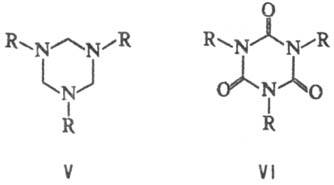
Производные гексагидро-1,3,5-Т. — антисептики (напр., V; R = Alk, гидроксиалкил), бактерициды, отбеливатели; 1,3,5-тринитро-1,3,5-триазациклогексан (V; R = NO2), или гексоген,- бризантное ВВ. Аллилцианурат (V; R = = OCH2CH=CH2) и аллилизоцианурат (VI; R = = CH2CH=CH2)-модификаторы в производстве меламино-формальдегидных смол. Мн. кетопроизводные 1,3,5-Т. — физиологически активные вещества; напр., рибофуранозид 4-амино-1,3,5-триазин-2-она (5-азацитидин) проявляет противоопухолевую и противолейкемич. активность; 6-диметиламино-1 — метил-3-циклогексил-1,3,5-триазин-2,4-дион (гексазинон) — гербицид.
Несимметрично замещенные производные 1,3,5-Т., которые не м. б. получены методами тримеризации, синтезируют из соответствующих нециклич. соед. (бигуанидов, цианамиди-нов, изоцианатов и др.). Некоторые фторорг. производные получаютпо схеме:
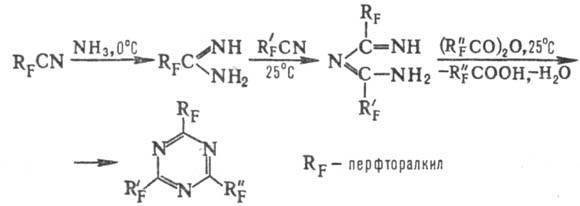
Используя в подобных реакциях вместо нитрилов динитри-лы, синтезируют производные формулы VII, а также полимеры формулы VIII, отличающиеся высокой термич. и хим. стабильностью:
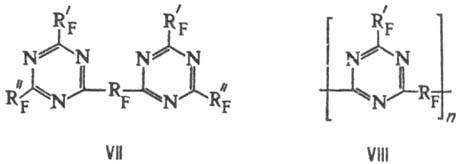
Первые-смазки и гидравлич. жидкости с температурой кипения до 400 °C, вторые-высокостойкие герметики.
2,4,6-Замещенные 1,3,5-Т. получают гл. обр. из цианур-хлорида, последовательно заменяя в нем один, два или три атома Cl (во все более жестких условиях) на одинаковые или разные нуклеоф. группы. Некоторые из полученных таким путем разл. производных — красители для целлюлозных волокон, оптич. отбеливатели, антисептики; мн. диаминопро-изводные-гербициды-атразин, прометрин, симазин, хлор-сульфурон и др.; инсектициды; 2,4,6-триазидо-1,3,5-Т.-циа-нуртриазид — инициирующее ВВ.
1,2,4,-Т. и его производные. Незамещенный 1,2,4-Т. — блед-но-желтое масло, т. пл. 16–17,5 °C, т. кип. 156 °C/740 мм рт. ст., 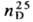 1,5149; раств. в органических растворителях и разбавленных кислотах, плохо — в воде. Производные 1,2,4-Т. термически стабильны; при окислении надкислотами превращаются в 1,2,4-триазин-5-оны или 1,2,4-триазин-5,6-дионы (если положение 5 занято — в l-N-оксиды); при восстановлении Zn в CH3COOH — в 1,2-дигидро-1,2,4-Т. и далее (с сужением цикла) — в индазолы. Легко вступают в диеновый синтез, присоединяя диенофилы обычно по положениям 3 и 6 (иногда 2 и 5), напр.:
1,5149; раств. в органических растворителях и разбавленных кислотах, плохо — в воде. Производные 1,2,4-Т. термически стабильны; при окислении надкислотами превращаются в 1,2,4-триазин-5-оны или 1,2,4-триазин-5,6-дионы (если положение 5 занято — в l-N-оксиды); при восстановлении Zn в CH3COOH — в 1,2-дигидро-1,2,4-Т. и далее (с сужением цикла) — в индазолы. Легко вступают в диеновый синтез, присоединяя диенофилы обычно по положениям 3 и 6 (иногда 2 и 5), напр.:
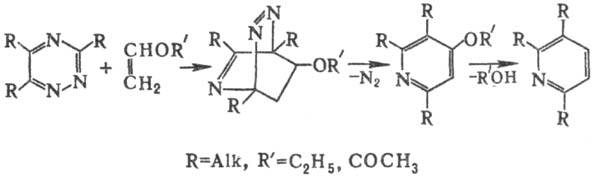
Осн. способы получения 1,2,4-Т. и его производных-конденсация α-дикетонов с амидразонами, семикарбазида-ми, тиосемикарбазидами, аминогуанидинами или гидрази-дами кислот (при замыкании цикла аммиаком), напр.:
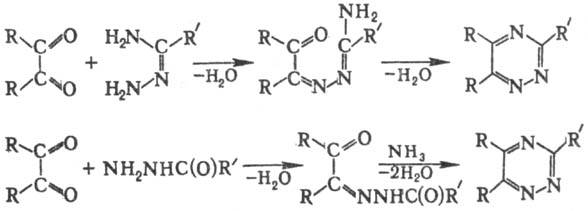
Наряду с α-дикетонами для подобных синтезов используют также α-кетокислоты, α-галогенкетоны, ацилциа-ниды.
Производные 1,2,4-Т. — гербициды (напр., метрибузин, ме-тамитрон), противобактериальные средства, соед. с противоопухолевой активностью (1,2,4-триазин-3,5-дион, 6-метил-1,2,4-триазин-3,5-дион и их нуклеозиды); 3- и 5-замещен-ные- реагенты для аналит. определения Fe, Co, Ni, Zn, Cr и др. металлов.

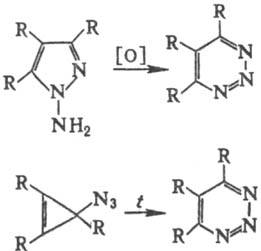
1,2,3-Т. и его производные. Незамещенный 1,2,3-Т. — бесцветные кристаллы, т. пл. 69,5–71 °C, возгоняется в вакууме. 1,2,3-Т. и его производные при комнатной температуре устойчивы к воде, кислотам и основаниям. При нагр. гидролизуются до 1,3-дике-тонов; надкислотами окисляются в 1(или 3)-N-оксиды; LiAlH4 восстанавливает их в дигидропроизводные. Три-алкилзамещенные 1,2,3-Т. при термолизе и фотолизе чаще всего расщепляются с образованием N2, алкина и нитрила. Получают 1,2,3-Т. и его производные окислением N-ами-нопиразолов пероксидами или термич. перегруппировкой циклопропенилазидов в мягких условиях:
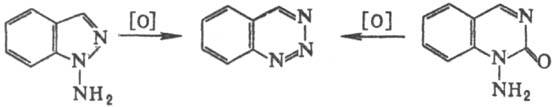
Бензо-1,2,3-Т. и его производные получают циклизацией 2-аминобензиламинов, 2-аминобензамидов или 2-амино-бензгидразидов под действием HNO2, а также окислением N-аминоиндазолов или N-амино-2-хиназолинонов:
Некоторые производные 1,2,3-Т. — ингибиторы коррозии, инсектициды.
Лит.: Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 185–94; Мельников Н. Н., Пестициды. Химия, технология и применение, М., 1987, с. 639–61; Neunhoeffer H., WileyP.F., Chemistry of 1,2,3-triazines and 1,2,4-tria-zines, tetrazines and pentazines, N. Y., 1978; Comprehensive heterocyclic chemistry, ed. by A. Katritzky, Ch.W. Ress, v. 3, pt 2B, Oxf., 1984, p. 369–530; Hearn M.J., Levy F., "Organic preparations and procedures int.", 1984, v. 16, № 3–4, p. 199–277.
Г. С. Швиндлерман
Значения в других словарях
- Триазины — Шестичленные гетероциклические соединения, содержащие три атома азота в цикле. Известны главным образом замещенные Т. всех трёх возможных типов: вицинальные 1, 2, 3-Т. (I), несимметричные 1, 2, 4-Т. (II) и симметричные 1, 3, 5-Т. (III):... Большая советская энциклопедия
- Триазины — Химические соединения, характеризующаяся тем, что в своем составе содержат шестиатомное кольцо, состоящее из 3 атомов азота и 3 ат. углерода. Энциклопедический словарь Брокгауза и Ефрона
