спин-орбитальное взаимодействие
СПИН-ОРБИТАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ
взаимодействие между магн. моментами, связанными со спиновыми и орбитальными моментами количества движения электронов и ядер в квантовой системе — атоме, молекуле, кристалле и т. п. С.-о.в. обусловливает вклад в энергию системы, которому отвечают три слагаемых гамильтониана в уравнении Шрёдингера. Первое слагаемое связано с магн. полем, возникающим при перемещении электрона относительно ядра в электрич. поле ядра и действующим на спиновый магн. момент; второе — с магн. полем, возникающим при движении данного электрона в электрич. поле всех остальных электронов, третье — с взаимод. спинового магн. момента данного электрона с магн. полями, создаваемыми всеми остальными электронами при их движении.
Для электронов i и j с радиусами-векторами ri и rj и импульсами (Моментами количества движения) pi и pj их С.-о. в. друг с другом и с ядрами а, заряды которых равны Zα (в единицах элементарного заряда е) и радиусы-векторы Rα, приводит к дополнит. вкладу в гамильтониан системы, состоящему из след. трех сумм:
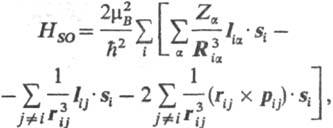
где ђ и mВ-постоянная Планка и магнетон Бора соотв.; Riα = ri-Rα, rij=ri — rj (rij-длина вектора rij); Iiα = = (ri — Rα)x pi — момент количества движения i-го электрона относительно начала системы координат на ядре α, рij = =pi — pj, Iij = rij x pi, si-оператор спина i-го электрона.
Из этих сумм, как правило, осн. вклад в энергию системы дает первая, тогда как вторая и третья (их обычно наз. "взаимодействия спин-другая орбиталь") дают значительно меньшие вклады. Если ими пренебречь, оператор С.-о. в. сводится к следующему:
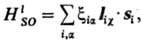
где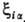 - функции координат электронов и ядер, а также зарядов ядер. Эти функции пропорциональны
- функции координат электронов и ядер, а также зарядов ядер. Эти функции пропорциональны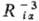 , поэтому при их усреднении по всем возможным положениям электронов наиб. существенны те конфигурации системы, при которых электроны находятся вблизи ядер. Если волновая функция молекулы образована из мол. орбиталей в форме линейной комбинации атомных орбиталей (см. ЛКАО-приближение), то в средние величины
, поэтому при их усреднении по всем возможным положениям электронов наиб. существенны те конфигурации системы, при которых электроны находятся вблизи ядер. Если волновая функция молекулы образована из мол. орбиталей в форме линейной комбинации атомных орбиталей (см. ЛКАО-приближение), то в средние величины 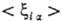 основной вклад дают интегралы
основной вклад дают интегралы 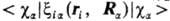 , вычисляемые с атомными орбиталями cα, центрированными на ядре α (см. орбиталь). Обычно функции
, вычисляемые с атомными орбиталями cα, центрированными на ядре α (см. орбиталь). Обычно функции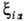 (ri, Rα) для атомов заменяют на некоторые постоянные, зависящие от главного n и орбитального l квантовых чисел
(ri, Rα) для атомов заменяют на некоторые постоянные, зависящие от главного n и орбитального l квантовых чисел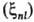 ; их наз. постоянными С.-о.в. В водородоподобных атомах
; их наз. постоянными С.-о.в. В водородоподобных атомах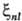 пропорциональна Z4 и обратно пропорциональна n3. В многоэлектронных атомах происходит экранирование ядра электронами и зависимость постоянной С.-о.в. от Z и n становится не столь резко выраженной и функционально более сложной. Тем не менее и в том и в другом случае С.-о.в. наиб. велико для электронов внутр. оболочек тяжелых атомов, а у молекул-для внутр. оболочек атомных остовов, что позволяет характеризовать величины С.-о.в. и для молекул с помощью атомных постоянных
пропорциональна Z4 и обратно пропорциональна n3. В многоэлектронных атомах происходит экранирование ядра электронами и зависимость постоянной С.-о.в. от Z и n становится не столь резко выраженной и функционально более сложной. Тем не менее и в том и в другом случае С.-о.в. наиб. велико для электронов внутр. оболочек тяжелых атомов, а у молекул-для внутр. оболочек атомных остовов, что позволяет характеризовать величины С.-о.в. и для молекул с помощью атомных постоянных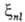
С.-о.в. приводит к расщеплению вырожденных уровней мультиплета, что проявляется в атомных и мол. спектрах как тонкая структура. Так, вследствие С.-о.в. низший возбужденный уровень атомов щелочных металлов расщепляется на два: 2P1/2 и 2Р3/2, где индекс внизу указывает квантовое число полного момента количества движения электрона на внеш. оболочке пр. Для Na (Z = 11, n = 3) это расщепление составляет 17,2см−1, для К (Z=19, n = 4) 57,7 см −1, для Cs (Z =55, n = 6) 554,1 см −1. У атомов галогенов расщепление уровней для np-электронов еще больше, а постоянные С.-о.в. таковы: для F 272 см −1, для Cl 587 см −1, для I 5060 см −1. При достаточно сильном С.-о.в. понятие мультиплетности термов вообще теряет смысл и рассматривается лишь полный момент количества движения электронов, а не спин и орбитальный момент в отдельности. Запрет на квантовые переходы между уровнями с разной мультиплетностью при наличии С.-о.в. снимается, что приводит, напр., к фосфоресценции — излучат. переходу из состояний с временами жизни, обратно пропорциональными квадратам матричных элементов оператора С.-о.в., и к ин-теркомбинац. конверсии (см. люминесценция, фотохимические реакции). Поскольку время фосфоресценции зависит не только непосредственно от времени жизни "фосфоресцирующего" состояния рассматриваемых молекул, но и от среды, в которой они находятся, для учета этой зависимости вводят представление о межмолекулярном С.-о.в. У двухатомных и линейных многоатомных молекул соотношение С.-о.в. и др. взаимодействий, напр. спин-вращательного, позволяет выделять разл. случаи связи спинов, орбитальных и др. моментов (см. хунда случаи связи), что дает возможность для каждого случая связи проводить специфич. классификацию квантовых состояний молекулы.
В выражении для HSO не представлен член, отвечающий взаимод. ядерного магн. спинового момента и орбитального момента электронов, 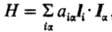 , где аiα(Riα) =
, где аiα(Riα) =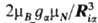 , gα-g-фактор ядра α, mN- ядерный магнетон, Iα- ядерный спин. Связанное с этим членом расщепление уровней заметно меньше, чем обусловленное С.-о.в.; напр., для электронного состояния 2Р1/2 атома Na величина aiα составляет 94,5 МГц, а для состояния 2Р3/2-19,1 МГц, т. е. примерно 0,003–0,001 см−1. Обычно член Я выделяют (вместе с др. членами того же порядка малости) в орбитальное сверхтонкое взаимодействие, или сверхтонкое ядерное магн. взаимодействие, проявляющееся в спектрах ЭПР (см. электронный парамагнитный резонанс).
, gα-g-фактор ядра α, mN- ядерный магнетон, Iα- ядерный спин. Связанное с этим членом расщепление уровней заметно меньше, чем обусловленное С.-о.в.; напр., для электронного состояния 2Р1/2 атома Na величина aiα составляет 94,5 МГц, а для состояния 2Р3/2-19,1 МГц, т. е. примерно 0,003–0,001 см−1. Обычно член Я выделяют (вместе с др. членами того же порядка малости) в орбитальное сверхтонкое взаимодействие, или сверхтонкое ядерное магн. взаимодействие, проявляющееся в спектрах ЭПР (см. электронный парамагнитный резонанс).
Лит. см. при ст. спин.
Н. В. Степанов
Значения в других словарях
- СПИН-ОРБИТАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ — Взаимодействие ч-ц, зависящее от величины и взаимной ориентации их орбитального и спинового моментов кол-ва движения и приводящее к т. н. тонкой структуре уровней энергии системы. С.-о. в.— релятив. Физический энциклопедический словарь
- Спин-орбитальное взаимодействие — Взаимодействие частиц, зависящее от величин и взаимной ориентации их орбитального и спинового моментов количества движения и приводящее к т. н. тонкому расщеплению уровней энергии системы (см. Тонкая структура). С.-о. в. — релятивистский эффект (См. Большая советская энциклопедия
- СПИН-ОРБИТАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ — СПИН-ОРБИТАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ — взаимодействие частиц, зависящее от величин и взаимной ориентации их спинового и орбитального моментов; обусловливает тонкую структуру уровней энергии системы. Большой энциклопедический словарь
