селективные ионообменные смолы
СЕЛЕКТИВНЫЕ ИОНООБМЕННЫЕ СМОЛЫ (комплексообразующие ионообменные смолы)
ионообменные смолы, содержащие группы, способные образовывать координац. связи с поглощаемыми из растворов ионами или молекулами. Отличаются высокой селективностью, определяемой сродством комплексообразующей группы (лиганда) к сорбируемым ионам и структурой полимера (свойства полимерного каркаса, пористость, пространственное расположение групп). Наиб. селективны С. и с., образующие с катионами металлов устойчивые внутрикомплексные соед. — хелаты.
Сравнение селективности С. и. с. осуществляют по коэф. распределения k = ссм/ср, где ссм и ср — концентрация вещества в смоле и исходном растворе; при этом большое значение имеют сольватац. характеристики сорбируемых ионов и их концентрация. Ряды селективности С. и. с. для разл. ионов существенно отличаются от рядов селективности др. ионообменных смол.
Наиб. активные лиганды-карбоксильные, фосфонатные, иминодиацетатные, глиоксиматные, тиомочевинные, пири-динсодержащие группы, образующие, напр., след. комплексные соединения (М-металл):
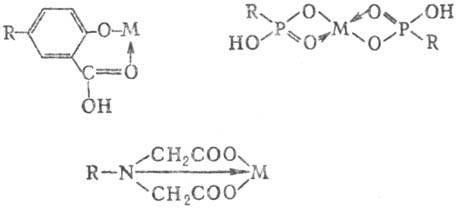
С. и. с. получают гл. обр. поликонденсацией и полимеризацией, а также методом полимераналогичных превращений, чаще всего путем хлорметшшрования полимерной матрицы с послед. введением комплексообразующих групп. Наиб. применение находят поликонденсац. амино-альдегидные (меламино-формальдегидные), мочевино-формальдегидные, феколо-формальдегидные и резорцино-формаль-дегидные смолы, а также полимеризационные С. и. с. на основе сополимеров стирола или аминостирола с дивинилбензолом, тройного сополимера стирола, малеинового ангидрида и дивинилбензола, полиэпихлоргидрина.
Осн. применение С. и. с. — извлечение металлов (гл. обр. тяжелых) из растворов пром. сточных вод. В извлечении Cr наиб. селективны сополимеры эпихлоргидрина с пиридином, Со и Ni-смолы на основе полиаминов, Cr, Zn и Ti-амино-фосфоновые смолы на основе эфиров фосфорной кислоты, аминов и формальдегида. Аминокарбоновые смолы на основе стирола обладают наиб. селективностью гл. обр. к металлам II группы; порядок селективности:
Sr2+ < Ва2+ < Ca2+ < Mg2+ < Со2+ < Zn2+ < Cd2+ < Ni2+ < Pb2+ < 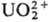 < Cu2+ < Hg2+.
< Cu2+ < Hg2+.
Др. области применения С. и. с. — анализ и концентрирование микроэлементов из растворов. Комплексы С. и. с. с металлами-катализаторы гидрирования непредельных соед., кетонов и спиртов, изомеризации, полимеризации, гидроформилирования и др.
Лит.: Херинг Р., Хелатообразующие ионообменники, пер. с нем., М., 1971; Энциклопедия полимеров, т. 3, М., 1977, с. 1081–87; Салдадзе К. М., Копылова В. Д., Комплексообразующие иониты (комплекснты), М., 1980; Копылова В. Д., Астанина А. Н., Ионитные комплексы в катализе, М., 1987.
Г. К. Салдадзе
