пропиленкарбонат
ПРОПИЛЕНКАРБОНАТ (1,2-пропиленкарбонат, 4-метил-1,3-диоксолан-2-он, формула I)
мол. м. 102,09; бесцветная жидкость со слабым эфирным запахом; т. пл. −48,8 °C, т. кип. 241,7 С; 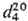 1,2057;
1,2057; 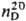 1,4209; η 0,46 мПа∙с; γ 41,2 мН/м; ц 16,48∙10−30 Кл∙м; давление пара, ГПа: 48,7 (140 °C), 118,1 (164 °C), 232,7 (185 °C), 291,0 (193 °C), 600,0 (220 °C);
1,4209; η 0,46 мПа∙с; γ 41,2 мН/м; ц 16,48∙10−30 Кл∙м; давление пара, ГПа: 48,7 (140 °C), 118,1 (164 °C), 232,7 (185 °C), 291,0 (193 °C), 600,0 (220 °C); 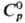 167 Дж/(моль∙К);
167 Дж/(моль∙К); 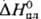 9,6 кДж/моль, ΔHисп 53,2 кДж/моль (170 °C),
9,6 кДж/моль, ΔHисп 53,2 кДж/моль (170 °C), 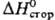 −1818 кДж/моль. П. раств. в этаноле, диэтиловом эфире, ацетоне, ароматич. углеводородах, карбоновых кислотах; не раств. в алифатич. углеводородах, CS2; неограниченно смешивается с водой при температуре выше 80 °C, в холодной воде раств. 17,5% по массе. П. растворяет мн. полимеры, полиэфирные волокна и смолы, напр. полиакрилонитрил, ПВХ, нитрат и ацетат целлюлозы, полиэтилентерефталат. Образует азеотропную смесь с про-пиленгликолем, которую разделяют ректификацией с добавлением ароматических углеводородов.
−1818 кДж/моль. П. раств. в этаноле, диэтиловом эфире, ацетоне, ароматич. углеводородах, карбоновых кислотах; не раств. в алифатич. углеводородах, CS2; неограниченно смешивается с водой при температуре выше 80 °C, в холодной воде раств. 17,5% по массе. П. растворяет мн. полимеры, полиэфирные волокна и смолы, напр. полиакрилонитрил, ПВХ, нитрат и ацетат целлюлозы, полиэтилентерефталат. Образует азеотропную смесь с про-пиленгликолем, которую разделяют ректификацией с добавлением ароматических углеводородов.
П. обладает свойствами циклич. карбонатов органических. При действии оснований или кислот (в меньшей степени) гидро-лизуется до 1,2-пропиленгликоля и CO2. Со спиртами, в зависимости от условий, образует простые эфиры пропи-ленгликоля или полипропиленгликолей; с многоатомными спиртами вступает в реакцию переэтерификации. Гид-роксиалкилирует карбоновые кислоты, фенолы, ароматич. амины; в реакции с дисахаридами, пектинами, белками образуются соед., обладающие поверхностной активностью.
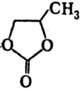
С NH3, алифатич. аминами и гидразином П. реагирует без выделения CO2 с образованием пропиленгликолькарбама-тов (полупродуктов для синтеза оксазолидонов и полиуретанов):
Поликонденсация П. с дикарбоновыми кислотами, многоатомными спиртами, циклич. алкиленаминами, формальдегидом приводит к линейным сополимерам (в т. ч. полиуретанам и поликарбонатам).
При термокаталитич. расщеплении П. в присутствии галогени-дов щелочных металлов или тетраалкиламмония образуются пропиленоксид и CO2; протонодонорные вещества ускоряют реакцию.
Получают П. конденсацией пропиленгликоля с производными угольной кислоты (фосгеном, эфирами хлоругольной кислоты, диалкилкарбонатами); взаимод. пропиленхлоргидрина с Na-солью алкилкарбонатов или с концентрир. растворами неорг. карбонатов; конденсацией пропиленоксида с трихлор-уксусной кислотой.
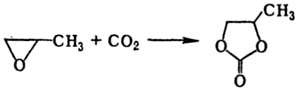
В промышленности П. синтезируют из пропиленоксида и CO2 в присутствии галогенидов металлов или тетраалкиламмония при 150–200 °C и давлении 5–10 мПа:
Реакцию можно проводить в присутствии металлоорг. соед. и азотистых оснований.
П. — растворитель полимеров в хим. и текстильной промышленности; исходное вещество для синтеза мономеров и полимеров, пластификаторов, модификаторов, средств защиты растений; исходный или промежуточный продукт в производстве 1,2-пропиленгликоля; высокополярный электролит (хим. источники тока, конденсаторы); абсорбент CO2, H2S и COS из прир. и синтетич. газов; экстрагент ароматических углеводородов; осушитель газообразного формальдегида; компонент формовочных смесей в литейной промышленности.
П. не вызывает коррозию, малотоксичен. Т. всп. 128 °C, т. самовоспл. 400 °C.
Объем производства в России 300 т/год (1990).
Лит.: Коренькова О. П., Кваша В. Б., "Хим. пром.", 1961, № 9, с. 625–30; Шапиро А. Л. [и др.], "Химия и технология топлив и масел", 1971, № 5. с. 14–18; Алкиленкарбонаты. Сб. научных трудов ВНИИНефтехим, Л., 1975; Pcppel W.I., "Ind. and Eng. Chem.", 1958, v. 50, p. 767–70.
А. М. Рыженков
