первое начало термодинамики
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
один из осн. законов термодинамики; является законом сохранения энергии для систем, в которых существ, значение имеют тепловые процессы (поглощение или выделение тепла). Согласно П. н. т., термодинамич. система (напр., пар в тепловой машине) может совершать работу только за счет своей внутр. энергии или к.-л. внеш. источника энергии. П. н. т. часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из некоторого источника.
П. н. т. вводит представление о внутренней энергии системы как функции состояния. При сообщении системе некоторого количества теплоты Q происходит изменение внутр. энергии системы DU и система совершает работу А:
DU = Q + А.
П. н. т. утверждает, что каждое состояние системы характеризуется определенным значением внутр. энергии U, независимо от того, каким путем приведена система в данное состояние. В отличие от значений U значения A и Q зависят от процесса, приведшего к изменению состояния системы. Если начальное и конечное состояния α и b бесконечно близки (переходы между такими состояниями наз. инфи-нитезимальными процессами), П. н. т. записывается в виде:
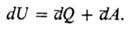
Это означает, что бесконечно малое изменение внутр. энергии dU является полным дифференциалом функции состояния, т. е. интеграл 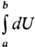 = Ub — Ua , тогда как бесконечно малые количества теплоты
= Ub — Ua , тогда как бесконечно малые количества теплоты 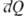 и работы
и работы 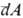 не являются дифференц. величинами, т. е. интегралы от этих бесконечно малых величин зависят от выбранного пути перехода между состояниями а и b (иногда их наз. неполными дифференциалами).
не являются дифференц. величинами, т. е. интегралы от этих бесконечно малых величин зависят от выбранного пути перехода между состояниями а и b (иногда их наз. неполными дифференциалами).
Из общего количества работы, производимой системой объема У, можно выделить работу обратимого изотермич. расширения под действием внеш. давления pe, равную peV, и все остальные виды работы, каждый из которых можно представить произведением некоторой обобщенной силы 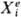 , действующей на систему со стороны окружающей среды, на обобщенную координату xi , изменяющуюся под воздействием соответствующей обобщенной силы. Для инфинитези-мального процесса
, действующей на систему со стороны окружающей среды, на обобщенную координату xi , изменяющуюся под воздействием соответствующей обобщенной силы. Для инфинитези-мального процесса
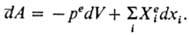
П. н. т. позволяет рассчитать макс. работу, получаемую при изотермич. расширении идеального газа, изотермич. испарении жидкости при пост. давлении, устанавливать законы адиабатич. расширения газов и др. П. н. т. является основой термохимии, рассматривающей системы, в которых теплота поглощается или выделяется в результате хим. реакций, фазовых превращ. или растворения (разбавления растворов).
Если система обменивается со средой не только энергией, но и веществом (см. открытая система), изменение внутр. энергии системы при переходе из начального состояния в конечное включает помимо работы А и теплоты Q еще и т. наз. энергию массы Z. Бесконечно малое количество энергии массы в инфинитезимальном процессе определяется хим. потенциалами mk каждого из компонентов системы:  =
=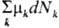 , где dNk — бесконечно малое изменение числа молей k-гo компонента в результате обмена со средой.
, где dNk — бесконечно малое изменение числа молей k-гo компонента в результате обмена со средой.
В случае квазистатич. процесса, при котором система в каждый момент времени находится в равновесии с окружающей средой, П. н. т. в общем виде имеет след. мат. выражение:
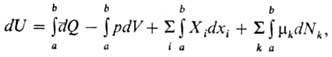
где p и mk равны соответствующим значениям для окружающей среды (индекс е при Xi обычно опускают). Это выражение используется в прикладной термодинамике применительно к системам, в которых производится работа хим., электрич., магн. и т. п. сил.
П. н. т. было сформулировано в сер. 19 в. в результате работ Ю. P. Майера, Дж. Джоуля и Г. Гельмгольца. Вместе со вторым началом термодинамики оно составляет основу классич. термодинамики. В 60-х гг. 20 в. сформулирован фундам. закон устойчивого равновесия систем (Д. Хацо-пулос, Д. Кинан, P. Хейвуд), следствиями которого являются как П. н. т., так и второе начало.
Лит.: Кубо Р., Термодинамика, пер. с англ., М., 1970; Гельфер Я. M., История и методология термодинамики и статистической физики, 2 изд., М., 1981; Хейвуд Р., Термодинамика равновесных процессов, пер. с англ., М., 1983; Alberty R. A., Physical chemistry, 7 ed, N. Y., 1987.
Г. П. Гладышев
Значения в других словарях
- ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ — Один из двух осн. законов термодинамики, представляет собой закон сохранения энергии для систем, в к-рых существ. значение имеют тепловые процессы. П. н. т. было сформулировано в сер. 19 в. в результате работ нем. учёного Ю. Р. Майера, англ. физика Дж. Физический энциклопедический словарь
- Первое начало термодинамики — Один из двух основных законов термодинамики (См. Термодинамика), представляет собой закон сохранения энергии для систем, в которых существенное значение имеют тепловые процессы. П. н. т. было сформулировано в середине 19 в. в результате работ Ю. Большая советская энциклопедия
- ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ — ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ — одно из основных положений термодинамики, являющееся по существу законом сохранения энергии в применении к термодинамическим процессам: Q=?U + A, где Q — сообщаемое термодинамической системе (напр. Большой энциклопедический словарь
