окислители
ОКИСЛИТЕЛИ
вещества, молекулы которых принимают электроны или отдают кислород в окислительно-восстановит. реакциях. Относит. окислит. способность веществ определяется путем сравнения изменения энергий Гиббса при реакциях веществ с одним и тем же восстановителем (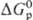 ), а в случае реакций между простыми веществами-сравнением DG0обр продуктов окисления простого вещества. Чем больше абс. величина
), а в случае реакций между простыми веществами-сравнением DG0обр продуктов окисления простого вещества. Чем больше абс. величина 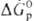 или
или 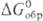 , тем более активным О. является данное вещество. Так, при обычных условиях в реакциях Ca + Х2 → СаХ2 (где X = Cl, F), Ca + 1/2O2, → CaO хлор — более активный О., чем О,, но менее активный, чем F2 (
, тем более активным О. является данное вещество. Так, при обычных условиях в реакциях Ca + Х2 → СаХ2 (где X = Cl, F), Ca + 1/2O2, → CaO хлор — более активный О., чем О,, но менее активный, чем F2 (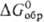 CaO -603,9, CaCl2 -749,3, CaF2 −1168,4 кДж/моль).
CaO -603,9, CaCl2 -749,3, CaF2 −1168,4 кДж/моль).
В случае электрохим. реакций или реакций в растворах для сравнения окислит. способности веществ используют стандартный электродный потенциал (пропорционален 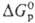 ). Окислит. свойства веществ в растворах зависят от величины pH раствора.
). Окислит. свойства веществ в растворах зависят от величины pH раствора.
Сильнейшие О. — атомарные F, О, Cl, некоторые своб. радикалы, сильные O.-F2, O2, O3, Cl2, фториды кислорода, галогенов, благородных газов, фториды, оксиды и хлориды азота, фториды и оксиды переходных металлов в высоких степенях окисления, олеум, некоторые кислоты (конц. HNO3, HClO4), соли (напр., гипохлориты, K2Cr2O7, KMnO4) и комплексные соед., пероксиды. Некоторые вещества проявляют окислит. свойства в плазменном состоянии (напр., CF4 или при фотохим. активации (напр., SF6).
О. применяют: при сжигании орг. топлива; для окислит. выплавки металлов из сульфидных руд; для удаления примесей из металлов и сплавов; в орг. и неорг. синтезе; в жидких ракетных топливах и смесевых ВВ; для отбеливания шерсти, хлопка, целлюлозы, шелка; для хим. травления металлов и полупроводников; в хим. источниках тока в составе катодов и др.
Э. Г. Раков
Значения в других словарях
- Окислители — Так называются обыкновенно в химии вещества, более или менее богатые кислородом и притом сравнительно мало прочные и, в силу этой своей незначительной прочности, способные, при подходящих условиях... Энциклопедический словарь Брокгауза и Ефрона
