диоксинафталины
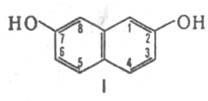
ДИОКСИНАФТАЛИНЫ (дигидроксинафталины) C10H6(OH)2
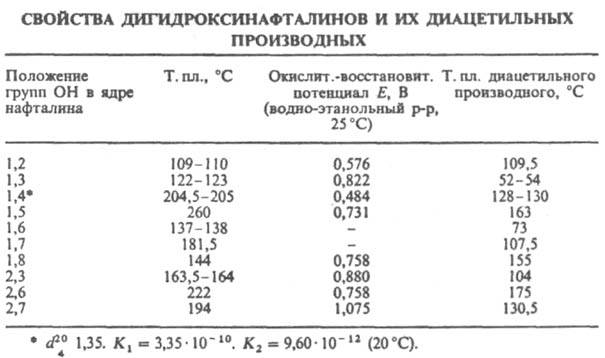
мол. м. 160,16; бесцветные кристаллы (см. табл.); плохо раств. в холодной воде, напр., растворимость при 20 °C в 100 г H2O 1,3-, 1,5- и 2,7-Д. (формула I) — 1,8, 0,016 и 0,108 г (14 °C) соотв.; хорошо раств. в спиртах, диэтиловом эфире, водных растворах щелочей (щелочные растворы на воздухе быстро темнеют из-за образования продуктов окисления).
Д. обладают всеми хим. свойствами, характерными для фенолов. Легко образуют с (CH3СО)2O или CH3COCl устойчивые, с четкими температурами плавления ацетильные производные, с помощью которых их идентифицируют. С диметилсульфатом дают диметиловые эфиры. Легко окисляются. Так, 1,2- и 1,4-Д. окисляются FeCl3 или PbO2 в эфире или бензоле до 1,2- и 1,4-нафтохинонов соотв., воздухом в водно-спиртовой среде в присутствии NaOH или KOH — до 2-гидрокси-1,4-нафтохинона.
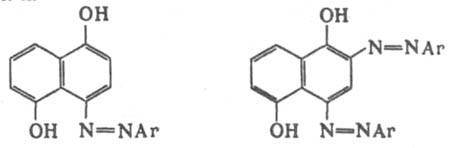
1,8-Д. воздухом в аналогичных условиях окисляется до 5-гидрокси-1,4-нафтохинона (юглона), 2,6-Д. действием PbO2 в среде бензола — в 2,6-нафтохинон (амфи-нафтохинон). При нагр. с (NH4)2SO3 или водным раствором NH3 под давлением OH-группы замещаются на NH2, причем замещение происходит легче в β-положение, чем в α-положение: при 120–150 °C образуются аминогидроксинафталины, при 200–240 °C — диаминонафталины (реакция Бухерера). Д. карбоксилируются действием CO2 под давлением при 140–250 °C в присутствии щелочей (реакция Кольбе — Шмитта). 1,4-Д. конденсируется с малеиновым ангидридом при 220 °C (кат. — AlCl3, NaCl) в хинизарин. Д. сочетаются с солями диазония с образованием азокрасителей, напр., из 1,5-Д. получают 4-азо- и 2,4-дисазокрасители:
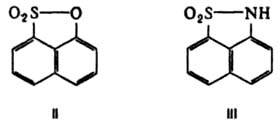
В промышленности 1,5-, 1,6-, 2,6- и 2,7-Д. получают щелочным гидролизом соответствующих нафталиндисульфокислот конц. раствором NaOH при 220–320 °C, 1,3- и 1,7-Д. — из 1-нафтол-3-сульфокислоты и 2-нафтол-8-сульфокислоты соотв.; 2,3-Д. — из 2-нафтол-3,6-дисульфокислоты с послед. десульфированием 2,3-дигидроксинафталин-6-сульфокислоты 30%-ной H2SO4 при 150–200 °C; 1,8-Д. — из 1,8-нафтсультона (формула II) или 1,8-нафтсультама (III):
1,2- и 1,4-Д. синтезируют восстановлением соответствующих нафтохинонов. Цветные реакции: при взаимодействии с раствором FeCl3 1,6-Д. дает медно-красный осадок, 1,8-Д. — темно-зеленую окраску, 2,3-Д. — темно-синюю. 1,5-Д. (азурол) — азосоставляющая в производстве азокрасителей, напр., из него получают о-оксиазокрасители, образующие на шерсти после хромирования прочные черные окраски (диамант черный П и др.); азурол применяют также для синтеза 1,5-нафтилендиизоцианата. 1,3-, 1,7-, 1,6-, 1,8-Д. — компоненты цветных фотоматериалов. 2,3-Д. — азосоставляющая в диазотипии, а также реагент для экстракционно-спектрофотометрич. определения Fe(III), Mo, Ti, V. Нитрозопроизводные 1,5-, 1,6-, 2,7-Д., в молекулах которых группа NO находится в орто-положении к OH-группе, образуют лаки с солями Cr(III) и Fe(III), устойчивые к действию света, растворов кислот и щелочей. 1,6-Д. — промежут. продукт в производстве фотопроявителей.
Лит.: Доналдсон Н., Химия и технология соединений нафталинового ряда, пер. с англ., М., 1963, с. 366–77.
Н. Б. Карпова
