дейтерий
ДЕЙТЕРИЙ (тяжелый водород) (от греч. deuteros — второй) D
стабильный изотоп водорода с мас. ч. 2, ат. м. 2,01416219. Ядро атома Д. — дейтрон состоит из одного протона и одного нейтрона, энергия связи между ними 2,23 МэВ. Поперечное сечение ядерной реакции (n,γ) 53∙10−33 м2, поперечное сечение захвата тепловых нейтронов дейтронами 15∙10−32 м2 (для протонов 3∙10−29м2). Молекула двухатомна, длина связи 0,07417 нм; осн. частота колебаний атомов 3118,46 см−1; энергия диссоциации 440 кДж/моль, константа диссоциации К = p2D/pD2 = 4,173∙10−73 (293,15 К). С др. изотопами водорода Д. образует молекулы протодейтерия HD (мол. м. 3,02205) и дейтеротрития DT (мол. м. 5,03034). В прибрежной морской воде соотношение D/(D + Н) составляет (155–156)∙10−6, в поверхностных водах — (132–151)∙10−6, в прир. газе — (110–134)∙10−6.
Свойства. Коэф. сжимаемости Д. (pV/RT) при 273,15 К: 1,0121 (2,0266 МПа), 1,0624(10,133 МПа), 1,130(20,266 МПа). C0 [в Дж/(моль∙К)]: 20,81 (20 К), 30,11 (100 К), 29,30 (298 К); теплопроводность 0,135 Вт/(м∙К) (25 К); η 1,23∙10−2 мПа∙с (293,15 К). Д. раств. в жидкостях (напр., в бензоле, толуоле, октане, гептане, CCl4, CS2) лучше, чем H2, причем это различие возрастает с понижением температуры. Молекула D2 может находиться в орто- и пара-состояниях. Ортодейтерий (o-D2) имеет параллельную (одного знака) ориентацию ядерных спинов, а парадейтерий (п-D2) — антипараллельную. Это обусловливает некоторое различие магн., оптич. и термич. свойств разл. модификаций. При обычных условиях D2 (нормальный Д., н-D2) представляет собой смесь 2/3 орто- и 1/3 пара-модификаций, которые могут взаимно превращаться друг в друга (орто-пара-превращение). Каждой данной температуре соответствует определенный равновесный состав (равновесный Д., p-D2). Так, доля п-D2 составляет: 0,333 (при 300 К), 0,251 (60 К), 0,148 (40 К), 0,019 (20 К). При низких температурах термодинамически стабилен o-D2. Самопроизвольное орто-пара-превращение при низких температурах происходит очень медленно, что позволяет получить жидкий Д., близкий по составу к нормальному. Орто-пара-превращение ускоряется в присутствии катализаторов (соед. Fe, Cr, Со, Mn, РЗЭ). Свойства Д. приведены в табл. 1 и 2.
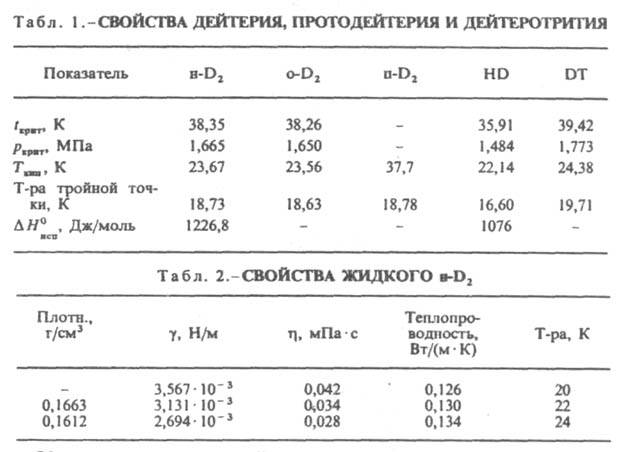
Уравнение температурной зависимости давления пара над твердым и жидким Д.: lg 0,0075p (Па) = А — В/Т + СT (значения А, В и С приведены в табл. 3).
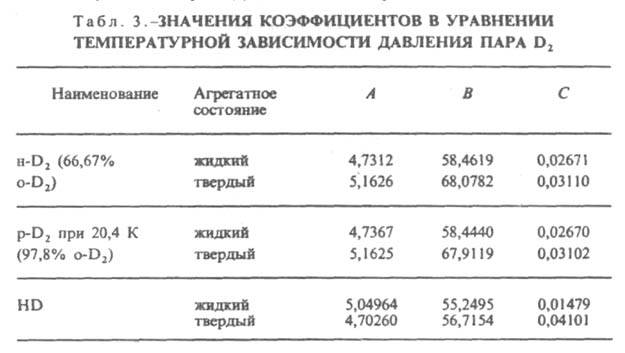
Теплота испарения o-D2 (в Дж/моль): 1202,9 (24,25 К), 1029,5 (30,53 К). Твердый D2 имеет тетрагон, объемноцентрированную решетку, а = 0,338 нм, с = 0,560 нм; т. пл. 18,73 К. H2 и D2 не изоморфны, обнаружена их ограниченная взаимная растворимость в твердом состоянии. При 4,2 К предельная растворимость D2 в H2 ок. 10% по объему, а растворимость H2 в D2 21%. По химическим свойствам D2 аналогичен H2, однако скорость реакций при замещении Н на D заметно уменьшается, напр., при окислении орг. соед., взаимод. H2 с Cl2 — в 5–10 раз. При электролизе воды D2 выделяется медленнее, чем H2. Важное практич. значение имеют реакции изотопного обмена Д. Константа равновесия реакции H2 + D2 ⇄ 2HD составляет: 1,345 (50 К), 2,903 (200 К), 3,44 (373,15 К), 3,80 (700 К). Осуществляют ее в присутствии катализатора (Pt, Ni, РЗЭ). Для реакции НDO(ж) + D2(г) ⇄ D2O(ж) + HD(г) (где ж — жидкость, г — газ) константа равновесия: 3,96 (223,15 К), 2,92 (323,15 К), 2,40 (373,15 К). Для реакции H2O(ж) + HD ⇄ НDO(ж) + H2(г) константа равновесия: 4,69 (223,15 К), 3,37 (323,15 К), 2,69 (373,15 К). Изотопный обмен между водой и D2 или HD может протекать в паровой фазе в присутствии катализаторов (напр., Ni) или в жидкой под давлением (из-за плохой растворимости изотопов водорода в воде) в присутствии катализаторов (в т. ч. гидрофобных) в гомог. или гетерог. системе. Некоторые реакции изотопного обмена Н протекают очень быстро, напр., в группах OH (щелочи, спирты) и NH (NH3, амины). Важнейшие соед. Д.- тяжелая вода D2O. Дейтериды соед., аналогичные гидридам. Большое практич. значение имеет дейтерид лития 6LiD — осн. компонент заряда термоядерного (водородного) оружия. Для аналит. определения Д. применяют масс-спектрометрич., спектральные, хроматографич., а также денсиметрические (путем измерения плотности) методы изотопного анализа.
Получение. Д. выделяют гл. обр. из тяжелой воды, напр., электролизом, реакцией с металлами. Д. получают также низкотемпературной ректификацией из электролитич. водорода или азотоводородной смеси для синтеза NH3 (водород которой содержит 250–300 м. д. HD). Исходный водород или азото-водородную смесь после тщательной очистки от примесей (O2 до 10−9 мольных долей, остальные газы — до 10−7–10−8 мольных долей) сжижают и двухступенчатой ректификацией при 22–24 К выделяют конц. HD. Последний в присутствии катализатора превращается в смесь H2 + D2 + HD, из которой низкотемпературной ректификацией получают 99,8%-ный D2. Сжиганием с воздухом или O2 последний переводят в тяжелую воду.
Применение. Д. (в виде D2O) — замедлитель нейтронов в ядерных реакторах. Дейтроны, обычно получаемые путем ионизации атомов Д., используются в качестве бомбардирующих частиц в ядерных реакциях, в частности для получения быстрых нейтронов. Д. применяется также как изотопный индикатор в научных исследованиях в химии, биологии, физиологии, агрохимии и др. (в т. ч. в опытах с живыми организмами и при диагностич. исследованиях человека). Соед. Д. используются также при спектроскопич. исследованиях. Изделия из монокристаллов на основе KD2PO4 применяются для создания систем управления и преобразования лазерного излучения. Д. — ядерное топливо для энергетики будущего, основанной на управляемом термоядерном синтезе. В первых энергетич. реакторах такого типа предполагается осуществить реакцию D + T ⇄ He + n + 17,6 МэВ. Д. открыт Г. Юри с сотрудниками в 1932.
Лит.: Выделение дейтерия из водорода методом глубокого охлаждения, М., 1961; Тупицын И. Ф., Тяжелые изотопы водорода, дейтерий и тритий, М., 1961; Андреев Б. М., Зельвенский Я. Д., Катальников С. Г., Тяжелые изотопы водорода в ядерной технике, М., 1987
Я. Д. Зельвенский
Значения в других словарях
- дейтерий — -я, м. физ. Изотоп водорода с массовым числом 2 (вдвое массивнее легкого изотопа водорода). [От греч. δεύτερος — второй] Малый академический словарь
- Дейтерий — (лат. Deuterium, от греч. déuteros — второй) D, 2Н, тяжёлый водород, стабильный изотоп Водорода с массовым числом 2. Ядро атома Д. — Дейтрон. Большая советская энциклопедия
- дейтерий — орф. дейтерий, -я Орфографический словарь Лопатина
- ДЕЙТЕРИЙ — ДЕЙТЕРИЙ, изотоп (D, или 2Н) водорода, ядра которого (ДЕЙТРОНЫ) помимо протона содержат также нейтрон. На каждый миллион атомов водорода, существующего в природе, приходится около 156 атомов дейтерия. Научно-технический словарь
- Дейтерий — (греч. deuteros второй) стабильный изотоп водорода, ядро которого состоит из 1 протона и 1 нейтрона; в биохимических исследованиях используется в качестве метки. Медицинская энциклопедия
- дейтерий — ДЕЙТЕРИЙ [дэ; тэ], -я; м. [от греч. deuteros — второй] Физ. Изотоп водорода, имеющий атомную массу, равную 2, соединение которого с кислородом даёт "тяжёлую воду" (вдвое массивнее лёгкого изотопа водорода; применяется в ядерной энергетике). ◁ Дейтериевый, -ая, -ое. Толковый словарь Кузнецова
- дейтерий — ДЕЙТЕРИЙ [дэ, тэ], я, м. Тяжёлый водород, стабильный изотоп водорода. | прил. дейтериевый, ая, ое. Толковый словарь Ожегова
- дейтерий — [< гр. второй] – изотоп хим. элемента водорода с атомным весом 2,01363; его соединение с кислородом даёт “тяжёлую воду”, отличающуюся по своим физическим свойствам от обыкновенной воды; отношение количеств дейтерия к водороду в обычной воде равно 1:5000 Большой словарь иностранных слов
- дейтерий — дейтерий м. Изотоп водорода с массовым числом 2 (вдвое тяжелее лёгкого изотопа водорода). Толковый словарь Ефремовой
- ДЕЙТЕРИЙ — ДЕЙТЕРИЙ (лат. deuterium, от греч. deuteros — второй) — D, 2Н, тяжелый водород, стабильный изотоп водорода с массовым числом 2. Ядро атома (дейтрон) состоит из протона и нейтрона. С кислородом образует тяжелую воду. Открыт Г. Юри в 1932. Большой энциклопедический словарь
