бензотиофены
БЕНЗОТИОФЕНЫ
мол. м. 134,2; бесцветные кристаллы. Существуют в виде двух изомеров — бензо [в] тиофена (формула I) и бензо [с] тиофена (II).
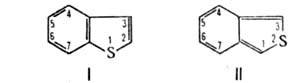
Для бензо [в] тиофена (тионафтена) т. пл. 31,34 °C (пикрата 149 °C), т. кип. 219,9 °C, 103–105 °C/20 мм рт. ст.; d440 1,1937, nD20 1,6302. Он хорошо раств. в органических растворителях, плохо — в воде; μ 2,06∙10−30 Кл∙м (бензол). Обладает ароматич. с веществами. Электроф. замещение идет гл. обр. в положения 3 и 2 (реакц. способность др. положений уменьшается в ряду 6 > 5 > 4 > 7). Металлирование с помощью C4H9Li идет в положение 2. Электронодонорные заместители в положении 2 или 3 направляют замещение в соседнее положение, электроноакцепторные — в бензольное кольцо. Введение одной или двух алкоксигрупп в бензольное кольцо значительно облегчает ацилирование и направляет его в положение 2. При взаимодействии с Na в жидком NH3 образуется о-этилтиофенол, с никелем Ренея — этилбензол. Сильные алкилирующие средства алкилируют по S с образованием солей бензотиофения. Бензо [в] тиофены с группой NH2 во 2 или 3 положении мало устойчивы. Обычно их выделяют в виде солей или N-ацильных производных. 2- и 3-Гидрохсибензотиофены существуют только в виде оксопроизводных.
Бензо [в] тиофен и его алкильные производные обнаружены в сланцевых маслах, кам.-yr. смоле и нефтях. Его получают взаимод. стирола с H2S при 600 °C. Бензо [в] тиофен и его производные синтезируют циклизацией сульфидов PhSCH(R)COR' (R=H, Alk; R'= OH, OAlk, Alk, Ar), взаимод. коричных кислот с SOCl2:
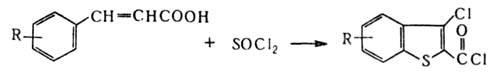
аннелированием бензольного кольца к тиофеновому, напр.:
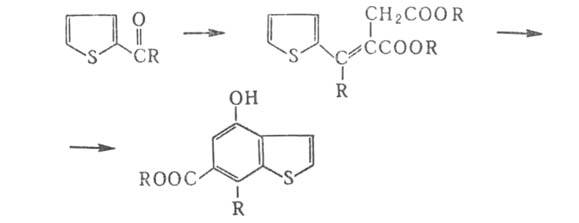
реакцией S с экзогалогенопроизводными алкилбензолов, напр.:
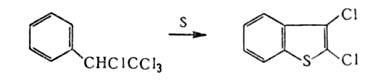
Бензо [в] тиофен используют как добавку к электролиту при никелировании; бензо [в]тиофен-3(2H)-он и его производные (тиоиндоксилы) применяют в синтезе тиоинди-гоидных красителей.
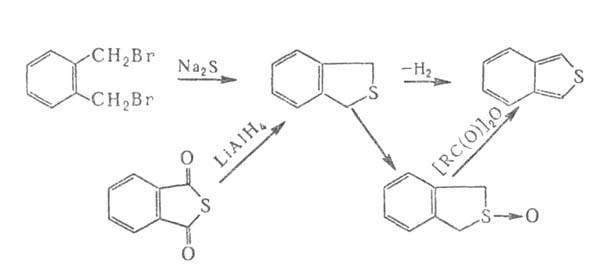
Бензо [с] тиофен (изобензотиофен) — вещество с сильным запахом нафталина; т. пл. 50–51 °C. Разлагается уже при −30 °C в атмосфере N2. Нестабильность обусловлена повыш. электронной плотностью у углеродных атомов в положениях 1 и 3 (1,3-замещенные Б. устойчивы). Легко образует аддукты с малеиновым ангидридом и др. диенофилами. Получают его из 1,3-дигидробензо [с] тиофена, который в свою очередь синтезируют из о-ксилолдибромида или фталевого тиоангидрида:
Лит.: Hartough H. D.. Meisel S. Н.. в кн.: Compounds with condensed thiophene rings, N.Y.. 1954, p. 17–224; Iddon В., Scrowston R. M., в кн.: Advances in heterocyclic Chemistry, v. 11. N.Y.-Z.. 1970, p. 177–381.
В. И. Шведов
