аммиак
АММИАК (от греч. hals ammoniakos, букв. — амонова соль; так назывался нашатырь, который получали близ храма бога Амона в Египте) NH3
бесцветный газ с резким запахом. Молекула имеет форму правильной пирамиды (см. рис. 1). Связи N— Н полярны; μ 4,85∙10−30 Кл∙м (0–150 °C); энергия связи N—Н 389,4 кДж/моль. Поляризуемость молекулы 22,6∙10−25 см3. У атома N имеется неподеленная пара электронов, которая обусловливает способность А. к образованию донорно-акцепторной и водородной связей. Существование водородных связей и значительная полярность молекул А. — причины сильного взаимодействия между ними, вследствие чего физические свойства А. во многом аномальны по сравнению со свойствами однотипных соединений (PH3, SbH3, AsH3). Для NH3 т. пл. −77,7 °C, т. кип. −33,35 °C; dt4 0,790 ( −40 °C), 0,681 ( −33,35 °C), 0,639 (0 °C), 0580 (40 °C); tкрит 133 °C, pкрит 11,425 кПа, dкрит 0,235 г/см3; ΔH0исп 23,27 кДж/моль, ΔH0пл, 5,86 кДж/моль; для газа Cр° 35,63 Дж/(моль∙К), ΔH0o6p −45,94 кДж/моль, S0298 192,66 Дж/(моль∙К).
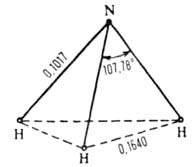
Рис. 1. Структура молекулы NH3 (длина связи — в нм).
Твердый А. — бесцветные кристаллы с кубич. решеткой (а = = 0,515 нм, 2 = 4, пространственная группа Р213). В жидком А. молекулы ассоциированы вплоть до критич. температуры, электролитич. диссоциация совершенно ничтожна, произведение концентраций [NH;][NH2] составляет 10−22 ( −33,4 °C); 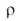 8∙106 Ом∙см;
8∙106 Ом∙см; 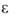 25,4 ( −77 °C). Жидкий А. растворяет щелочные и щел.-зем. металлы, Al, Eu, Yb, P, S, I, мн. интерметаллиды и др. Растворы металлов в жидком А. имеют металлич. проводимость, поскольку содержат ионы металла и сольватированные электроны; они являются сильнейшими восстановителями. Растворенные в А. соед. с полярной ковалентной или ионной связью диссоциируют на ионы. В жидком А. многие вещества способны отщеплять протон, кислотные свойства проявляют в нем даже углеводы, амиды кислот, некоторые углеводороды.
25,4 ( −77 °C). Жидкий А. растворяет щелочные и щел.-зем. металлы, Al, Eu, Yb, P, S, I, мн. интерметаллиды и др. Растворы металлов в жидком А. имеют металлич. проводимость, поскольку содержат ионы металла и сольватированные электроны; они являются сильнейшими восстановителями. Растворенные в А. соед. с полярной ковалентной или ионной связью диссоциируют на ионы. В жидком А. многие вещества способны отщеплять протон, кислотные свойства проявляют в нем даже углеводы, амиды кислот, некоторые углеводороды.
Растворимость А. в воде (% по массе): 42,8 (0 °C, 33,1 (20 °C), 23,4 (40 °C), 14,1 (60 °C). Плотность водных растворов (г/см3): 0,970 (8% по массе NH3), 0,947 (16%), 0,889 (32%), 0,832 (50%), 0,733 (75%). Для бесконечно разб. водного раствораΔH0растворения 133,26 кДж/моль. А. хорошо раств. (но хуже, чем в воде) в спирте, ацетоне, хлороформе, бензоле и др. органических растворителях. Образует гидраты с двумя (т. пл. ок. −90 °C), одной ( −79 °C) и 0,5 ( −78,2 °C) молекулами воды.
В системе NH3—H2O установлено существование эвтектик: лед + NH3*H2O (33,23% по массе NH3, т. пл. −100,3 °C), NH3*H2O + NH3*0,5H2O (55,11%, −83,3 °C), NH3*H2O + NH3 (80,05%, — 92,5 °C). В водном растворе А. частично ионизирован на NH4+ и OH , что обусловливает щелочную реакцию раствора (pKа 9,247).
Разложение А. на водород и азот становится заметным выше 1200–1300 °C, в присутствии катализаторов — выше 400 °C. А. весьма реакционноспособен. Для него типичны реакции присоединения, в частности протона при взаимодействии с кислотами. В результате образуются соли аммония, которые по многим свойствам подобны солям щелочных металлов.
А. — основание Льюиса, присоединяет не только H+ , но и др. акцепторы электронов, напр. BF3 с образованием BF3*NH3. Дает аммины при взаимодействии с солями. Щелочные и щел.-зем. металлы реагируют с жидким и газообразным А., давая амиды. При нагр. в атмосфере А. многие металлы и неметаллы (Zn, Cd, Fe, Cr, B, Si и др.) образуют нитриды. Жидкий А. взаимод. с серой по реакции: 10S + 4NH3 → 6H2S + N4S4. Ок. 1000 °C А. реагирует с углем, образуя HCN и частично разлагаясь на N2 и H2. Большое практич. значение имеет реакция А. с CO2, ведущая к образованию карбамата аммония NH2COONH4, который при 160–200 °C и давл. до 40 МПа распадается на воду и мочевину. Водород в А. может быть замещен галогенами. А. горит в атмосфере O2, образуя воду и N2. Каталитич. окислением А. получают NO промежут. продукт в производстве HNO3. Каталитич. окисление А. в смеси с CH4 дает HCN. Такие сильные окислители, как H2O2, K2Cr2O7 и KMnO4, окисляют А. в водных растворах. Газообразный А. окисляется Br2 и Cl2 до N2.
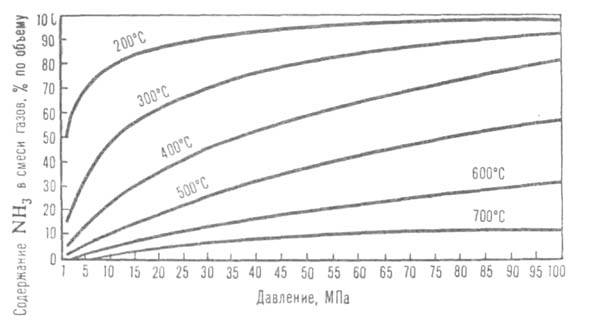
Рис. 2. Зависимость равновесного содержания NH3 в газовой смеси (H2: N2 = 3) от давления при разных температурах.
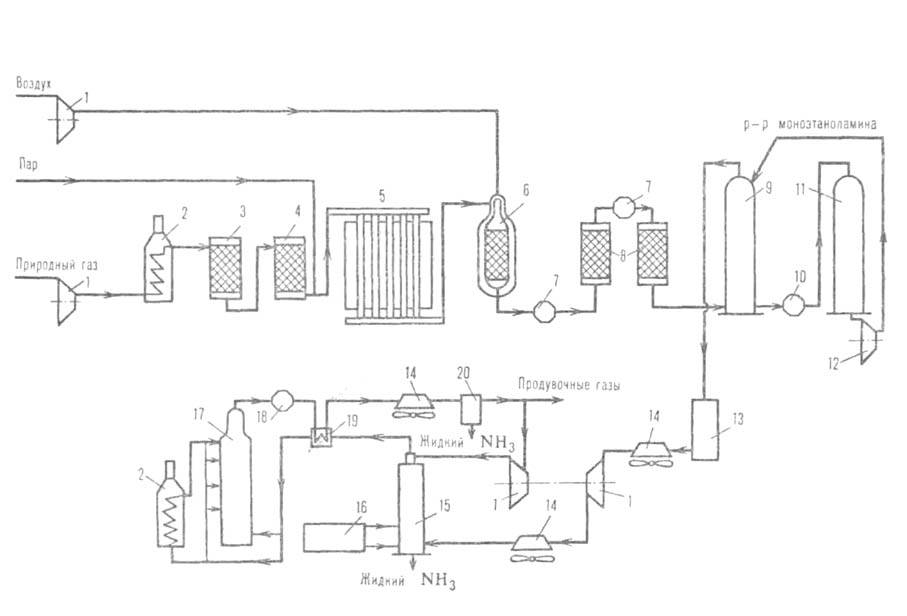
Рис. 3. Агрегат синтеза аммиака мощностью 1360 т/сут: 1 — компрессоры; 2 — подогреватели; 3 — аппарат для тарирования сераорг. соед.; 4 — адсорбер H2S; 5 — трубчатая печь (первичный риформинг); 6 — шахтный конвертор (вторичный риформинг); 7 — паровые котлы; 8 — конверторы СО; 9 — абсорбер CO2; 10 — кипятильник; 11 — регенератор раствора моноэтаноламина; 12 — насос; 13 — аппарат для гидрирования остаточных CO и CO2; 14 — воздушные холодильники; 15 — конденсац. колонна; 16 — испаритель жидкого NH3 (для охлаждения газа и выделения NH3); 17 — колонна синтеза NH3; 18 — водоподогреватель; 19 — теплообменник; 20 — сепаратор.
Осн. пром. способ получения А. — по реакции 1/2N2 + 3/2H2 ⇄ NH3. Сдвигу равновесия вправо способствуют повышение давления и понижение температуры (см. рис. 2). Тепловой эффект реакции при 29,4 МПа составляет 52,38 кДж/моль при 500 °C и 51,29 кДж/моль при 400 °C (с учетом теплоты смешения газов). Процесс проводят в присутствии кат. — Fe, активированного K2O, Al2O3, CaO и др. Каталитич. яды — сернистые и кислородсодержащие соединения. Для известных катализаторов скорость реакции описывается уравнением Темкина — Пыжева:
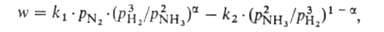
где w — наблюдаемая скорость процесса, равная разности скоростей образования и разложения A., kl и k2-константы скорости образования и разложения А., рH2 , pN2 и pNH3 — парциальное давление соответствующего газа, α=0,5 для большинства пром. катализаторов. При давл. ~ 30 МПа и температуре ~ 500 °C, используемых на практике, равновесная концентрация А. в газовой смеси составляет ~ 30%. Однако равновесие на выходе из колонны синтеза, как правило, не достигается, поскольку с целью увеличения производительности единицы объема катализатора процесс проводят при высоких объемных скоростях ( ~ 15000 ч −1). Поэтому при однократном прохождении через массу катализатора возможно превращ. в А. лишь 15–25% исходной газовой смеси. Для полного превращ. необходима многократная циркуляция, которую осуществляют с помощью компрессора. В цикл непрерывно вводят свежую газовую смесь взамен пошедшей на образование А. Осн. сырье (~ 90%) для получения H2 в производстве А. — прир. газ, перерабатываемый в осн. методом двуступенчатой паровой конверсии (см. водород); незначит. долю (менее 10%) составляет коксовый газ и электролитич. водород. Мощность установок по производству А. из прир. газа 200 и 420 тыс. т/год. Производство А. в агрегатах мощностью 1360 т/сут осуществляется в одной технол. линии (см. рис. 3) и включает след. стадии: 1) очистку прир. газа от сернистых соед. каталитич. гидрированием их до H2S с послед. его поглощением ZnO; 2) паровую конверсию прир. газа под давл. 3,8 МПа при 860 °C на катализаторе Ni-Al в трубчатой печи (первичный риформинг); 3) паровоздушную конверсию остаточного метана в шахтном конверторе (вторичный риформинг) при 990–1000 °C и 3,3 МПа, на катализаторе Ni-Al; на этом этапе водород обогащается азотом воздуха для получения смеси состава H2: N2 = 3, поступающей на синтез NH3; 4) конверсию CO до CO2 и H2 сначала при 450 °C и 3,1 МПа на катализаторе Fe-Cr, затем при 200–260 °C и 3,0 МПа на катализаторе Zn-Cr-Cu; 5) очистку H2 от CO2 абсорбцией раствором моноэтаноламина или горячим раствором K2CO3 при 2,8 МПа; 6) очистку газа путем гидрирования от остаточных CO и CO2 в присутствии Ni-Al при 280 °C и 2,6 МПа; 7) компримирование очищенного газа до 30 МПа и синтез А. на железном промотированном катализаторе при 420–500 °C. Реактор синтеза А. представлен на рис. 4.
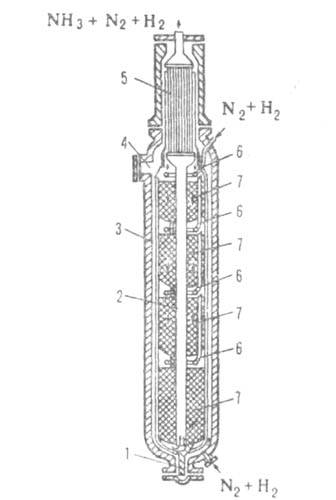
Рис. 4. Колонна синтеза аммиака: 1 — люк для выгрузки катализатора; 2 — центр, труба; 3 — корпус; 4 — люк для загрузки катализатора; 5 — теплообменник; 6 — трубы для ввода холодного газа; 7 — катализатор.
А. выпускается в жидком виде либо в виде водного раствора-аммиачной воды, чаще всего с содержанием 25% NH3. А., поставляемый на нужды промышленности, содержит не менее 99,96% по массе NH3, до 0,04% H2O, до 2 мг/л машинного масла, до 1,0 мг/л Fe. В техн. А., транспортируемый по трубопроводу, добавляется до 0,2–0,4% H2O для ингибирования коррозии стали. А. обнаруживается по характерному запаху. Бумажка, смоченная раствором Hg2(NO3)2, при действии А. чернеет. Малые количества А. в водных растворах открывают с помощью реактива Несслера. Количественно А. определяют титриметрически.
Применяют А. в производстве HNO3, мочевины, NH4NO3, (NH4)2CO3, (NH4)2SO4 и др., аммофоса, уротропина, как жидкое удобрение, в качестве хладагента. Мировое производство А. составило в 1982 ок. 89 млн. т, в т. ч. в СССР 17,76, США 14.06, СРР 3,14, Франции 1,9, Японии 2,01, ФРГ 1,92 млн. т.
Жидкий А. хранят при 2,0 МПа или при атм. давлении и −33 °C. Перевозят в стальных баллонах (окрашены в желтый цвет, имеют надпись "Аммиак" черного цвета), железнодорожных и автомобильных цистернах, по воде — в спец. танкерах, транспортируют также по трубопроводам. При содержании в воздухе 0,5% по объему А. сильно раздражает слизистые оболочки. При остром отравлении поражаются глаза и дыхат. пути, при хронич. отравлениях наблюдаются расстройство пищеварения, катар верх. дыхат. путей, ослабление слуха. Жидкий А. вызывает сильные ожоги кожи. ПДК 20 мг/м3. Смесь А. с воздухом взрывоопасна, КПВ 15–28%; для воздушно-аммиачных смесей, содержащих 9–57% по объему А., т. всп. ок. 1000 °C. Чистый А. был получен Дж. Пристли в 1774.
Лит.: Малина И. К., Развитие исследований в области синтеза аммиака, М., 1973; Алексеев А. М. [и др.], "Ж. Всес. хим. о-ва им. Д.И.Менделеева", 1978, т. 23, [№] 1, с 31–38; Синтез аммиака, М., 1982; Жаворонков Н. М., Овчаренко Б. Г., Охотский С. М., в кн.: Развитие химической промышленности в СССР, т. 2, М., 1984, с. 7–37. См. также лит. при ст. азот.
Н. М. Жаворонков, Л. Д. Кузнецов
Значения в других словарях
- аммиак — -а, м. Бесцветный газ с резким неприятным запахом, представляющий собой соединение азота с водородом и образующий при растворении в воде так наз. нашатырный спирт. [От греч. ‛άλς ’αμμωνιακόν — смолистая камедь] Малый академический словарь
- Аммиак — NH3, простейшее химическое соединение азота с водородом. Один из важнейших продуктов химической промышленности; синтез А. из азота воздуха и водорода — основной метод получения т. н. связанного Азота. В природе... Большая советская энциклопедия
- аммиак — АММИАК, NH3, химич. соединение азота с водородом. Бесцветный газ с резким удушливым запахом. Химически активен. Легко растворяется в воде (10%-ный водный раствор А. известен как нашатырный спирт), при взаимодействии... Ветеринарный энциклопедический словарь
- аммиак — АММИАК а, м. ammoniaque m. <�Слово> аммиак, представляет собой искусственное образование химика Я. Д. Захарова в результате сокращения слова аммониак в 1801 г., заимствованного в 1799 г. из фр. яз. ЭС. Словарь галлицизмов русского языка
- аммиак — Аммиа́к/. Морфемно-орфографический словарь
- аммиак — орф. аммиак, -а Орфографический словарь Лопатина
- аммиак — NH3, простейшее химич. соединение азота с водородом. Конечный продукт распада и исходное соединение при биосинтезе азотсодержащих веществ в живых клетках. Концентрация свободного А. в живых тканях в виде иона аммония (NH 4) невелика. Биологический энциклопедический словарь
- АММИАК — АММИАК (NH3), бесцветный, негорючий газ, с едким запахом, состоящий из азота и водорода. Используется для производства азотистых удобрений. Научно-технический словарь
- Аммиак — Бесцветный газ (химическая формула — 4), важное звено в круговороте азота в биосфере, продукт деятельности микроорганизмов-азотфиксаторов, связывающих атмосферный азот. Кроме того... Экологические термины и определения
- Аммиак — I Аммиак химическое соединение азота с водородом, в организме человека и животных образуется в процессе азотистого обмена, токсичен. В медицине 10% водный раствор аммиака известен как нашатырный спирт. При растворении в воде... Медицинская энциклопедия
- аммиак — АММИАК -а; м. [франц. ammoniaque]. Бесцветный газ с резким неприятным запахом, представляющий собой соединение азота с водородом и образующий при растворении в воде нашатырный спирт (применяется для производства удобрений, в холодильных установках и т.п. Толковый словарь Кузнецова
- аммиак — АММИАК, АММОНИАК м. летучая щелочь, нашатырная щелочь, состоящая из азота и водорода; известна как составная часть нашатыря и спирта его. Аммиаковый, аммиачный, нашатырный. Толковый словарь Даля
- аммиак — аммиак м. Бесцветный газ с резким запахом, представляющий собою соединение азота с водородом. Толковый словарь Ефремовой
- аммиак — АММИ’АК, аммиака, мн. нет, ·муж. (см. аммониак). 1. Бесцветный газ с едким запахом, состоящий из азота и водорода (·хим. ). 2. Нашатырный спирт (·разг., спец., ·апт. ). Толковый словарь Ушакова
- аммиак — [ < гр. смолистая камедь] – бесцветный газ с резким неприятным запахом, соединение азота с водородом; образуется при гниении органических веществ, например, навоза; в промышленности аммиак получается синтетически из элементов азота и водорода... Большой словарь иностранных слов
- АММИАК — АММИАК (от греч. hals ammoniakos — нашатырь) — NH3, бесцветный газ с резким удушливым запахом; плотность 0,681 г/см3 (-33,35 °С) — tпл -77,7 °С, tкип -33,35 °С; при давлении 0,9 МПа сжижается при комнатной температуре. Большой энциклопедический словарь
- аммиак — АММИАК, а, м. Бесцветный газ с едким запахом, соединение азота с водородом. | прил. аммиачный, ая, ое. Толковый словарь Ожегова
