аллильные комплексы переходных металлов
АЛЛИЛЬНЫЕ КОМПЛЕКСЫ ПЕРЕХОДНЫХ МЕТАЛЛОВ
В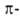 аллильных комплексах (А. к.) металл связан со всеми тремя атомами С лиганда, имеющего делокализованную систему
аллильных комплексах (А. к.) металл связан со всеми тремя атомами С лиганда, имеющего делокализованную систему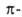 электронов; считают, что
электронов; считают, что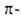 аллильный лиганд занимает в координац. сфере металла два координац. места. Существуют также
аллильный лиганд занимает в координац. сфере металла два координац. места. Существуют также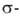 аллильные производные, в которых металл связан только с α-углеродным атомом аллильной группы. Такие соед. — частный случай комплексов переходных металлов с
аллильные производные, в которых металл связан только с α-углеродным атомом аллильной группы. Такие соед. — частный случай комплексов переходных металлов с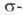 связью металл-углерод.
связью металл-углерод.
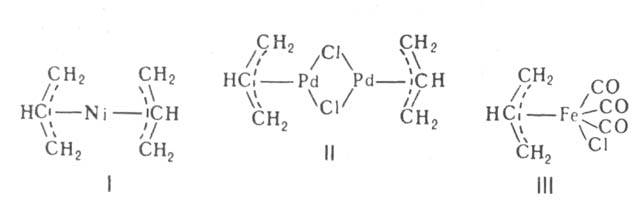
Основные типы А.к.: 1) гомолигандные, содержащие в молекуле только аллильные группы, напр. бис-(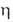 -аллил)-никель (формула I) (такие комплексы известны для большинства переходных металлов); 2) мономерные и димерные аллилметаллгалогениды, наиб. характерные для Pd и Ni, напр. ди-
-аллил)-никель (формула I) (такие комплексы известны для большинства переходных металлов); 2) мономерные и димерные аллилметаллгалогениды, наиб. характерные для Pd и Ni, напр. ди-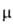 -хлоро-бис-(
-хлоро-бис-(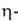 аллил)палладий (формула II); 3) аллилкарбонилметаллы, образуемые гл. обр. Mo, W, Mn, Fe, Co, напр. (
аллил)палладий (формула II); 3) аллилкарбонилметаллы, образуемые гл. обр. Mo, W, Mn, Fe, Co, напр. ( -аллил)(трикарбонил)хлорожелезо (формула III). Получен, кроме того, ряд комплексов, содержащих, помимо
-аллил)(трикарбонил)хлорожелезо (формула III). Получен, кроме того, ряд комплексов, содержащих, помимо -аллильного, циклопентадиенильные, диеновые, ареновые и др. орг. лиганды.
-аллильного, циклопентадиенильные, диеновые, ареновые и др. орг. лиганды.
Свойства А. к. изменяются в широких пределах, напр. I-светло-оранжевая жидкость с т. пл. 1 °C, II и III-твердые желтые вещества с т. пл. 152–155 и 58 °C (в обоих случаях с разложением). Большинство гомоаллильных комплексов существует только при низких температурах. Многие из них пирофорны, а соответствующие им аллилгалогениды достаточно устойчивы к окислению.
Хим. превращения А.к. сопровождаются в большинстве случаев разрушением связи металл-лиганд. Так, при окислит. сольволизе аллилпалладийгалогенидов образуются олефины, альдегиды и кетоны, при щелочном гидролизе-олефины. Эти многостадийные реакции включают автокатализ продуктами распада комплексов и идут с участием растворителя. Гидрогенолиз комплексов приводит к их разложению с образованием алканов. При действии CO, фосфинов, фосфитов и др. электронодонорных соединений А. к. частично или полностью разрушаются, напр.:
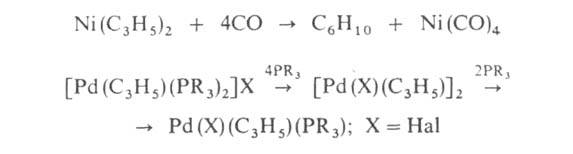
А. к. — промежут. соединения во мн. реакциях непредельных соединений, которые идут в присутствии комплексов переходных металлов, напр. карбонилировании, изомеризации, гидрировании, окислении, олиго- и полимеризации. Важная роль А. к. в этих процессах обусловлена их способностью легко вступать в реакции с CO, олефинами, ацетиленами и др. ненасыщенными соединениями. Такие реакции внедрения по связи металл-лиганд через промежут. аллильные производные часто являются ключевыми в каталитич. процессах.
аллильные производные часто являются ключевыми в каталитич. процессах.
В спектрах ЯМР некоторых А. к. наблюдается магнитная эквивалентность всех терминальных протонов (т. наз. дина-мич. аллильные системы), что объясняется быстрыми и обратимыми переходами комплексов в аллильные производные, межмол. обменом, вращением аллильного лиганда и др.
аллильные производные, межмол. обменом, вращением аллильного лиганда и др.
Методы синтеза А.к.:
1. Взаимод. солей металлов, гл. обр. галогенидов, с ал-лильными производными Na, Li, Mg, Sn, Zn, В, Hg. Метод применим прежде всего для синтеза гомоаллильных комплексов, напр.: NiBr2 + 2C3H5MgBr → [Ni(C3H5)2]. Аналогично получают некоторые аллилгалогенидные, аллилкарбонильные и аллилциклопентадиенильные комплексы, напр.:
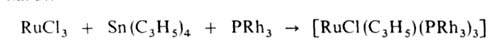
2. Взаимод. аллилгалогенидов или аллиловых спиртов с металлами, их солями, карбонилами или др. производными. Например, обработкой водно-метанольного раствора PdCl2 или Na2PdCl4 аллилхлоридами и CO получают аллилпалла-дийхлориды:
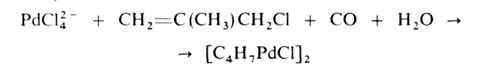
Реакцией карбонилов металлов с аллилгалогенидами синтезируют аллилкарбонилметаллы: Fe(CO)5 + C3H5Х → [Fe(X)(CO)3(C3H5)].
3. Взаимод. моно- или диолефинов с солями, карбонилами металлов и их производными, напр.:
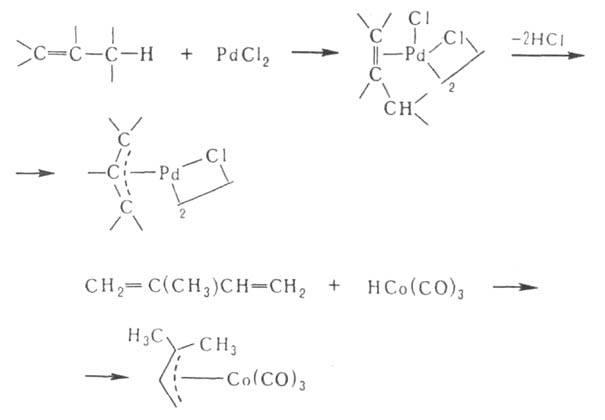
4. Превращение в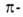 аллильные др. лигандов, гл. обр. координированных диенов:
аллильные др. лигандов, гл. обр. координированных диенов:
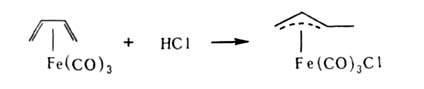
Формально к этому же методу можно отнести перегруппировку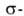 аллильных производных карбонилов металлов в
аллильных производных карбонилов металлов в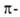 аллильные, напр.:
аллильные, напр.:
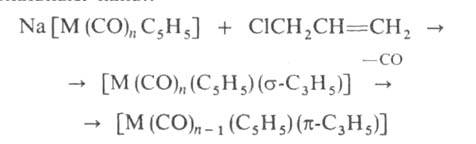
где M=Fe, Mo, W; n = 2, 3.
А. к. — высокоактивные и избирательные катализаторы, напр. бис-(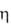 -аллил)никель — циклим, тримеризации бутадиена в 1,5,9-циклододекатриен,
-аллил)никель — циклим, тримеризации бутадиена в 1,5,9-циклододекатриен, 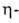 аллилникельгалогениды — стереоспецифич. полимеризации 1,3-бутадиена.
аллилникельгалогениды — стереоспецифич. полимеризации 1,3-бутадиена.
Лит.: Крицкая И.И., в кн.: Методы элементоорганической химии. Типы металлоорганических соединений переходных металлов, под ред. А.Н. Несмеянова, К.А. Кочешкова, кн. 2, М., 1975, с. 734–908.
Л. В. Рыбин
