акрилонитрил
АКРИЛОНИТРИЛ (нитрил акриловой кислоты, 2-пропеннитрил, винилцианид) CH2=CHCN
мол. м. 53,06; бесцветная жидкость с резким запахом; т. затв. −83,55 °C, т. кип. 77,3 °C; d420 0,8064, nD20 1,3914; η 0,40 мПа∙с (20 °C), 0,25 мПа∙с (60 °C); давление пара (кПа): 11,3 (20 °C), 26,67 (40 °C), 108,7 (80 °C); 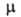 (пар) 1,29∙1029 Кл∙м; потенциал ионизации 10,75 эВ; ркрит 3,54 МПа, tкрит 246 °C; C0p 2,09
(пар) 1,29∙1029 Кл∙м; потенциал ионизации 10,75 эВ; ркрит 3,54 МПа, tкрит 246 °C; C0p 2,09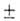 0,12 кДж/(кг∙К); ΔH0обр −190 кДж/моль (газ), −152 кДж/моль (жидкость).ΔH0исп 32,6 кДж/моль (0–80 °C); ΔH0сгор 1,76 МДж/моль, ΔS6 (пар) 274,1 Дж/(моль∙К).
0,12 кДж/(кг∙К); ΔH0обр −190 кДж/моль (газ), −152 кДж/моль (жидкость).ΔH0исп 32,6 кДж/моль (0–80 °C); ΔH0сгор 1,76 МДж/моль, ΔS6 (пар) 274,1 Дж/(моль∙К).
А. смешивается со многими орг. растворителями; растворимость в воде 7,3% (20 °C). Образует азеотропные смеси с водой (87,5% А.; т. кип. 70,5 °C), бензолом (47% А.; 73,3 °C), метанолом (38,7% А.; 61,4 °C), CCl4 (21% А.; 66,2 °C) и др.
Для А. Наиб. характерны реакции по связи C=C, в т. ч. полимеризация с образованием полиакрилонитрила и сополимеризация с бутадиеном, стиролом, винилхлоридом и др. Для предотвращения самопроизвольной полимеризации А. при хранении ингибируют NH3, гидрохиноном или др. В присут. оснований А. легко присоединяет по связи C—C вещества, имеющие подвижный атом Н (цианэтилирование). Восстанавливается H2 над никелем Ренея до пропионитри-ла, в избытке H2 — до пропиламина, при электрохим. гидро-димеризации превращ в адиподинитрил. Хлорируется до 1,2-дихлор- и 1,1,2-трихлорпропионитрила. Вступает в диеновый синтез, образуя ненасыщ. циклич. нитрилы. Под действием конц. H2SO4 превращ. в акриламид и акриловую кислоту.
Осн. пром. метод получения А. — окислит. аммонолиз пропилена (кат. — молибдаты или фосформолибдаты Bi, молибдаты или вольфраматы Те и Ce, оксиды Sb, U, Sn и Fe):
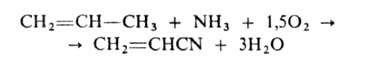
Процесс проводят при 400–485 °C и длительности контакта 2—4 с (стационарный кат.) и 10–20 с (псевдоожиженный кат.). Исходная смесь содержит 5–8% C3H6, 5–9% NH3, 0–30% водяного пара (остальное-воздух). Наряду с основной, сильно экзотермичной реакцией (ΔН = = −515 кДж/моль), происходит образование HCN, ацетонитрила, CO и CO2. Реакц. газы промывают горячим раствором (NH4)2SO4 в H2SO4 для связывания NH3, а затем-водой. Из водного раствора ректификацией выделяют А. и побочные товарные продукты-HCN и CH3CN. Выход А. 75–80% по пропилену.
А. получают также прямым присоединением HCN к ацетилену. Смесь C2H2 и HCN [мольное соотношение (5–10):1] барботируют через водный раствор, содержащий CuCl, HCl, KCl и NaCl, при pH 1–3, 70–90 °C и давлении, близком к атмосферному. А. очищают ректификацией; выход 80–90% по HCN.
А. используют в производстве полиакрилонитрильных волокон, АБС-пластиков, бутадиен-нитрильного каучука, сополимеров с винилхлоридом, стиролом (пластик САН) и др., цианэтилцеллюлозы, акриламида, метилакрилата, глутаминовой кислоты и адиподинитрила. Мировое производство А. более 2,5 млн. т/год (1980). А. обладает раздражающим действием, легко всасывается через неповрежденную кожу; токсич. действие подобно цианидам; ПДК 0,5 мг/м3, в воде водоемов-2 мг/л. Т. всп. 0 °C, т. воспл. 2 °C, т. самовоспл. 370 °C, КПВ 3–17%, температурные пределы воспламенения от −5 до 25 °C
Производство в СССР 209 тыс. т (1985).
Лит.: Далин М. А., Колчин И. К., Серебряков Б. Р., Нитрил акриловой кислоты, Баку, 1968; Бобков С. С., Смирнов С. К.. Синильная кислота, М, 1970; Теддер Дж., Нехватал А., Джубб А., Промышленная органическая химия, пер. с англ., М., 1977; Kirk-Othmer encyclopedia, 3 ed., v. I, N.Y.-[a.o.], 1978, p. 414–26.
С. К. Смирнов
Значения в других словарях
- Акрилонитрил — CH2 = CH — C ≡ N, органическое соединение, бесцветная жидкость с характерным запахом, tkип 77,3° С, плотность 806 кг/м3, растворима в воде, смешивается с большинством органических растворителей, легко полимеризуется в Полиакрилонитрил. В промышленности... Большая советская энциклопедия
- акрилонитрил — орф. акрилонитрил, -а Орфографический словарь Лопатина
- АКРИЛОНИТРИЛ — АКРИЛОНИТРИЛ — CH2=CHCN, бесцветная жидкость, tкип 77,3 °C. Сырье в производстве полиакрилонитрила, бутадиен-нитрильных каучуков, АБС-пластика и др. сополимеров. Большой энциклопедический словарь
