азиды органические
АЗИДЫ ОРГАНИЧЕСКИЕ
производные азотистоводородной кислоты HN3, в которой атом Н замещен на орг. радикал. Азидогруппа —N3 м. б. связана с атомом С, напр., в алкил- и арилазидах (диазоиминосоединениях) RN3, ацилазидах (диазоимидах) RC(O)N3, или с гетероатомом, напр. в азидах арилсульфокислот. Азиды (А.) могут содержать неск. азидогрупп в молекуле.
Названия А. образуют, прибавляя к названию радикала окончание "азид", напр. CH3Ы3-метилазид, C6H5C(O)N3-бензоилазид, или ставя перед названием соединения, радикал которого входит в А., приставку "азидо", напр. C6H5H3-азидобензол, НC(O)CH2N3-азидоацетальдегид.
Многие А. (особенно содержащие более 25% азидного азота) легко разлагаются; при сильном нагревании или ударе взрываются. А. раств. в органических растворителях, плохо — в воде.
Азидогруппа линейна. Ее конфигурация на примере CH3N3 приведена ниже:
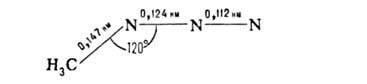
Строение группы —N3 промежуточное между тремя предельными структурами с преобладающим вкладом первых двух:
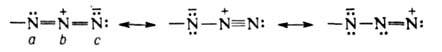
Атом Nb имеет гибридизацию sp, Na-sp2, Nc — spx (1 < x < 2).
В алифатич. соед. группа —N3 проявляет отрицат. индукционный эффект. С ароматич. кольцом может вступать в р, 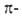 или
или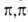 -сопряжение, проявляя соотв. положит. или сла-боотрицат. мезомерный эффект; константы Гаммета
-сопряжение, проявляя соотв. положит. или сла-боотрицат. мезомерный эффект; константы Гаммета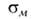 0,37,
0,37, 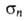 -0,08,
-0,08, 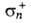 -0,54,
-0,54, 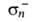 -0,11. Основные свойства проявляет атом Na.
-0,11. Основные свойства проявляет атом Na.
В ИК-спектрах арил- и алкилазидов проявляются асимметричные и симметричные валентные колебания в областях 2135–2090 и 1300–1270 см −1. В УФ-спектрах алифатич. А. имеются два максимума, напр. для C4H9N3 при 285 и 215.нм (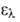 25 и 500 соотв.).
25 и 500 соотв.).
При наличии в молекуле А. ацильной, эфирной или сульфонильной группы, сопряженной с азидогруппой, степень двоесвязанности связи N—N2 понижается, облегчая ее разрыв:
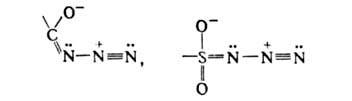
Такие А. менее стабильны, температуры разложения их ниже, а реакционная способность выше, чем у алкил- и арилазидов. Термич. и фотохим. разложение А. сопровождается выделением N2 (промежуточно образуются нитрены), напр.:
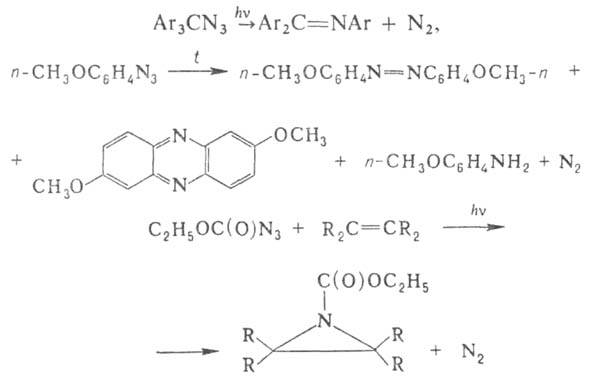
Отщепление N2 от ацилазидов при 20–150 °C в средах от нейтральной до сильнокислой сопровождается внутримол. перегруппировкой с образованием изоцианатов, которые мгновенно взаимод. с растворителем, напр. со спиртом образуют уретаны (см. Курциуса реакция).
В результате 1,3-диполярного циклоприсоединения А. к ненасыщенным соед. (диполярофилам) при температурах ниже температуры разложения А. образуются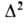 -1,2,3-триазолины (формула I) и 1,2,3-триазолы (II), напр.:
-1,2,3-триазолины (формула I) и 1,2,3-триазолы (II), напр.:
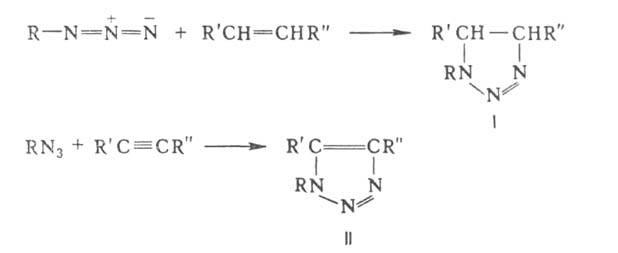
Циклоприсоединение А. к нитрилам приводит к тетразолам:
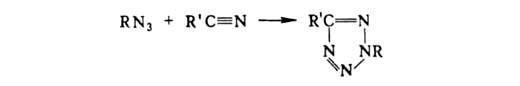
Алкил- и арилазиды при взаимодействии с реактивом Гриньяра превращаются в диазоаминосоединения:
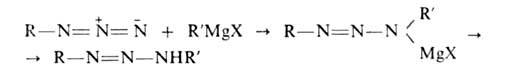
Ацилазиды гидролизуются разб. водными растворами кислот или оснований до карбоновых кислот и HN3.
А. получают действием NaN3 на алифатич. и ароматич. галогенсодержащие соед. [RHal, RSO2Hal, RC(O)Hal], напр.: RHal + NaN3 → RN3 + NaHal. Арилазиды синтезируют также по реакции:
[ArN=N] + Hal− + NaN3 → ArN3 + N2 + NaHal
Нитрозирование арилгидразинов или гидразидов карбоновых кислот приводит соотв. к арил- или ацилазидам, напр.:
ArNH—NH2 + HONO → ArN3 + H2O. Азидоформиаты получают при 0 °C в среде хлороформа:
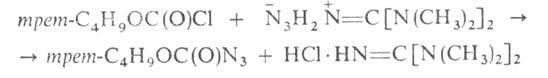
Количеств. определение азидогруппы в арил- и алкилазидах основано на восстановлении ее арсенат-иоыами до аминогруппы и иодометрич. титровании образовавшихся арсенит-ионов; в ацилазидах — на газометрич. определении N2, выделившегося при перегруппировке Курциуса. Колориметрически и фотометрически А. определяют по интенсивно красному окрашиванию с солями Fe(III).
А. используют для стерилизации масел (напр., бензил-азид, толилазид), как ацилирующие агенты аминокислот, в синтезе полипептидов, аминов (см. Шмидта реакция) и многих азотсодержащих ароматич. и гетероциклич. соединений. 2-Азидо-4-метилтио-6-изопропиламино-сим-триазин (азипротрин)-гербицид.
Лит.: Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 313–25; L'Abbe G., "Chem. Revs.", 1969, v. 69, №3, p. 345–63; Hedayatullah M., Hugueny J., "Synth. Commun.", 1981, v. 11, № 8, p. 643–46.
Р. Я. Попова
