Смайлса перегруппировка
СМАЙЛСА ПЕРЕГРУППИРОВКА
внутримол. анионотропная перегруппировка ароматич. соединений, происходящая в присутствии оснований по схеме:
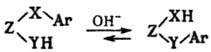
Х-обычно S, SO, SO2, О; YH = OH, NH2, NHR, SH; Z-цепочка, состоящая, как правило, из 2–3 атомов С Реакцию осуществляют при нагр. (50–100 °C) ароматич. соед. в растворе щелочи (растворители- вода, вода-этанол, вода-ацетон, вода — диоксан) от неск. минут до неск. часов. Известны примеры фотохим. С. п. Направление перегруппировки в осн. определяется относит. нуклеофильностью X и У.
Часто нуклеоф. центры X и Y находятся в орто-положениях по отношению друг к другу в бензольном кольце:
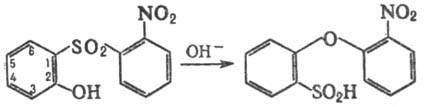
В таких случаях заместитель, введенный в положение 6 этого бензольного кольца (напр., CH3, Cl, Br), значительно ускоряет С.п., т. к. он обусловливает оптим. конформацию молекулы в переходном состоянии.
Нуклеофугные группы в орто-положениях арила соединений Ar-X-Z-YH и Ar-Y-Z-XH достаточно легко подвергаются внутримол. нуклеоф. замещению с образованием би- и полициклич. систем с двумя гетероатомами X и Y в одном цикле. При этом необходимо учитывать возможность протекания С. п. Так, o-гидроксидифенилсульфиды циклизуются в феноксатиины без С. п., а циклизации о-аминодифенил-сульфидов в фенотиазины предшествует С. п., напр.:
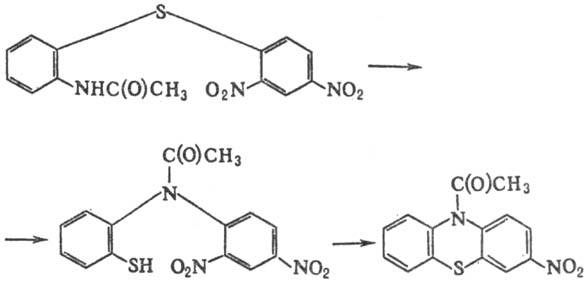
Механизм С. п. включает образование переходного состояния (формула I):
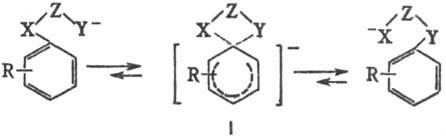
При наличии достаточного количества электроноакцепторных групп (напр., NO2) в орто- и пара-положениях мигрирующего арила (они ускоряют С. п.) промежут. анионные спи-рокомплексы. Майзенхаймера (I) довольно устойчивы.
Частный случай С. п. — перегруппировка Трюса (открыта В. Трюсом в 1958) о-толиларилсульфонов под действием литийорг. соединений в о-бензилсульфиновые кислоты:
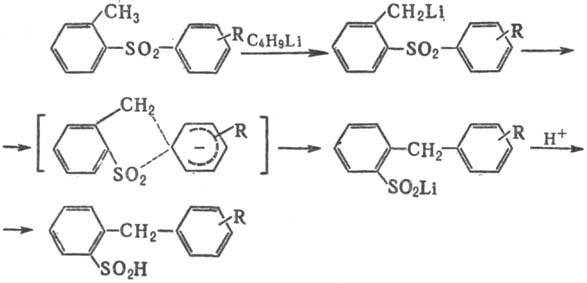
Перегруппировка изучалась С. Смайлсом начиная с 1930; несколько примеров аналогичных реакций было известно ранее.
Лит.: Марч Дж., Органическая химия, пер. с англ., т. 3, М., 1987, с. 44–45; Warren L. А., Smiles S., "J. Chem. Soc.", 1930, p. 956–63; Truce W. E., Kreider E. M., Brand W. W., в кн.: Organic Reactions, v. 18, N.Y., 1970, p. 99–215; Drozd V. N, "Int J. Sulfur Chemistry", 1973, v. 8, № 3, p. 443–67.
В. Н. Дрозд
