Реформатского реакция
РЕФОРМАТСКОГО РЕАКЦИЯ
получение эфиров β-гидроксикарбоновых кислот взаимод. альдегидов или кетонов с эфирами α-галогенкарбоновых кислот в присутствии Zη (т. наз. классическая P.p.):
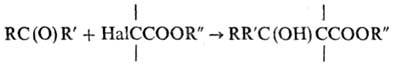
В реакцию вступают разл. альдегиды и кетоны (насыщенные или ненасыщенные, ароматические, галогензамещенные и др.). Второй компонент — обычно эфиры α-бромкарбоновых кислот (α-хлорэфиры малоактивны, а соответствующие иодиды малодоступны). Реакция экзотермична; ее осуществляют в безводном диэтиловом эфире, ТГФ или диоксане, либо в ароматич. растворителе (бензоле, толуоле, ксилоле и др.). Цинк (обычно в виде мелкодисперсного порошка) предварительно активируют; выходы реакции возрастают, если использовать амальгаму Zn или Zn, получаемый in situ при восстановлении его галогенидов интеркалатом калия в графите. Реакция инициируется с помощью I2 или CH3MgI. Выход эфиров β-гидроксикарбоновых кислот составляет 50–75%.
Механизм реакции включает образование промежут. цинкорг. соединений (реактива Реформатского), напр.:
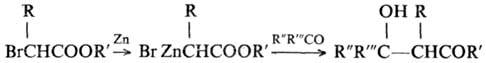
Осн. побочные реакции: 1) реакция Вюрца, в которую могут вступать галогенэфиры карбоновых кислот, напр.:
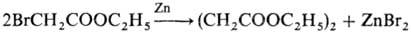
2) альдольная или кротоновая конденсация карбонильного соед., напр.:
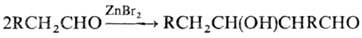
3) енолизация карбонильного соед., напр.:
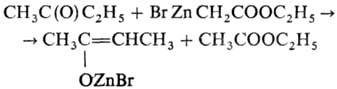
4) дегидратация β-гидроксиэфира карбоновой кислоты.
Последняя реакция в сочетании с P.p. может рассматриваться как метод синтеза α,β-ненасыщенных сложных эфиров карбоновых кислот.
Вместо эфиров β-гидроксикарбоновых кислот в P.p. могут использоваться их виншюги, а также др. соед., содержащие активир. атом галогена (напр., HalCH2C(O)NR2, HalCH2CH=CHCN, Hal3CCOOR). В этих случаях часто вместо Zn в качестве катализатора применяют Al (в этом случае реакцию наз. Также синтезам Годемара; разработана М. Годемаром в 1974).
При использовании винилогов эфиров α-галогенкарбоновых кислот (эта реакция м. б. использована для синтеза каро-тиноидов) образуются d-гидрокси-α,β-ненасыщенные кислоты:
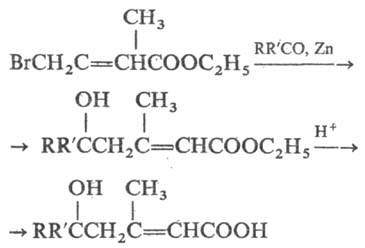
Сложные эфиры d-гидроксикислот при гидролиза легко дегидратируются или претерпевают ретроальдольный распад. Поэтому в этом синтезе обычно используют трет-бутиловые или триметилсилиловые сложные эфиры, которые гидролизуются до кислот в мягких условиях.
В орг. синтезе иногда используют соли лантаноидов, что позволяет осуществлять реакции, которые не идут в присутствии Zn, напр. с пространственно затрудненными ацетофенонами:
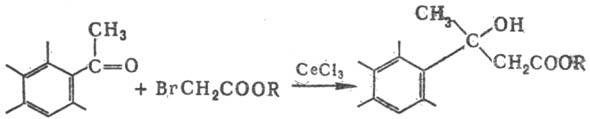
В реакции, подобной P.p., вместо альдегидов и кетонов используют др. карбонилсодержащие соед. (сложные эфиры, ангидриды и галогенангидриды кислот, кетены и др.), а также азометины. Таким путем получают мн. важные классы орг. веществ, напр. кетокислоты и лактамы:
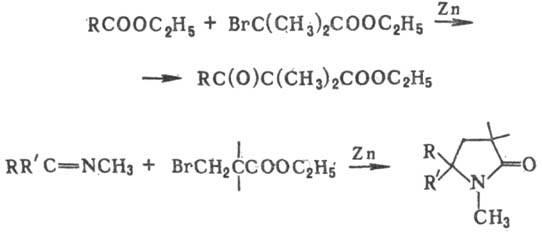
P.p. широко используют в лаб. синтезе. Реакция открыта С.Н. Реформатским в 1887.
Лит.: Шрайнер Р., в сб.: Органические реакции, пер. с англ., сб. 1, М., 1948, с. 9–52; Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 163–64; RathkeM.W., в сб.: Organic reactions, v. 22, N.Y.-[а.о.], 1975, p. 423–60; Houben-Weyl, Bd VII/2a, 1973, S. 599–600, 617; Bd VII/2b, 1976, S. 1972; "J. Org. Chem.", 1983, v. 48, № 22, p. 4108–111; Nagasawa K. [a.o.], "Tetrahedron Lett.", 1985, v. 26, № 52, p. 6477–80; Ogini N. [a.o.], "Chem. Express", 1987, v. 1, № 8, p. 495–98.
А. А. Соловьянов
Значения в других словарях
- Реформатского реакция — Синтез эфиров β-оксикарбоновых кислот (2) взаимодействием альдегидов или кетонов с эфирами α-галогенкарбоновых кислот (1) в присутствии металлического цинка: (X — галоген, R — органический радикал). Р. Большая советская энциклопедия
