Клайзена конденсация
КЛАЙЗЕНА КОНДЕНСАЦИЯ (ацилирование по Клайзену, сложноэфирная конденсация)
взаимод. сложных эфиров карбоновых кислот в присутствии основных катализаторов с соед., содержащими активную метиленовую группу, с образованием новой углерод-углеродной связи:
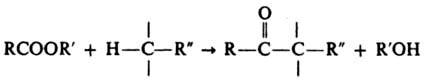
R и R'-opr. радикалы, R: — обычно COOAlk, C(O)Alk, CN. Для осуществления процесса исходные вещества и катализатор (напр., Na, AlkONa, NaNH2, NaH) кипятят в осушенном инертном растворителе (иногда до неск. сут). Для ускорения реакции в ряде случаев образующийся спирт отгоняют в вакууме. При самоконденсации сложных эфиров образуются β-кетоэфиры. Таким образом получают, напр., ацетоуксусный эфир:

При конденсации двух разл. эфиров (перекрестная К. к.) реакция проходит успешно, если один из реагентов не содержит активного атома водорода. Так, из этилформиата получают альдегидоэфиры (1), из этилбензоата-β-кетоэфиры (2), из диэтилоксалата — кетоэфиры или дикетодиэфиры (в зависимости от.соотношения реагентов) (3):
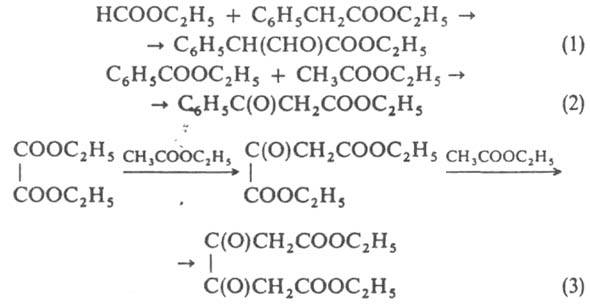
Чтобы избежать самоконденсации, реакцию проводят в избытке ацилирующего эфира. Если оба сложных эфира содержат активные атомы Н, образуется смесь четырех β-кетоэфиров, что существенно снижает выход продуктов перекрестной конденсации. С помощью диэтилоксалата или этилформиата можно также ацилировать этиловые эфиры кротоновой (n = 1) и сорбиновой (n = 2) кислот, напр.:
НCOOC2H5+CH3(CH=CН)nCOOC2H5:НС(O)CH2(CH=CН)nCOOC2H5
Реакцией сложных эфиров карбоновых кислот с кетонами получают р-дикетоны или β-кетоальдегиды:
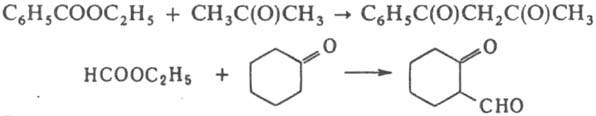
В случае эфиров дикарбоновых кислот происходит внутримол. конденсация (см. Дикмана реакция). К. к. обратима и по механизму близка к альдольной конденсации, напр.:
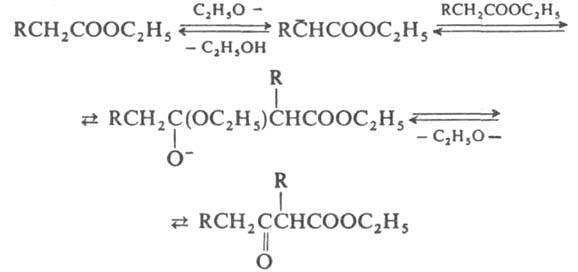
В реакцию, подобную К. к., вступают сложные эфиры минер. кислот, напр.:
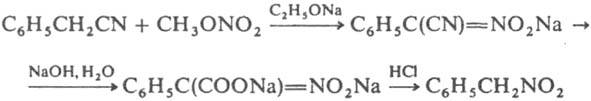
Выходы в К. к. достигают 80–90%. Побочные реакции взаимод. сложных эфиров с конденсирующими агентами, напр. аммонолиз при использовании в качестве катализа NaNH2 или образование ацилоинов при действии Na. к. широко применяют в промышленности для синтеза β-дикарбонильных соед., в т. ч. ацетоуксусного эфира и ацетилацетона. Реакция открыта А. Гёйтером в 1863 и подробно изучена Л. Клайзеном в 1887.
Лит.: Хаузер Ч. Р., Хадсон Б. Е. мл., в гн.: Органические реакции, пер. с англ., сб. 1, М., 1948, с. 345–98; Айрис Д. К., Карбанионы в органическом синтезе, пер. с англ.. Л., 1969, с. 131–34; Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 83, 106, 201, 323, 348.
С. К. Смирнов
Значения в других словарях
- Клайзена конденсация — Сложно эфирная конденсация, способ получения β-кето (или β-альдегидо) эфиров взаимодействием одинаковых или разных сложных эфиров в присутствии щелочных агентов. Типичный пример К. к. — получение ацетоуксусного эфира (См. Большая советская энциклопедия
