Бэмфорда — Стивенса реакция
БЭМФОРДА — СТИВЕНСА РЕАКЦИЯ
лаб. способ получения олефинов и (или) диазоалканов разложением тозилгидразонов под действием алкоголятов в протонных растворителях, напр.:
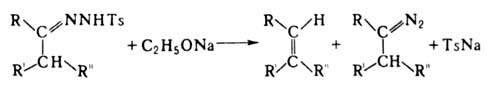
где R, R', R" — H, алкил или циклоалкил, арил; Ts-n-CH3C6H4SO2. При использовании тозилгидразонов неразветвленных линейных или циклич. кетонов с ненапряженным циклом выход соответствующих олефинов или цилоалкенов составляет 30–90%; в случае тозилгидразонов альдегидов выходы олефинов ниже, т. к. в значительных количествах образуются продукты побочных реакций — фрагментации, внедрения и перегруппировок. Диазосоединения образуются преим. из тозилгидразонов ароматич. ряда.
Считается, что механизм реакции включает депротонирование связи N—Н с последующим элиминированием n-то-лилсульфината и образованием диазосоединения (последняя стадия контролирует скорость реакции). Если образующееся диазосоединение в присутствии избытка основания способно достаточно быстро протонироваться, может возникнуть карбкатион и затем — продукты его превращений:

В случае неустойчивых диазосоединений (или же в отсутствие донора протонов) может образовываться карбен и далее — продукты его реакций.
Модификация Б. — С.р. (реакция Шапиро) — синтез замещенных олефинов последовательной обработкой сульфонилгидразонов альдегидов или кетонов алкиллитием (обычно CH3Li или C4H9Li) и электрофилом (напр., кислотой, алкилгалогенидом, альдегидом) в апротонном растворителе при температуре от −25 до −50 °C:
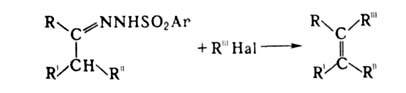
где Ar = Ph, n-CH3C6H4. Реакция открыта У. Р. Бэмфордом и Т. С. Стивенсом в 1952.
Лит.: Casanova J., Waegell В., "Bulletin de la Societe chimique de France", 1975. pt. 2, N 3–4, p. 922–32; Shapiro R. Н., в кн.: Organic reactions, v. 23, N.Y., 1976. p. 405–507.
А. М. Моисеенков
