Абрамова реакция
АБРАМОВА РЕАКЦИЯ
α-гидроксиалкилирование орг. гидрофосфорильных соед. (в т. ч. тиогидро- и иминогидрофосфорильных) альдегидами и кетонами в присутствии оснований (напр., алкоголятов или аминов) или кислот:
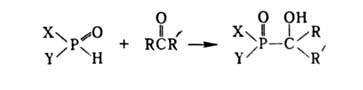
где X, Y-обычно R"O, R", R''2N, Н, ОН; R и R"-орг. радикалы; R'-орг. радикал или Н.
А. р. осуществляется по механизму нуклеоф. присоединения. При использовании фосфинистых кислот процесс протекает автокаталитически. Легкость протекания реакции определяется электрофильностью карбонильного соед.; напр., хлораль реагирует с диалкилфосфитами энергично и с саморазогреванием, альдегиды и кетоны, не содержащие в α-положении к карбонильной группе электроноакцепторных заместителей,-медленно. При нагревании в присутствии кислот продукты реакции часто распадаются до исходных веществ, а в присутствии оснований (В) претерпевают внутримолекулярную изомеризацию:
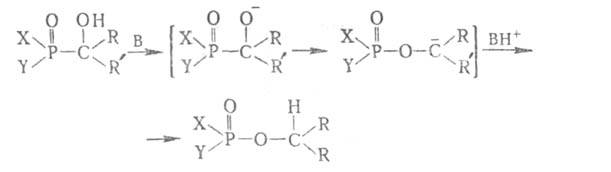
Важная модификация А. р. — взаимод. альдегидов и кетонов с силилфосфитами или силилфосфонитами:
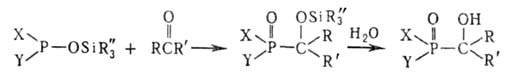
Родственный А. р. процесс-присоединение к альдегидам и кетонам фосфористой или фосфорноватистой кислоты, приводящее к α-гидроксифосфоновым, α-фосфонистым или α- фосфиновым кислотам.
А. р. применяют в промышленности, напр. для синтеза хлорофоса из диметилфосфита и хлораля.
Реакция открыта А. Е. Арбузовым и М. М. Азоновским в 1947 на примере взаимод. диэтилацетофосфоната с диэтилфосфитом Na, позднее подробно изучалась В. С. Абрамовым.
Лит.: Абрамов B.C., в кн.: Химия и применение фосфорорганических соединений, М., 1957, с. 218–22; Пудовик А.Н. [и др.], в кн.: Реакция и методы исследования органических соединений, кн. 19, М., 1968, с. 45–59; ThiemJ. [u.a.], "Chemische Berichte", 1977, Bd 110, № 9, S. 3190–3200; Wroblewski A., Konieczko W,. "Monatshefte fur Chemie", 1984, Bd 115, № 6/7, S. 785–91.
Э. Е. Нифаптьев
