Водородный показатель
Водоро́дный показатель
PH, отрицательный десятичный логарифм концентрации (точнее, активности) ионов водорода (в г-ион/л) в данном растворе:
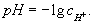
В. п. служит количественной характеристикой кислотности растворов, которая оказывает существенное влияние на направление и скорость многих химических и биохимических процессов. При обычных температурах (точнее, при 22 °С) pH = 7 для нейтральных, pH < 7 для кислых и pH > 7 для щелочных растворов. Точное измерение и регулирование pH необходимо как при лабораторных химических и биохимических исследованиях, так и в многочисленных промышленных технологических процессах, а также при оценке свойств почвы и проведении мероприятий по повышению её плодородия.
Вода диссоциирует на ионы по уравнению
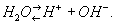
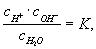
где с — молярные концентрации, а К — постоянная при данной температуре величина (1,8·10-16 г-ион/л при 22 °С). В 1 л воды содержится
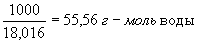
(количество диссоциировавших молекул настолько мало, что его можно не учитывать). Поэтому
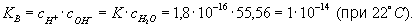
Константу КВ называют ионным произведением воды. Поскольку в чистой воде (и в любой нейтральной среде)
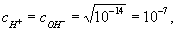
то
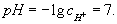
При добавлении к воде кислот cH+ возрастает, а pH соответственно уменьшается. Так, для 0,01 молярного (М) раствора HCl концентрация cH+ = 10-2 и pH = —lgcH+ = 2. Наоборот, при добавлении щелочей возрастает cOH-; тогда
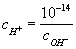
уменьшается и соответственно возрастает pH.
Например, в 0,01 М растворе NaOHcOH- = 10-2. Это значит, что
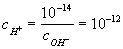
и pH = 12.
Для точных определений pH используют преимущественно методы потенциометрии (см. Электрохимические методы анализа). При определениях, не требующих высокой точности, pH измеряют б. ч. с помощью набора индикаторов, меняющих свою окраску каждый при определённом pH. Шкала pH обычно используется для растворов, имеющих концентрации ионов водорода от 1 г-ион/л и меньше.
Нейтральным водным растворам отвечает pH = 7 лишь при комнатных температурах. При повышении температуры диссоциация воды усиливается, KB возрастает, и при 100 °С чистая вода имеет pH — 6. При температурах ниже 22 °С в чистой воде pH > 7. При этом во всех случаях в нейтральной среде cH+ = cOH-.
Лит.: Киреев В. А., Краткий курс физической химии, 4 изд., М., 1969.
В. Л. Василевский.
Значения в других словарях
- водородный показатель — ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (рН) равен -lg aH, где aH-термодинамич. активность ионов H+ в растворе (в моль/л). В. п. — количеств. характеристика кислотности водных растворов. Вода диссоциирует на ионы H+ и OH−. Химическая энциклопедия
- водородный показатель — ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (рН), величина, характеризующая активную реакцию (кислотность) среды. Постоянство рН биол. жидкостей — необходимое условие нормального течения жизненных процессов (см. Кислотно-щелочное равновесие). В. Ветеринарный энциклопедический словарь
- водородный показатель — ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (pH) — величина, характеризующая концентрацию ионов водорода в растворах. Ботаника. Словарь терминов
- Водородный показатель — I Водородный показатель (рН) отрицательный десятичный логарифм активности, или концентрации, водородных ионов в растворе (—lg [H]). В. п. является основной количественной характеристикой кислотности водных растворов. Медицинская энциклопедия
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ — ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (обозначается рН), показатель кислотности или щелочности раствора. Шкала водородных показателей выражает ряд значений рН, основанных на логарифмическом измерении концентрации, или активности, ионов водорода. Научно-технический словарь
- водородный показатель — (рН) -параметр, характеризующий концентрацию водородных ионов в растворе, т. е. степень его щелочности или кислотности. Показатель рН может изменяться от 0 до 14. Раствор, в котором рН равно семи, является нейтральным, ниже семи — кислым, выше — щелочным. Толковый словарь по полиграфии
- Водородный показатель — PH (a. pH-value; н. pH-Wert; ф. pH valeur; и. valor del pH), — характеризует концентрацию (точнее активность) ионов водорода в растворах; численно равен отрицат. Горная энциклопедия
- ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ — ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (рН) — характеризует концентрацию (активность) ионов водорода в растворах; численно равен отрицательному десятичному логарифму концентрации (активности) водородных ионов (H+) — выраженной в молях на литр: рН=-lg(H+). Большой энциклопедический словарь
