КРИСТАЛЛОХИМИЯ
Раздел кристаллографии, в к-ром изучаются закономерности расположения атомов в кристаллах и природа хим. связи между ними. К. основана на обобщении результатов экспериментальных рентгенографич. и др. дифракц. методов исследований ат. структуры кристаллов (см. РЕНТГЕНОВСКИЙ СТРУКТУРНЫЙ АНАЛИЗ, ЭЛЕКТРОНОГРАФИЯ, НЕЙТРОНОГРАФИЯ), на классич. и квант. теориях хим. связи, на расчётах энергии крист. структур с учётом симметрии кристаллов. Кристаллохим. закономерности позволяют объяснить и в ряде случаев предсказать, исходя из хим. состава в-ва, расположение атомов или молекул в кристаллической решётке и расстояния между ними. Хим. связь между атомами в кристаллах возникает за счёт вз-ствия внеш. валентных электронов атомов. Равновесное расстояние между атомами обычно составляет 1,5—4 ? (в зависимости от типа хим. связи). При сближении атомов на расстояния, меньшие, чем равновесное, возникает резкое их отталкивание. Это позволяет в первом приближении приписать атомам для того или иного типа связи определ. «размеры», т. е. нек-рые пост. радиусы, и тем самым перейти от физ. модели кристалла как атомно-электронной системы к его геом. модели как системе несжимающихся шариков. Полное кристаллохим. описание ат. структуры того или иного кристалла включает указание размеров элем. ячейки, пространств. группы симметрии кристалла, координат атомов, расстоянии между ними, типа хим. связи; описания окружения атомов, характерных ат. группировок, тепловых колебаний атомов и т. п. По хар-ру хим. связи кристаллы делят на четыре осн. группы — ионные кристаллы (напр., NaCl), ковалентные (напр., алмаз, кремний), металлические (металлы и интерметаллич. соединения) и молекулярные кристаллы (напр., нафталин). 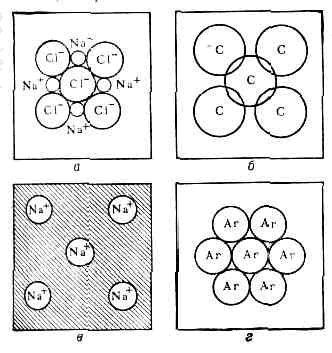
Осн. типы хим. связи в кристаллах: а — ионная связь; б — ковалентная связь; в — металлич. связь; г — связь за счёт сил Ван-дер-Ваальса.
В ионных кристаллах эл-ны переходят от атомов металлов, к-рые становятся положит. ионами (катионами), к атомам неметаллов, к-рые становятся отрицат. ионами (анионами), что приводит к электростатич. притяжению между ними (рис., а). В случае ковалентной связи валентные эл-ны соседних атомов обобществляются, образуя «мостики» электронной плотности между связанными атомами (рис., б). В металлич. кристаллах валентные эл-ны образуют общий электронный «газ», осуществляющий коллективное вз-ствие атомов кристалла (рис., в). Расстояния между атомами для этих трёх типов связи составляют 1,5—2,5 ?. В мол. кристаллах атомы внутри молекул объединены прочными ковалентными связями, а атомы соседних молекул взаимодействуют за счёт более слабых ван-дер-ваальсовых сил, (рис., г), имеющих диполь-дипольное и дисперсионное происхождение (см. МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ). Расстояние между атомами соседних молекул 3,5—4 ?. Во многих кристаллах связь имеет промежуточный хар-р, напр. в кристаллах полупроводников (Ge, GaAs) связь в осн. ковалентная, но с примесью ионной и металлической. В нек-рых кристаллах (напр., лёд, органич. кристаллы) существует т. н. водородная связь (см. МЕЖАТОМНОЕ ВЗАИМОДЕЙСТВИЕ).
Каждому крист. в-ву присуща определ. структура, но при изменении тсрмодинамич. условий она иногда может меняться (полиморфизм). Обычно чем проще ф-ла соединения, тем более симметрична его структура. Кристаллы с одинаковой хим. ф-лой (в смысле числа и соотношения разл. атомов) могут иметь одинаковую крист. структуру (говорят, что они образуют данный «структурный тип») несмотря на различие типов связи (и з о с т р у к т у р н о с т ь): изоструктурны галогениды щелочных металлов типа NaCl и нек-рые окислы (напр., MgO), ряд сплавов (напр., Ti— Ni). Есть большие серии изоструктурных соединений с ф-лой вида АВ2, АВ3, АВХ3 и т. п. Изоструктурны кристаллы мн. элементов, напр. g-Fe и Cu, образующие гранецентрированную кубич. решётку, но такую же структуру имеют и отвердевшие инертные газы. Если кристаллы изоструктурны и обладают одинаковым типом связи, то их называют изоморфными (см. ИЗОМОРФИЗМ). Во многих случаях между изоморфными кристаллами возможно образование непрерывного ряда твёрдых растворов.
В геом. модели кристалла К. использует концепцию эфф. радиусов атомов, ионов и молекул (к р и с т а л л о х и м и ч е с к и е р а д и у сы). На основе эксперим. данных о расстояниях между атомами в кристаллах построены таблицы кристаллохим. радиусов для всех типов связей, так что межат. расстояние равно сумме радиусов (св-во аддитивности кристаллохим. радиусов). Молекулы в органич. кристаллах предстают как бы окаймлённые «шубой» ван-дер-ваальсовых радиусов.
Осн. геом. представлением в К. явл. теория плотной упаковки, к-рая наглядно объясняет расположение атомов в ряде металлич. и ионных структур. В последнем случае используется представление о заселении «пустот» в упаковке анионов катионами, имеющими меньший ионный радиус.
В мол. кристаллах структурной ед. плотной упаковки явл. молекула. К. органич. соединений рассматривает правила плотной упаковки молекул, связь симметрии молекул и симметрии кристалла, типы органич. структур. Особые кристаллохнм. закономерности выявляются в структуре полимеров, жидких кристаллов, биологических кристаллов.
Координац. число К и вид координац. многогранника характеризуют хим. связь данного атома и структуры кристалла в целом. Напр., Be (за редкими исключениями) и Ge имеют тетраэдрич. окружение (K=4), у Аl и Cr координац. многогранник — октаэдр, у Pd и Pt — квадрат (K=4). Малые координац. числа указывают на значит. роль направленной ковалентной связи, большие — на большую роль ионной или металлич. связей.
Во многих крист. структурах (графит, MoS2 и др.) сосуществуют связи разл. типов. Такие структуры наз. гетеродесмическими, в отличие от гомодесмических — с однотипной связью (алмаз, металлы, NaCl, кристаллы инертных элементов). Для гетеродесмич. структур характерно наличие фрагментов, внутри к-рых атомы соединены более прочными (обычно ковалентнымп) связями. .Эти фрагменты могут представлять собой отд. «острова», цепи, слои, каркасы. Островные структуры типичны для мол. кристаллов. Часто в кач-ве «островов» выступают отд. молекулы и многоат. ионы (напр., SO-4, NO-3, СО-3) или ат. группировки типа РtСl6 в комплексных соединениях. Ряд кристаллов имеет цепочечное строение, типичный пример — кристаллы полимеров. Слоистую структуру имеют BN, MoS2, многие силикаты. Для нек-рых классов соединений характерно наличие устойчивых структурных группировок, сочетающихся в них по-разному. Так, в силикатах осн. структурный элемент — тетраэдрич. группировка SiO4 может выступать либо изолированной, либо образовывать пары, кольца, цепочки, слои и т. п.
Образование той или иной крист. структуры определяется общим принципом термодинамики: наиболее устойчива структура, к-рая при данном давлении и данной темп-ре Т имеет минимальную свободную энергию W= U-ST, где U — энергия связи кристалла (энергия, необходимая для разъединения кристалла на отд. атомы или молекулы) при T=0 К, S — энтропия.
Свободная энергия тем выше, чем сильнее связь в кристаллах. Она составляет 100—20 ккал/моль для кристаллов с ковалентной связью, несколько меньше у ионных и металлич. кристаллов и наиболее низка для мол. кристаллов с ван-дер-ваальсовыми связями (1—10 ккал/моль). Теоретич. определение свободной энергии и предсказание структуры пока возможны лишь для сравнительно простых случаев. Они проводятся в рамках зонной квантовой теории тв. тела. В ряде случаев достаточно точные результаты даёт использование полуэмпирич. выражений для потенц. энергии вз-ствия атомов в кристаллах с тем или иным типом связи.
Значения в других словарях
- кристаллохимия — Кристалл/о/хи́м/и/я [й/а]. Морфемно-орфографический словарь
- Кристаллохимия — Изучает пространственное расположение и химическую связь атомов в кристаллах (См. Кристаллы), а также зависимость физических и химических свойств кристаллических веществ от их строения. Будучи разделом химии, К. тесно связана с кристаллографией (См. Большая советская энциклопедия
- кристаллохимия — орф. кристаллохимия, -и Орфографический словарь Лопатина
- кристаллохимия — КРИСТАЛЛОХИМИЯ раздел химии, изучающий пространств. расположение и хим. связи атомов в кристаллах, а также зависимость физ. и хим. свойств кристаллич. веществ от их строения. Изучая влияние хим. состава вещества на его структуру... Химическая энциклопедия
- КРИСТАЛЛОХИМИЯ — КРИСТАЛЛОХИМИЯ — изучает зависимость структуры и свойств кристаллов от их химического состава. Большой энциклопедический словарь
