золото
ЗОЛОТО (Aurum) Au
хим. элемент I гр. периодической системы, ат. н. 79, ат. м. 196,9665; относится к благородным металлам. В природе один стабильный изотоп 197Au. Конфигурация внеш. электронной оболочки 5d106s1; степени окисления +1, +3, редко +5; энергии ионизации Au0 : Au+ : Au2+ : Au3+ соотв. равны 9,2258, 20,5 и 30,5 эВ; электроотрицательность по Полингу 2,4 сродство к электрону 2,8 эВ; атомный радиус 0,144 нм, ионные радиусы (в скобках указаны координац. числа) Au+ 0,151 нм (6), Au3+ 0,082 нм (4), 0,099 нм (6). Содержание 3. в земной коре 4,3–10 % по массе, в воде морей и океанов менее 5∙10−6 мг/л. Относится к рассеянным элементам. Известно более 20 минералов, из которых главный — самородное 3. (электрум, медистое, палладистое, висмутистое 3. и др.), представляющее собой твердый раствор Ag (от следов до 43%) в 3. и содержащее также Cu, Fe, Pb, реже — металлы платиновой группы, Mn, Bi и др. Хим. соединения 3. в природе редки, в осн. это теллуриды — калаверит AuТе2, креннерит (Au,Ag)Te2, сильванит AuAgTe4, петцит Ag3AuTe2, мутманнит (Ag,Au)Te, монтбрейит Au2Те3 и др. 3. присутствует гл. обр. в кварце, карбонатах, пирите, арсенопирите, галените, сфалерите, халькопирите. В рудах 3. присутствует в виде вкраплений размерами б. ч. 0,1–1000 мкм, иногда находят самородки до неск. десятков кг. Генетич. типы пром. месторождений 3.: гидротермальные высокотемпературные золото-арсенопиритовой формации; гидротермальные среднетемпературные кварц-сульфидной и золото-кварцевой формаций; гидротермальные низкотемпературные золото-серебряной формации; месторождения выветривания и метаморфизованные; аллювиальные россыпи. 3. извлекают из собственно золотых руд и, попутно, из железных, медных, свинцово-цинковых и урановых руд. Мировые пром. ресурсы 3. (без СССР) ок. 65 тыс. т.
Свойства. 3. — желтый металл; кристаллич. решетка гранецентрир. кубическая, а = 0,40786 нм, z = 4, пространственная группа Fm3m. Т. пл. 1064,4 °C, т. кип. 2880 °C; плотн. твердого 3. 19,32 г/см3, жидкого 17,22 г/см3 (1100 °C); С0p 25,39 Дж/(моль∙К); ΔH0пл 12,55 кДж/моль,ΔH0исп 348 кДж/моль; S0298 47,40 Дж/(моль∙К); уравнения температурной зависимости давления пара: для твердого 3. lgp (гПа) = 3,94 — 19820/T — 0,3061gT — 0,16∙10−3 Т (298–1337 Т), для жидкого lgp(Па) = 10,710 + 17866/Т (1337–3150 К); температурные коэф. линейного расширения (5,98–19,10)∙10−6 К−1 (40–1200 К), объемного (1,79–5,73)∙10−5 К−1 (40–1200 К); теплопроводность 318 Вт/(м∙К) при 273 К; ρ (2,06–2,84)∙10−8 Ом∙м (273–373 К), температурный коэф. ρ 4,0∙10−3 К−1 (273–373 К); диамагнетик, магн. восприимчивость —29,59∙10−6. З. — очень мягкий и пластичный металл, твердость по Моосу ~ 2,5, по Бринеллю 220–250 МПа; модуль упругости 81 ГПа; σраст 10–25 МПа. 3. устойчиво на воздухе и в воде; с O2, H2, N2, P, Sb и С непосредственно не взаимодействует. Фосфид Au2Р3 (ΔH0обр −102 кДж/моль) и антимонид AuSb2 (ΔH0обр −13 кДж/моль) получают косвенным путем. 3. не раств. в растворах щелочей и кислотах, раств. в горячей H2SeO4, смесях кислот — H2SO4 с HNO3, H2SO4 с НMnO4, а также в царской водке (HCl + HNO3): Au + HNO3 + 4HCl → H[AuCl4] + NO + 2H2O; после осторожного выпаривания выделяются желтые кристаллы комплексной золотохлористоводородной кислоты НAuCl4.3H2O. В водных растворах цианидов (Na, Ca, К) при доступе O2 или др. окислителей 3. раств. с образованием дицианоаурат-иона (цианирование): 2Au + 4CN− + H2O + 0,5O2 → 2[Au(CN)2]− + 2OH−, что лежит в основе важнейшего пром. способа извлечения 3. из руд. С галогенами в отсутствие влаги 3. без нагревания не взаимод., при нагр. порошка 3. в атмосфере галогенов образуются золота галогениды. С мн. металлами 3. дает сплавы. На легком образовании амальгамы 3. основан один из методов извлечения 3. из горных пород. Соед. золота неустойчивы, в водных растворах гидролизуются, легко восстанавливаются до металла. В табл. 1 приведены значения стандартных окислительно-восстановит. потенциалов E0 некоторых соед. AuLn (где L — лиганд, п = 1,3). Важнейшим соед. 3. посвящены отдельные статьи [см. Золота цианиды, Золотоорганические соединения, Калия дицианоаурат(I)], ниже приводятся сведения о других соединениях 3.
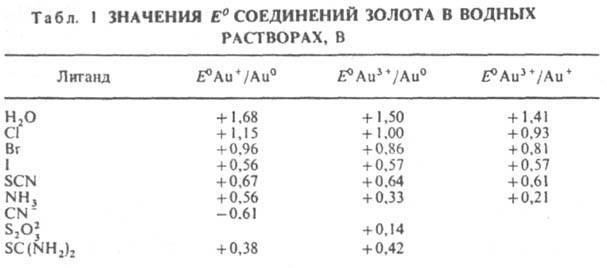
Гидроксид Au(OH)3 — темно-коричневые кристаллы; при нагр. дегидратируется с образованием сначала AuO(ОН), а затем сесквиоксида Au2O3, который выше 160 °C разлагается на 3. и O2; растворимость в воде 2,4∙10−12 моль/л при 20 °C, в растворах HNO3 — до 0,38 моль/л при 25 °C, в растворах NaOH — до 8∙10−4 моль/л при 25 °C. В последнем случае в растворе 3. находится в виде гидроксоаурат-ионов [Au(OH)4]− (pH 7–13). Образуется Au(OH)3 при добавлении конц. раствора щелочи или Mg(OH)2 к растворам Н[AuCl4]. Ауpaты неустойчивы, легко разлагаются при нагревании. Аураты щелочных металлов хорошо раств. в воде, растворимость растет с увеличением ионного радиуса катиона; аураты Mg, Ca, Sr, Ba, Tl(I) ограниченно растворимы. Аураты с некоторыми орг. веществами образуют взрывчатые смеси. Предполагают, что при действии на гидроксид 3. растворов щелочи образуются аурат-анионы [H2AuO3]−, [HAuO3]2−, [AuO3]3−. См. также табл. 2.
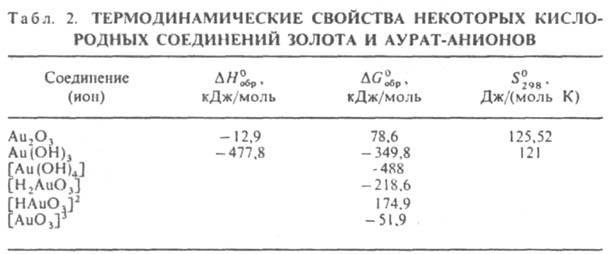
Др. кислородные соед. 3. неустойчивы, легко образуют взрывчатые смеси. Соед. Au2O3 с аммиаком Au2O3.4NH3 наз. "гремучим 3."; взрывается при 145 °C, иногда и при более низких температурах; без взрыва раств. в растворах цианидов щелочных металлов. Гемисульфид 3. Au2S — черно-коричневые кристаллы; ΔG0обр 29 кДж/моль; плохо раств. в воде (произведение растворимости 4∙10−69 при 25 °C), раств. в растворах цианидов и полисульфидов щелочных металлов. Получают взаимод. конц. раствора K[Au(CN)2] с H2S с послед. нагреванием до кипения с избытком соляной кислоты. Сесквисульфид Au2S3 — черные кристаллы; разлагается при нагр. до 200 °C; не раств. в соляной и серной кислотах, раств. в HNO3 с выделением элементарного 3., растворах KCN, бромной воде. Получают взаимод. H2S с AuCl3 или комплексными хлоридами 3. в безводном эфире на холоду. Известны комплексные соед., содержащие анионы [AuS3]2−, [AuS2]−, [AuS]−, [Au(SO3)2]3−, [Au(S2O3)2]3−. Моноселенид AuSe существует в двух кристаллич. модификациях моноклинной сингонии. При обработке солянокислых растворов 3. на холоду селеноводородом осаждается сесквиселенид Au2Se3.H2Se, устойчивый (после сушки) в интервале 40–390 °C; при 535–650 °C разлагается с выделением элементарного 3. Селенат (IV) Au2(SeO3)3.3H2SeO3 лимонно-желтые кристаллы; не раств. в воде, раств. в соляной и селенистой (при нагр.) кислотах. Селенат (VI) Au2(SeO4)3 желтые кристаллы; ΔH0обр −954 кДж/моль; не раств. в воде, разлагается соляной кислотой, раств. в H2SO4, HNO3 и горячей конц. H2Se04. Теллурид (гемителлурид) AuТе2 — кристаллы от латунно-желтого до серебристо-белого цвета с металлич. блеском; плотн. 9,3 г/см, ΔH0обр −11 кДж/моль; хрупок, твердость по Моосу 2,5–3. Тиоцианат AuSCN — бесцветные кристаллы; не раств. в воде и органических растворителях; при 140 °C разлагается до металлич. 3. и (SCN)n; под действием воды образует в растворах прочные комплексные анионы [Au(SCN)2]− и [Au(SCN)4]−. Коллоидное 3. При восстановлении 3. в разб. растворах его солей, а также при электрич. распылении 3. в воде образуются коллоидные растворы 3., окраска которых зависит от степени дисперсности частиц, а интенсивность окраски от их концентрации. Частицы 3. в коллоидном растворе отрицательно заряжены. Гидрофобный золь 3. в солянокислом водном растворе можно представить схемой:
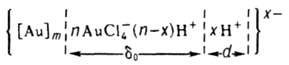
[Au]m — ядро мицеллы (число атомов т в зависимости от условий может меняться от неск. сотен до миллионов единиц); AuCl4− — ионы, определяющие отрицательный заряд коллоидной частицы 3. и величину потенциала адсорбц. слоя толщиной d0; H+ — противоионы, определяющие потенциал диффузионного слоя (электрокинетич. потенциал), из которых х ионов находится в размытой части двойного слоя толщиной d; n — количество ионов AuCl4−, адсорбированных на поверхности ядра мицеллы, при этом п << т.
Получение. Источники З. — руды и пески собственно золотых россыпных и коренных месторождений (содержание 3. в них 5–15 г/т), а также промежут. продукты (0,5–3 г/т) свинцово-цинкового, медного, уранового и некоторых др. производств. Из россыпей 3. извлекают гравитац. методами, используя т. н. ловушки, отсадочные машины, концентрац. смолы, шлюзы, разл. промывочные приборы. Со дна рек и озер золотоносные пески добывают и обогащают на драгах. При извлечении 3. из коренных руд используют комбинир. схемы, включающие обогатительные (гравитация, флотация) и металлургические (выщелачивание, ионообменная сорбция из пульп, цианирование, реже амальгамирование) операции. При использовании цианирования измельченную руду или концентрат обрабатывают раствором NaCN при перемешивании; из цианистых растворов 3. осаждают порошком Zn, с помощью ионообменных смол или активир. углей. Конечные продукты схемы — обычно гравитационный концентрат (т. н. золотая головка) и черновое 3. Очищают 3. растворением в царской водке с послед. избират. осаждением (напр., с помощью FeSO4), хлорированием в расплаве или растворе (хлоринация) и электролитич. рафинированием в солянокислом растворе.
Определение. Качественно 3. обнаруживают по образованию окрашенных осадков и растворов. Используют реакции соед. 3. с Hg2Cl2, H2O2, SnCl2, K4[Fe(CN)6], KI, бснзидином, 1-нафтиламином, о-толуидином, гваяковой смолой, комплексоном III, аскорбиновой кислотой, фенилтиомочевиной, дитизоном, родамином, изохинолином и др. Можно использовать сорбцию на ионообменных смолах, а также методы электрофореза, хроматографии (круговой тонкослойной, осадительной и распределительной), люминесценции. Количественно 3. определяют гравиметрически (в виде металлич. 3.), титриметрически (восстановлением Au3+ с послед. титрованием избытка восстановителя), фотометрически (по оранжевой окраске бромаурат-иона, а также по интенсивной окраске соед. 3. с разл. орг. реагентами), электрохимически, спектральными методами, методами активац., атомно-абсорбц. и пробирного анализов. Для предварит. концентрирования 3. используют хим. методы, жидкостную экстракцию и хроматографию.
Применение. 3. — валютный металл, выполняет функцию всеобщего эквивалента денег. 3. и его сплавы используют для декоративных целей, изготовления ювелирных изделий, монет, медалей, зубных протезов, деталей хим. аппаратуры, электрич. контактов и проводов, изделий микроэлектроники, для плакирования труб в хим. промышленности, в производстве припоев, катализаторов, часов, для окрашивания стекол, изготовления перьев для авторучек, нанесения покрытий на металлич. поверхности (в самолетостроении, космич. технике и др. областях). Искусств. радиоактивный изотоп 198Au (T1/2 2,967 сут) используют для лечения опухолей в радиотерапии. Мировое производство 3. (без СССР) ок. 1100 т/год (1984). Осн. производители — ЮАР, СССР, Канада, США, Бразилия, Австралия. Некоторые препараты Au(I) токсичны, накапливаются в почках, в меньшей мере — в печени, селезенке и гипоталамусе; накопление 3. в почках может привести к их заболеванию, а также к дерматитам, стоматитам, тромбоцитопении. 3. было известно человеку уже в древнейшие времена; возможно, что оно явилось первым металлом, который человечество стало применять для своих потребностей. Имеются данные о добыче 3. и изготовлении из него разл. изделий в Египте (4100–3900 до н. э.), Индии, Индокитае (2000–1500 до н. э.) и др.
Лит.: Бусев А. И., Иванов В. М., Аналитическая химия золота, М., 1973; Малышев В. М., Румянцев Д. В., Золото, М., 1979; Паддефет Р., Химия золота, пер. с англ., М., 1982; Благородные металлы. Справочник, под ред. Е. М. Савицкого, М., 1984; Марфунин А. С., История золота, М., 1987.
В. С. Стрижко, М. А. Меретуков
Значения в других словарях
- золото — -а, ср. 1. Химический элемент, благородный металл желтого цвета, обладающий большой ковкостью и тягучестью (употребляется для выделки драгоценных изделий и в качестве мерила ценности). 2. собир. Изделия из этого металла, золотые вещи. Малый академический словарь
- золото — Зо́лот/о. Морфемно-орфографический словарь
- Золото — (лат. Aurum) Au, химический элемент 1 группы периодической системы Менделеева; атомный номер 79, атомная масса 196,9665; тяжёлый металл жёлтого цвета. Состоит из одного устойчивого изотопа 197Au. Историческая справка. Большая советская энциклопедия
- золото — орф. золото, -а Орфографический словарь Лопатина
- золото — Древнерусское – золото. Старославянское – злато. Общеславянское существительное zolto пришло из индоевропейского языка со значением «желтый». В памятниках древнерусского периода встречается с X... Этимологический словарь Семёнова
- Золото — 1) драг. металл, к-рый в ветхозаветные времена ввозился в Палестину из Хавилы (Быт 2:11), Савы (3Цар 10:1 и след.), Аравии (Пс 71:15) и Офира (3Цар 9:28). В евр. языке для обозначения З., помимо наиб. употребит. Библейская энциклопедия Брокгауза
- золото — 1) ружье; 2) пустота в душе Словарь воровского жаргона
- Золото — (англ. gold), один из первых металлов, освоенных человеком. Встречаясь в природе в виде самородков и золотого песка, З. не требует плавки. Как мягкий и редко встречающийся металл... Археологический словарь
- Золото — (Быт 2:11-12) — весьма твердый по составу, красивый по виду и ценный металл, «имя одной (реки) Фисон, — повествует свящ. бытописатель, — она обтекает всю землю Хавила, ту, где золото, и золото той земли хорошее» (Быт 2:11-12). Библейская энциклопедия архим. Никифора
- золото — На вес золота Словарь синонимов Абрамова
- Золото — • Aurum (ср. Argentum и nummi, Монеты), шло и в сыром, и в обработанном виде, особенно как украшение, на цепочки, запястья, драгоценные вещи, оружие и пр., но также на сосуды и утварь всякого рода. Как монета, оно называлось обыкновенно signatim. A. Словарь классических древностей
- золото — З’олото — известный с древнейших времен драгоценный металл, применявшийся для украшений и как эквивалент денег. Скиния и храм были внутри полностью отделаны и украшены золотом (Исх.25:11 -18,24-31,38-39; 3Цар.6:20 -22,28,30,32,35). Библейский словарь Вихлянцева
- золото — сущ., с., употр. часто (нет) чего? золота, чему? золоту, (вижу) что? золото, чем? золотом, о чём? о золоте 1. Золотом называют химический элемент (Au), благородный мягкий металл жёлтого цвета. Добыча золота. | Украшение из золота. Толковый словарь Дмитриева
- золото — Общеслав. Суф. производное (суф. -т-, ср. болото) от той же основы (с перегласовкой е/о), что и желтый. Корень тот же, что в лит. želtas «золотой, желтый», нем. Gold «золото» и т. д. Исходное *zolto > золото в результате развития полногласия, ср. Этимологический словарь Шанского
- Золото — Au (лат. Aurum * a. gold; н. Gold; ф. or; и. oro), — хим. элемент I группы периодич. системы Mенделеева; ат. н. 79, ат. м. 196,967. Природное З. состоит из стабильного изотопа 197Au. Горная энциклопедия
- ЗОЛОТО — ЗОЛОТО (символ Аu), встречающийся в природе ПЕРЕХОДНЫЙ ЭЛЕМЕНТ. Встречается как побочный продукт электролитической облагороженной меди. Научно-технический словарь
- Золото — В геральдике название золотого цвета. (Архитектура: иллюстрированный справочник, 2005) Архитектурный словарь
- золото — • Всемогущее (Барыкова). • Всесильное (Садовников). • Могучее (Иванов-Классик). • “О золото крылатое, о золото парящее! • “О золото несытое, жестокое и мстящее! • “О золото лучистое, сквозь темный вихрь горящее! • “О золото живое. • “Лукавое, глухое!” (Брюсов, Верхарн). Словарь литературных эпитетов
- золото — ЗОЛОТО -а; ср. 1. Химический элемент (Au), благородный тяжёлый мягкий ковкий металл жёлтого цвета (широко используется в промышленности, медицине, ювелирном деле и т. п.). Добывать з. Хранить з. в слитках. Поставить зубные коронки из золота. Толковый словарь Кузнецова
- золото — ЗОЛОТО, а, ср. 1. Драгоценный металл жёлтого цвета, употр. как мерило ценностей и в драгоценных изделиях. Чистое з. Ювелирные изделия из золота. Не всё то з., что блестит (посл.). Червонное з. Чёрное з. (о нефти). Мягкое з. (о ценных мехах пушных зверей). Толковый словарь Ожегова
- золото — З’ОЛОТО, золота, мн. нет, ср. 1. Один из благородных металлов, желтого цвета, употр. для драгоценных изделий и как мерило ценности. Браслет из чистого золота. Золото высокой пробы. Червонное золото. 2. собир. Изделия из золота. Сундуки полны золота. Толковый словарь Ушакова
- золото — Это слово имеет родню во многих других индоевропейских языках (среди этой родни и английское gold, и немецкое Gold, и латышское zelts). Этимологический словарь Крылова
- золото — золото I ср. 1. Один из благородных металлов жёлтого цвета, отличающийся мягкостью и пластичностью. 2. разг. Изделия из такого металла. 3. Золотые монеты, деньги. || перен. разг. Богатство. 4. Позолоченные шелковые нити для вышивания или ткачества. Толковый словарь Ефремовой
- ЗОЛОТО — ЗОЛОТО — в экономике — драгоценный металл; естественные свойства золотa — однородность, делимость, сохраняемость... Большой энциклопедический словарь
- золото — зо́лото прилаг. золото́й, укр., блр. зо́лото, ст.-слав. злато χρυσός (Супр.), болг. злато́, сербохорв. зла̑то, словен. zlatȏ, чеш., слвц. zlato, польск., в.-луж., н.-луж. zɫоtо. Родственно вост.-лит. žеl̃tаs "золотой", "золотисто-желтый", лтш. Этимологический словарь Макса Фасмера
- золото — ЗОЛОТО, злато ср. самый дорогой крушец (металл), находимый в самородном виде, т. е. не в руде. Червонное золото, чистое, одной пробы с червонцами. Красное золото, с медным сплавом; белое, с серебряным сплавом, также || платина. Толковый словарь Даля
