дистилляция
ДИСТИЛЛЯЦИЯ (перегонка) (от лат. distillatio — стекание каплями)
разделение жидких смесей на отличающиеся по составу фракции. Основана на различии в составах жидкости и образующегося из нее пара. Осуществляется путем частичного испарения жидкости и послед. конденсации пара. Отогнанная фракция (дистиллят) обогащена относительно более летучими (низкокипящими) компонентами, а неотогнанная жидкость (кубовый остаток) — менее летучими (высококипящими). Если из исходной смеси отгоняется не одна фракция, а несколько, Д. наз. фракционной (дробной). Дистилляц. установка состоит из испарителя 1, снабженного теплообменным устройством для подвода к раствору необходимого количества теплоты; дефлегматора 2 для частичной конденсации пара, выходящего из испарителя (при фракционной Д.); конденсатора 3 для сжижения отбираемого пара; холодильника 4; сборников дистиллята 5 и кубового остатка 6 (рис. 1). В зависимости от условий процесса различают простую и молекулярную Д.
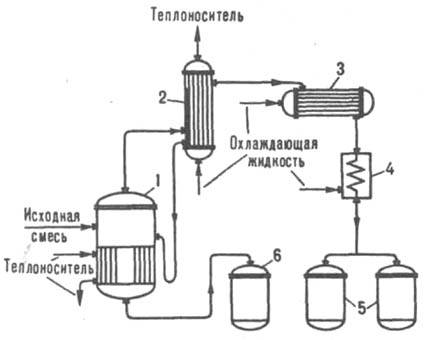
Рис. 1. Дистилляционная установка: 1 — испаритель; 2 — дефлегматор; 3 — конденсатор; 4 — холодильник; 5, 6 — сборники соотв. дистиллята и кубового остатка.
Простая дистилляция. Проводится при таких давлениях, когда длина своб. пробега молекул во много раз меньше, чем расстояние между поверхностями испарения жидкости и конденсации пара. Температура процесса при заданном давлении определяется условиями фазового равновесия между жидкостью и паром. При необходимости снижения температуры применяют Д. под вакуумом, а также с водяным паром или инертным газом (см. ниже). Распределение компонентов смеси между жидкостью и паром характеризуется коэф. относит. летучести:
αik = (yi/xi):(yk/xk), (1)
где хi и xk, уi и yk — содержания компонентов i и k соотв. в жидкости и образующемся из нее паре. Состав последнего определяется свойствами и межмолекулярным взаимод. компонентов. При небольших давлениях, когда пар с достаточной для практич. целей точностью подчиняется законам идеальных газов, в состоянии равновесия
αik = (pi0/pk0) (γi/γk), (2)
где pi0 и pk0 — давления паров чистых компонентов i и k при температуре кипения смеси, γi и γk — коэф. активности этих компонентов в жидкой фазе. При высоких давлениях учитывается неидеальность пара. Д. осуществляется периодически (исходная смесь загружается в аппарат однократно или подается в него в течение определенного времени, дистиллят отбирается в ходе процесса, а кубовый остаток выгружается после его завершения) или путем непрерывных подачи исходной смеси и отбора продуктов разделения (дистиллята и кубового остатка). Взаимосвязь количества W0и и расхода Wн исходной смеси, расхода отводимого в конденсатор пара G, количеств дистиллята Wд и кубового остатка Wк, а также содержаний произвольного i-го компонента в исходной смеси xiи, дистилляте хiд и кубовом остатке хiк выражается уравнениями материального баланса. При постоянном Wн/G = Y
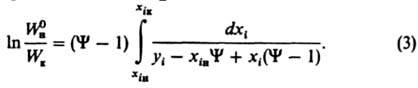
При однократной загрузке смеси (Y = 0) количество жидкости в аппарате изменяется от W0н до Wк, и уравнение (3) приводится к уравнению Рэлея:
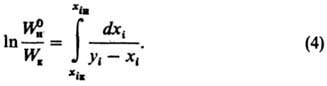
При непрерывной Д. расходы и составы исходной смеси и продуктов разделения связаны след. уравнениями:
Wи = Wк + Wд; Wиxiн = Wкxiк + Wдxiд. (5)
При расчете Д. всегда бывают заданы количество (или расход) исходной смеси, ее состав, а также условия, определяющие конечный результат процесса. В соответствии с его назначением м. б. заданы количество (или расход) кубового остатка (искомые величины — Wд, xiд и xiк), состав дистиллята xiд (хiк, Wд и Wк) либо кубового остатка xiк ( Wд, Wк и xiд). Неизвестные параметры рассчитывают совместным решением уравнений материального баланса с учетом зависимости между составами контактируемых пара (yi) и жидкости (xi). Эта зависимость определяется свойствами смесей, условиями процесса и его аппаратурным оформлением. Аппараты, применяемые для Д., делят на емкостные и пленочные. В емкостных аппаратах находится большой объем жидкости, интенсивно перемешиваемой в результате кипения. Состав образующегося пара близок к равновесному и определяется по уравнению:
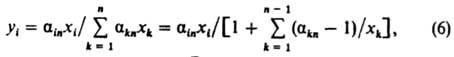
где n — число компонентов. Эти аппараты используют как для периодич., так и для непрерывной Д. В первом случае содержание низкокипящих компонентов в паре постепенно убывает, и средний состав дистиллята является промежуточным между составами паров, находящихся в равновесии с исходной смесью, и кубовым остатком. Во втором случае состав жидкости в аппарате практически идентичен составу кубового остатка, а состав дистиллята — составу равновесного с этой жидкостью пара. Поскольку дистиллят получается в результате парообразования из смеси конечного состава с наименьшим содержанием низкокипящих компонентов, вемкостных аппаратах при непрерывной Д. достигается меньшая степень разделения смеси, чем при периодич. Д. При расчете Д. n-компонентной смеси обычно задано распределение одного или неск. целевых компонентов между дистиллятом и кубовым остатком или относит. количество отгоняемого дистиллята. В общем случае имеется 2n −1 неизвестных: п — 1 значений хiд, п — 1 значений xik и Wк или Wд. Для их определения при расчете периодич. Д. имеются n уравнений материального баланса (для всего процесса в целом и для n −1 отдельных компонентов) и п −1 уравнений (3), которые должны быть решены совместно с п −1 уравнениями фазового равновесия (6). Следовательно, необходимо решить систему 2n −1 уравнений, из которых n уравнений — алгебраические, а п −1 — интегральные. Аналит. решение такой задачи чрезвычайно сложно, поэтому расчеты выполняются численными методами. При этом приходится задаваться относит. содержанием всех компонентов в одном из продуктов разделения (дистилляте или кубовом остатке). Наиб. простой метод — поинтервальный, который заключается в совместном решении уравнений, описывающих условия фазового равновесия, и уравнений материального баланса (3) и (4), записанных в конечных разностях. Для одного интервала ΔW/W принимается определенное значение относит. изменения количества дистиллируемой жидкости и последовательно вычисляется изменение ее состава, т. е. для каждого интервала находится изменение содержания всех компонентов Δxi. В первом приближении состав пара уi рассчитывается по уравнениям (6) как равновесный с жидкостью, состав которой соответствует началу интервала. Расчет заканчивается при достижении заданного распределения целевых компонентов между дистиллятом и кубовым остатком. Состав дистиллята находится усреднением составов пара, получающегося во всех последовательных интервалах. Критерий правильности расчета — совпадение этого среднего состава дистиллята с найденным по уравнениям материального баланса. При непрерывной Д. n-компонентной смеси состав дистиллята, совпадающий с составом пара, образующегося при кипении кубовой жидкости (хiд = уi), вычисляется по уравнениям (6), в которых хi и xk — содержания компонентов i и k в кубовом остатке. Таким образом, получается система 2n-1 алгебраич. уравнений, связывающих 2n величин: Wд, Wк, n — 1 значений хiд и п −1 значений хiк. Чтобы сделать эту систему уравнений определенной, достаточно задать любую из перечисл. величин. Ввиду нелинейности уравнений (6) аналит. решение практически невозможно и приходится использовать численные методы. Д. многокомпонентных смесей рассчитывают с применением ЭВМ. В пленочных аппаратах жидкость распределяется по поверхности нагрева в виде пленки. По способу ее образования различают: аппараты с жидкостью, свободно стекающей по обогреваемой поверхности (напр., по поверхности труб) с помощью спец. распределит. устройств (рис. 2, а, б), а также с восходящим движением жидкости за счет силы трения на границе между жидкостью и паром, движущимся снизу вверх с достаточно большой скоростью; роторные — с жидкостью, "размазываемой" по внутр. поверхности обогреваемого корпуса при вращении ротора с неподвижными или подвижными лопастями (рис. 2, в). По характеру относит. движения фаз пленочные аппараты подразделяют на прямо- и противоточные. Объем и время пребывания жидкости в пленочных аппаратах очень малы, поэтому они используются только для непрерывной Д. и особенно эффективны при перегонке термолабильных веществ и вязких растворов. Состав жидкости в пленочных аппаратах изменяется по высоте, что обусловливает изменение температуры и состава пара. Жидкость и пар, проходящие через произвольное сечение аппарата, не находятся в равновесии и между ними происходит тепло- и массообмен. Скорость и влияние последних на результаты процесса определяются скоростями и характером относит. движения фаз. Уравнение материального баланса для элемента высоты аппарата dh имеет вид:
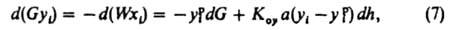
где G и W — расходы пара и жидкости, yip — содержание компонента i в паре, находящемся в равновесии с жидкостью состава xi, уi — состав пара, проходящего через рассматриваемое сечение аппарата, Kоу — коэф. массопередачи, а — площадь поверхности массообмена на единицу высоты аппарата.
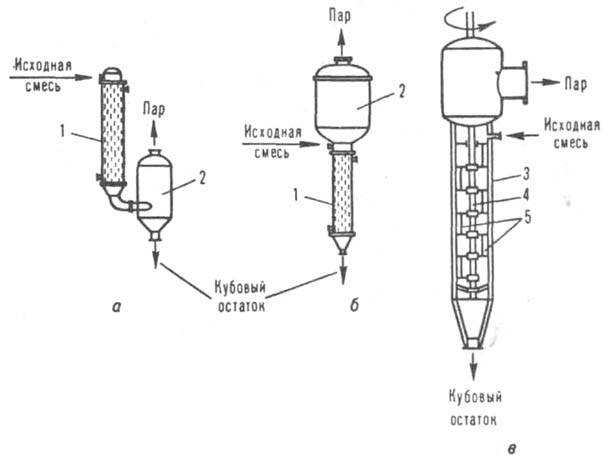
Рис. 2. Аппараты для простой дистилляции: a, б — соотв. прямо- и противоточные со стекающей жидкой пленкой; в — роторный; 1 — испаритель; 2 — сепарационный сосуд; 3 — обогреваемый корпус; 4 — вал; 5 — лопасти.
При немедленном отводе образующегося пара (тепло- и массообмен с жидкостью исключены) уравнение (7) превращается в уравнение простой Д. Поскольку Kоу > 0, знак второго слагаемого в правой части этого уравнения зависит от характера относит. движения фаз. Вследствие преимуществ. превращения в пар относительно более летучих компонентов содержание их в жидкости постепенно снижается, и она обогащается относительно менее летучими компонентами. Соотв. уменьшается содержание низкокипящих компонентов в равновесном паре. Поэтому при одинаковом направлении движения жидкости и пара последний поступает в произвольное по высоте сечение аппарата с содержанием низкокипящих компонентов уi, превышающим их содержание уip в паре, равновесном с жидкостью, которая проходит через то же сечение. Из-за градиента концентраций уi-уip возникают поток относительно более летучих компонентов из пара в жидкость и встречный поток относительно менее летучих компонентов из жидкости в пар. При большой скорости массообмена состав пара на выходе из аппарата приближается к равновесному с жидкостью конечного состава. При встречном движении фаз через произвольное сечение аппарата проходит пар с меньшим содержанием низкокипящих компонентов, чем отвечающее равновесию с жидкостью в этом сечении. Поэтому благодаря массообмену из жидкости в пар переходят гл. обр. низкокипящие, а в противоположном направлении — высококипящие компоненты. В результате на выходе из аппарата пар по составу приближается к равновесному с исходной смесью, имеющей наиб. содержание низкокипящих компонентов, т. е. достигается дополнительное по сравнению с простой Д. разделение смеси. Расход теплоты на простую Д. определяется по уравнению теплового баланса. Площадь поверхности нагрева испарителя находится из уравнения теплопередачи с учетом изменения коэф. теплопередачи и разности температур теплоносителя и кипящей жидкости с изменением ее состава во времени (при периодич. Д.) или по высоте (при непрерывной Д.). При Д. с дефлегмацией (конденсация преим. высококипящих компонентов при охлаждении смесей с целью их обогащения низкокипящими компонентами) связь состава пара уi, поступающего из испарителя в дефлегматор (рис. 1), с составами возвращаемой жидкости (флегмы) хiф и пара уiф, направляемого в конденсатор, определяется конструкцией и режимом работы дефлегматора. Обычно принимают, что выходящие из него жидкость и пар находятся в равновесии. Тогда взаимосвязь xiф и yiф описывается уравнением (6), а количества и состава жидкости в аппарате — уравнением (4), в которое вместо уi подставляют уiф. Большая, чем при простой Д., степень разделения смеси достигается благодаря частичной конденсации пара, образующегося в испарителе, и соответствующего увеличения расхода теплоты. Для отгонки из смесей высококипящих веществ с целью понижения температуры процесса используют Д. с водяным паром или инертным газом. Она основана на законе Дальтона, согласно которому давление паров над смесью р равно сумме парциальных давлений паров компонентов. Если отгоняемое вещество А не смешивается с водой, то р = рA0 + pв (рA0 — давление пара чистого вещества А при температуре процесса, pв — давление водяного пара), т. е. общее давление является линейной функцией рв, и вещество А можно отгонять при любой температуре, варьируя относит. расход водяного пара или инертного газа Gуд. Последний определяется соотношением:
Gуд = pвMв/рA0MAj, (8)
где Mв и MА — молекулярная масса воды (инертного газа) и отгоняемого вещества, j < 1 — степень насыщения водяного пара или инертного газа парами отгоняемого вещества по сравнению с равновесной степенью насыщения. При Д. в токе водяного пара образуется паровая смесь, которая затем конденсируется и охлаждается. Конденсат разделяется в сепараторе на отогнанный компонент и воду. Целевой продукт выделяется из конденсата тем легче и полнее, чем меньше его растворимость в воде. Если она значительна, приходится отгонять из воды целевой продукт и подвергать его осушке (применяют и др. способы, напр., высаливание). Эти затруднения отпадают при использовании инертного газа. Однако усложняется выделение отгоняемого вещества из образующейся парогазовой смеси вследствие необходимости охлаждения ее до низкой температуры, а нагревание и охлаждение газа требуют применения теплообменных аппаратов с большой площадью поверхности из-за низких коэф. теплоотдачи от стенки к газу и от газа к стенке. Поэтому данный метод применяется, когда Д. под вакуумом затруднительна или невозможна и проводится в емкостных аппаратах, снабженных барботажными устройствами для равномерного распределения пара или газа в объеме жидкости.
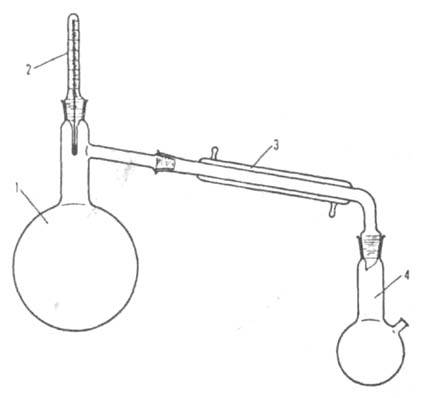
Рис. 3. Лабораторная установка для простой дистилляции: 1 — перегонная колба; 2 — термометр; 3 — холодильник (конденсатор); 4 — сборник дистиллята.
При простой Д. контролируются количество жидкости в аппарате, температура ее кипения, по которой судят о составе, и скорость отгонки дистиллята. Регулируемые параметры — количество исходной смеси, расходы теплоносителя, подаваемого в дистилляц. аппарат, и хладагента, используемого для конденсации отгоняемого пара и охлаждения конденсата. При Д. в токе водяного пара регулируется также его расход. При непрерывной Д. регулируемыми параметрами, кроме перечисленных, являются расходы исходной смеси и продуктов разделения. При Д. с дефлегмацией дополнительно регулируется расход флегмы путем изменения расхода хладагента, поступающего в дефлегматор. В лаб. практике применяют все способы Д. Конструкции приборов, изготовляемых обычно из стекла, весьма разнообразны и выбор их определяется гл. обр. физ.-хим. свойствами, и количеством разделяемой смеси. Для Д. смесей в количествах от неск. мг до 1 г используют капилляры, трубки с шарообразными расширениями и маленькие колбы. При большем количестве исходной смеси применяют, как правило, аппараты в виде колб соответствующих размеров. Типичная лаб. установка для Д. при атм. давлении показана на рис. 3. Простую Д. используют в хим., лесохим., фармацевтич. и др. отраслях промышленности для грубого разделения смесей на фракции, когда не предъявляются высокие требования к чистоте получаемых продуктов, а также для очистки жидких смесей от нелетучих или малолетучих примесей; в металлургии — для отгонки из руд или рудных концентратов летучих металлов (напр., Hg и Zn). Д. с дефлегмацией применяют в нефтепереработке и лаб. практике, Д. с водяным паром — в хим., нефтехим., парфюм. и др. отраслях промышленности для отгонки высококипящих компонентов из вязких смесей, содержащих значит. количества твердых или малолетучих жидких веществ.
Молекулярная дистилляция. Основана на зависимости скорости испарения вещества от его мол. массы при температурах ниже температуры кипения жидкости и низких давлениях (< 0,13 Па). При таких давлениях длина своб. пробега молекул соизмерима с расстоянием между поверхностями испарения жидкости и конденсации пара. При этом молекулы соударяются относительно редко и движутся практически независимо друг от друга, а расход и состав паровой смеси определяется скоростями испарения отдельных компонентов. Скорость испарения чистого вещества с мол. массой М при температуре T рассчитывается по уравнению Кнудсена — Ленгмюра:
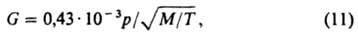
где р — давление пара вещества при температуре жидкости. Скорость испарения компонента смеси меньше, чем чистого вещества, и пропорциональна его мол. доле в смеси. При этом:
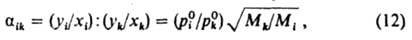
т. е., в отличие от условий разделения смесей с помощью обычной Д., αik зависит не только от давлений паров чистых компонентов при температуре процесса, но и от их мол. массы. Это позволяет разделять смеси, используя различие мол. масс компонентов при относительно низких температурах. Процесс включает перенос молекул испаряющегося компонента из объема жидкости к поверхности испарения, испарение молекул, перенос их в объеме паровой фазы от поверхности испарения к поверхности конденсации и конденсацию. Поскольку при молекулярной Д. жидкость не кипит, перемешивание паровыми пузырями, характерное для обычной Д., отсутствует, и перенос вещества в объеме жидкости осуществляется преим. путем мол. диффузии. Т. к. этот процесс более медленный, чем испарение с поверхности, жидкость со стороны поверхности обедняется относительно более летучими компонентами и в ней возникает градиент концентраций, что ухудшает условия разделения смеси. Для предотвращения этого уменьшают толщину слоя жидкости и обеспечивают ее перемешивание. Скорость испарения молекул с поверхности жидкости определяется ее температурой: чем она выше, тем больше давление пара и скорость испарения. Однако при увеличении давления пара уменьшается длина своб. пробега молекул и возрастает частота их соударений, что приводит к снижению эффективности разделения смеси. С целью ее повышения Д. проводят при давлениях более высоких, чем те, при которых молекулы достигают поверхности конденсации без соударений. Каждой смеси отвечает определенная оптим. температура, при которой достигается наиб. степень разделения. Для оценки последней используют представление о теоретич. мол. тарелке, под которой понимается устройство, обеспечивающее получение дистиллята с относит. содержанием компонентов, соответствующим соотношению скоростей их испарения при данной температуре, а состав жидкости во всем ее объеме одинаков, т. е. жидкость идеально перемешана. В производств. условиях при однократном испарении степень разделения колеблется от 0,3 до 0,95 теоретич. тарелки. Конденсация на охлаждаемой поверхности не является лимитирующей стадией процесса, т. к. температура этой поверхности поддерживается как минимум на 30–40 °C ниже температуры жидкости.
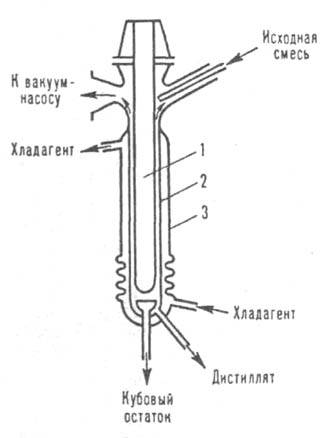
Рис. 4. Аппарат для молекулярной дистилляции. 1,2 — внутренняя обогреваемая и внешняя охлаждаемая трубки; 3 — рубашка.
В аппарате для молекулярной Д. (рис. 4) исходная смесь распределяется в виде пленки на наружной поверхности внутр. трубки, которая обогревается подаваемым в нее теплоносителем. На расстоянии 10–30 мм от этой трубки находится трубка, снабженная рубашкой, в которую подается хладагент. Кубовый остаток и дистиллят, полученный на охлаждаемой поверхности, отводятся снизу. Для поддержания требуемого остаточного давления рабочее пространство аппарата соединено с вакуумной системой. По способу создания пленки различают аппараты со стекающей жидкостью и центробежные (пром. — с ротором диаметром до 3 м), позволяющие перерабатывать за 1 ч от микроколичеств до 1 т смеси. Для повышения эффективности разделения дистилляц. аппараты могут снабжаться двумя или более конденсаторами, работающими при разл. температурах, что дает возможность разделять смесь на неск. фракций. Применяют также многоступенчатые противоточные аппараты, степень разделения смеси в которых во много раз больше, чем в одноступенчатых. Рабочие параметры процесса: контролируемые — расход исходной смеси, скорость отгонки дистиллята, температура испаряющейся жидкости, температура хладагента, используемого для охлаждения поверхности конденсации, и давление, регулируемые — расходы исходной смеси, теплоносителя и хладагента. В лабораториях используют периодическую Д. для разделения небольших количеств (несколько мг) смесей термически стойких веществ и непрерывную Д. для перегонки значит. количеств (десятки и сотни г) термолабильных веществ. В первом случае аппаратом обычно служит обогреваемая колба с внутренним или выносным конденсатором, во втором — цилиндрич. испаритель (трубка) с конденсатором, снабженным охлаждающей рубашкой. Молекулярную Д. применяют для разделения и очистки смесей малолетучих и термически нестойких веществ, напр., при выделении витаминов из рыбьего жира, растит. масел и в производстве вакуумных масел.
• см. также дистилляция нефти, ректификация
Лит.: Коган В. Б., Теоретические основы типовых процессов химической технологии, Л., 1977; Гельперин Н. И., Основные процессы и аппараты химической технологии, кн. 1–2, М., 1981.
В. Б. Коган
Значения в других словарях
- ДИСТИЛЛЯЦИЯ — (от лат. distillatio — отекание каплями) (перегонка), разделение жидких смесей, основанное на различии темп-р кипения компонентов смеси или на различии их скоростей испарения. Для Д. создаются условия, при к-рых один из компонентов переходит в пар, к-рый затем конденсируется. Физический энциклопедический словарь
- дистилляция — Перегонка, разделение жидких смесей на отличающиеся по составу фракции; основана на различии в температурах кипения компонетов смеси. Микробиология. Словарь терминов
- дистилляция — -и, ж. Действие по знач. глаг. дистиллировать. Малый академический словарь
- дистилляция — Дистилл/я́ци/я [й/а]. Морфемно-орфографический словарь
- Дистилляция — (от лат. distillatio — стекание каплями) перегонка, разделение жидких смесей на отличающиеся по составу фракции. Процесс основан на различии температур кипения компонентов смеси. Большая советская энциклопедия
- дистилляция — орф. дистилляция, -и Орфографический словарь Лопатина
- ДИСТИЛЛЯЦИЯ — ДИСТИЛЛЯЦИЯ, извлечение жидкости путем кипячения раствора, в котором она содержится, с последующим охлаждением паров для их конденсации и сбора. Научно-технический словарь
- дистилляция — Перегонка, процесс нагревания жидкости с последующим охлаждением и конденсацией паров с целью получения более чистого, рафинированного продукта. *** Кулинарный словарь
- Дистилляция — (лат. destillatio и distillatio стекание каплями; син. перегонка) процесс очистки жидкости от растворенных в ней нелетучих примесей или разделения смесей жидкости на фракции путем испарения и последующей конденсации образующихся паров; широко применяется в фармацевтической и лабораторной практике. Медицинская энциклопедия
- дистилляция — ДИСТИЛЛЯЦИЯ -и; ж. [лат. distillatio — стекание каплями] Очищение жидкости от растворимых летучих веществ, изменение концентрации раствора, разложение жидкой смеси на фракции, осуществляемые путём нагрева или кипячения жидкого вещества. ◁ Дистилляционный, -ая, -ое. Толковый словарь Кузнецова
- дистилляция — См. дистиллировать Толковый словарь Даля
- дистилляция — [< лат. distillatio стекание каплями] – перегонка жидкости с целью очищения, изменения концентрации раствора и пр. Большой словарь иностранных слов
- дистилляция — ДИСТИЛЛ’ЯЦИЯ (или дестилляция), дистилляции, мн. нет, ·жен. (спец.). Действие по гл. дистиллировать. Толковый словарь Ушакова
- дистилляция — дистилляция ж. 1. Разделение жидких смесей на различающиеся по составу фракции; перегонка. 2. перен. Искусственное очищение ото всего излишнего. Толковый словарь Ефремовой
- ДИСТИЛЛЯЦИЯ — ДИСТИЛЛЯЦИЯ (от лат. distillatio — стекание каплями) (перегонка) — разделение многокомпонентных жидких смесей на отличающиеся по составу фракции; основано на различии в составах жидкости и образующегося из нее пара. Большой энциклопедический словарь
