азирины
АЗИРИНЫ
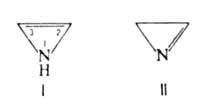
Существуют в виде двух изомеров: 1Н-А. и 2Н-А. (соотв. формулы I и II). В отличие от хорошо изученного 2Н-А. и его производных, 1Н-А. известны лишь в виде интермедиатов или побочных продуктов, напр. в реакциях присоединения нитренов к алкинам, вакуумного пиролиза триазолинов.
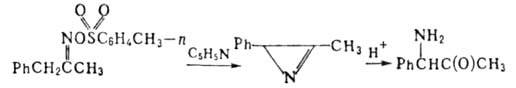
Большинство алкил- и арил-2Н-А. — нестабильные, дурно пахнущие, раздражающие кожу вещества. Не обладают основными свойствами и не раств. в разб. HCl; разлагаются конц. HCl. Катализируемый кислотами гидролиз 2Н-А. приводит к аминокетонам:
В безводной HClO4 производные 2H-А. ведут себя как карбкатионы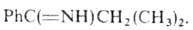 Присоединение хлор-ангидридов и ангидридов карбоновых кислот по связи
Присоединение хлор-ангидридов и ангидридов карбоновых кислот по связи дает N-ацил-2H — замещенные азиридины, которые в мягких условиях перегруппировываются в оксазолины или ациклич. соединения. Восстановление 2H-А. с помощью LiAlH4- удобный и стереоспецифич. синтез цис-азиридинов; каталитич. гидрирование (катализаторы — Pd/C, Ni-Ренея) сопровождается расщеплением связи
дает N-ацил-2H — замещенные азиридины, которые в мягких условиях перегруппировываются в оксазолины или ациклич. соединения. Восстановление 2H-А. с помощью LiAlH4- удобный и стереоспецифич. синтез цис-азиридинов; каталитич. гидрирование (катализаторы — Pd/C, Ni-Ренея) сопровождается расщеплением связи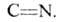 3-Арил- и 3-амино-2H-А. димеризуются под действием карбонилов металлов VI гр., давая производные пиррола или индола. Реакционноспособная двойная связь в 2H-А. легко участвует как 2
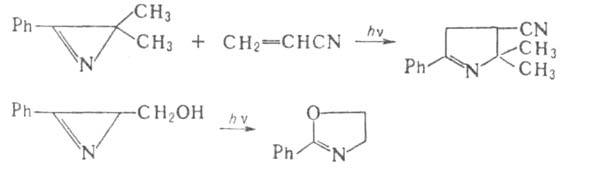
3-Арил- и 3-амино-2H-А. димеризуются под действием карбонилов металлов VI гр., давая производные пиррола или индола. Реакционноспособная двойная связь в 2H-А. легко участвует как 2 -компонента в диеновом синтезе. При фотолизе арил-2H-А. претерпевают необратимое раскрытие цикла с образованием 1,3-диполярных нитрил-илидов, которые легко вступают во внутри- или межмолекулярное 1,3-Диполярное циклоприсоединение, напр.:
-компонента в диеновом синтезе. При фотолизе арил-2H-А. претерпевают необратимое раскрытие цикла с образованием 1,3-диполярных нитрил-илидов, которые легко вступают во внутри- или межмолекулярное 1,3-Диполярное циклоприсоединение, напр.:
Термолиз 2H-А. сопровождается обычно раскрытием связи
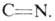
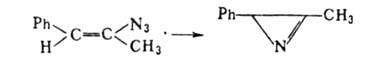
Общий метод синтеза 2H-А. — парофазный пиролиз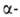 винил азидов при 100–120 °C или их фотолиз в атмосфере N2 при −30 °C, напр.:
винил азидов при 100–120 °C или их фотолиз в атмосфере N2 при −30 °C, напр.:
В связи с нестабильностью большинства 2H-А. реакции с ними проводят путем их генерирования в реакционной среде.
Лит.: Общая органическая химия, пер. с англ., т. 8, М., 1985, с. 687–97; Chemistry of hcterocyclic compounds, v. 42, pt 1, N.Y.-L., 1983.
