Пфицнера — Моффатта реакция
ПФИЦНЕРА — МОФФАТТА РЕАКЦИЯ
окисление спиртов в альдегиды или кетоны действием смеси ДМСО, дицикло-гексилкарбодиимида и фосфорной кислоты (реактив Пфиц-нера — Моффатта):
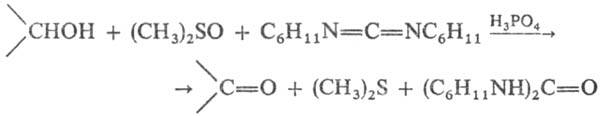
Для приготовления реактива используют безводные реагенты. Реакцию проводят в органическом растворителе (напр., в бензоле) или в его отсутствие при 20–100 °C.
С помощью П.-М. р. можно окислять спиртовые группы в алифатич. и жирно-ароматич. соед., сахарах, стероидах, пептидах, нуклеотидах и алкалоидах. Например, эта реакция м. б. использована для окисления остатков треонина в пептидах:
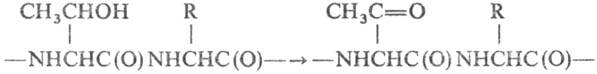
Реакция замедляется в случае экранирования группы OH объемными заместителями, третичные спирты в реакцию не вступают. Выход карбонильных соед. 70–90%.
Механизм П.-М. р. включает образование алкоксисульфониевой соли (формула I), ее разложение через промежут. илид (II):
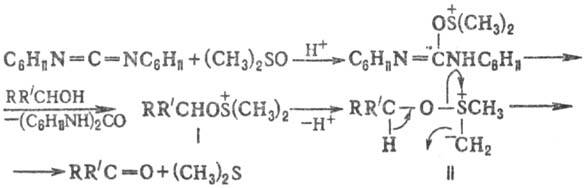
Известны многочисл. модификации реакции. Так, вместо H3PO4 в ряде случаев можно использовать H3PO3, CF3COOH, NCCH2COOH или соли кислот с орг. основаниями (напр., для окисления стероидов используют смесь C6H11N=C=NC6H11, CF3COOH∙C5H5N и ДМСО), а вместо дициклогексилкарбоднимида — диэтилкарбодиимид (образующаяся диэтилмочевина в отличие от дициклогек-силмочевины раств. в воде). Возможно также применение карбодиимидов на полимерном носителе, что позволяет устранить загрязнение продукта реакции производными мочевины.
П.-М. р. широко используют в препаративных целях. Она открыта в 1963 К. Пфицнером и Дж. Моффаттом.
Лит.: Физер Л., Физер М., Реагенты для органического синтеза, пер. с англ., т. 1, М., 1970, с. 328–31; там же, т. 5, М., 1971, с. 129–33; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 643–44; там же, т. 5, М., 1983, с. 270–73; Moffatt J., Oxidation, v. 2, ch. 1, N.Y., 1971, p. 1–46.
Г. И. Дрозд
